Основной причиной возникновения этого варианта ацидоза служит нарушение тканевого метаболизма с образованием избыточного количества нелетучих эндогенных кислот (лактоацидоз, кетоацидоз). При нарушениях доставки кислорода метаболизм клеток перестраивается на путь анаэробного гликолиза с внутриклеточным накоплением ионов водорода за счет образования органических и неорганических кислот. Метаболический ацидоз часто связан с первичным нарушением обмена веществ, например, при диабете, голодании, лихорадке, при гипоксии вследствие нарушений кровообращения.
Лактатный ацидоз развивается при избыточном образовании молочной кислоты или снижении ее выведения из крови. Наиболее частой причиной его является нарушение процессов анаэробного окисления при гипоксии тканей у больных, находящихся в послеоперационном периоде, панкреатите, лейкозах, анемиях. Ацидоз активирует клеточные катепсины, усиливается распад белков, увеличивается содержание свободных аминокислот в крови. Лактатный ацидоз при нарушениях периферического кровотока может быть осложнением кетоацидоза.
Лактат образуется при анаэробном метаболизме глюкозы. При соответствующих условиях практически все ткани могут продуцировать молочную кислоту. Чаще всего лактоацидоз бывает транзиторным при шоке, послеоперационной травме, при интенсивной физической нагрузке, во время которой имеет место дисбаланс между доставкой кислорода и потребностью в нем сокращающихся мышц. Печень и, в меньшей степени, почки утилизируют лактат, используя его в энергетическом обмене или превращая его обратно в глюкозу. В большинстве клинических случаев лактоацидоз связан с неадекватным обеспечением тканей кислородом, как при шоке или остановке сердца. При таких условиях повышена продукция молочной кислоты и уменьшен ее клиренс из-за плохой перфузии печени. У пациентов с декомпенсированным лактоацидозом при шоке с выраженной тканевой гипоксией отмечают высокий процент летальных исходов.
Лактоацидоз может быть связан с нарушениями, при которых отсутствует гипоксия тканей. Такие варианты ацидоза описаны у пациентов с лейкозами, лимфомами, лимфогранулематозом и другими злокачественными новообразованиями, некорригированным диабетом, тяжелой печеночной недостаточностью. Механизмы, вызывающие ацидоз при этих состояниях, недостаточно ясны. При новообразованиях может локально повышаться тканевой метаболизм с продукцией лактата или может возникать препятствие кровотоку к некарциноматозным клеткам. В большинстве случаев отмечается обширное опухолевое поражение печени. Возможно, именно нарушение функции печени обусловливает накопление лактата в крови. Лактацидоз также часто развивается при нераспознанной ишемии или инфаркте кишечника, а также у больных с сердечной недостаточностью, получающих сосудосуживающие средства.
Различные лекарственные средства, ингибирующие функции митохондрий, также могут вызывать угрожающий жизни лактат ацидоз. К препаратам, способным оказывать такой эффект, относятся бигуаниды, использующиеся для лечения сахарного диабета и противовирусные нуклеозидные аналоги, используемые для лечения синдрома приобретенного иммунодефицита (AIDS).
Лактацидоз может наблюдаться при нарушении доставки и утилизации кислорода тканями (шок, сердечная недостаточность, тяжелая анемия, дефекты митохондриальных ферментов или ингибирование их окисью углерода и цианидами), а также при избыточном образовании или недостаточной утилизации L-лактата (гликогенозы, эпилептические припадки, сахарный диабет, алкогольная интоксикация. Этанол вызывает легкое повышение молочной кислоты, но при алкогольной интоксикации клинически значимый лактат ацидоз не развивается, если нет другихосложнений, таких как печеночная недостаточность., печеночная недостаточность, злокачественные новообразования).
Лактацидоз может быть обусловлен накоплением в крови D-лактата (продукта метаболизма бактерий кишечника) при синдроме слепой петли и кишечной непроходимости. В этих случаях неабсорбированные углеводы попадают в толстую кишку, где он превращаются в D-молочную кислоту при чрезмерно быстром росте грам-положительных анаэробов. У таких пациентов периодически возникают эпизоды метаболического ацидоза, к которым приводит употребление пищи, богатой углеводами. Проявления включают спутанность сознания, церебральную атаксию, невнятность речи и провалы памяти. У них могут появляться симптомы интоксикации. Лечение включает использование антимикробных препаратов для снижения числа D-лактат продуцирующих микроорганизмов в кишке наряду с диетой, содержащей ограниченное количество углеводов.
Лактоацидоз также может быть связан с наследственными нарушениями метаболизма: дефицитом глюкозо-6-фосфатазы или другими врожденными заболеваниями с дефектом глюконеогенеза или окисления пирувата. Лактоацидоз может развиваться при ослаблении оксидативного метаболизма в митохондриях. Лактоацидоз описан при генетических митохондриальных нарушениях, при которых идет процесс накопления молочной кислоты. Одно из подобныхзаболеваний, именуемое MELAS, включает митохондриальную энцефалопатию (МЕ), лактат ацидоз (LA) и эпизоды подобные инсультам (S). Дети с этой патологией на протяжении первых лет жизни жалоб не предъявляют, но затем начинают проявляться нарушения моторного и конгитивного развития. Митохондриальные дефекты также приводят к замедлению роста, припадкам и повторным инсультам. При проведении терапии снижение уровня молочной кислоты в плазме у детей с тяжелым лактат ацидозом может приводить к выраженному клиническому улучшению.
При нормальной функции печени происходит самостоятельная компенсация лактатного ацидоза, так как 50% его утилизируется в печени.
Клиническая картина тяжелого лактацидоза характеризуется угнетением сознания (от оглушения до сопора), тахикардией, гипотензией, частым глубоким «ацидотическим» дыханием, нарушением периферического кровообращения, и, часто, олиго-или анурией. При ацидозе развивается резистентность к сосудосуживающему действию катехоламинов, что приводит к развитию стаза и нарушению микроциркуляции, усугубляющим гипоксию. Уменьшение рН менее 7,2 может привести к снижению сердечного выброса.
Под влиянием гипоксии и ацидоза повышается уровень кининов в плазме и внеклеточной жидкости, что вызывает вазодилатацию и резкое повышение проницаемости сосудистой стенки. Усиление катаболизма при ацидозе ведет к гипергидратации за счет увеличения продукции эндогенной воды. В связи с тем, в экскрецию протонов вовлекаются слизистые ЖКТ и дыхательных путей, то возможно развитие ацидотического ларинготрахеобронхита, бронхиолита и альвеолита, гастроэзофагита с продолжительным кашлем, рвотой, иногда с примесью крови.
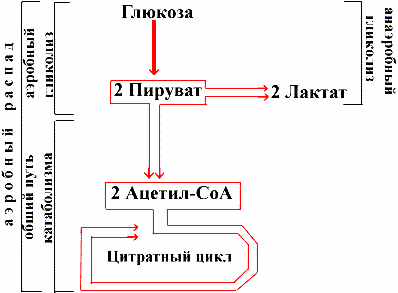
Рис.10. Схема лактоацидоза.
Кетоацидоз развивается при неполном окислении свободных жирных кислот, образующихся в избытке при усиленном липолизе и уменьшении образования в печени триглицеридов из-за низкой активности фермента ацилкарнитинтрансферазы.. Кетокислоты (ацетоуксусная и β-оксимасляная), образующиеся в печени из жирных кислот, являются источником энергии во многих тканях организма. Гиперпродукция кетокислот имеет место при недостаточном запасе углеводов или невозможности использования имеющихся доступных углеводов в энергетическом обмене. В этих условиях жирные кислоты мобилизуются из жировой ткани и поступают в печень, где превращаются в кетоны.Кетоацидоз развивается тогда, когда продукция кетонов превышает возможность их использования тканями.
Наиболее частая причина кетоацидоза – декомпенсированный сахарный диабет.
Диабетический кетоацидоз (ДКА) занимает первое место среди острых осложнений эндокринных заболеваний. Смертность при ДКА достигает 6-10%. При диабетическом кетоацидозе в крови накапливаются кетокислоты: ацетоацетат и β-гидроксибутират. ДКА возникает вследствие абсолютного или относительного дефицита инсулина, который может развиваться за несколько часов или дней.
У больных, получающих инъекции инсулина, причинами ДКА могут быть:
– назначение неадекватных (слишком низких) доз инсулина;
– нарушение режима инсулинотерапии;
– резкое возрастание потребности в инсулине: инфекционные заболевания (сепсис, в особенности уросепсис, пневмония., другие инфекции дыхательных и мочевых путей, менингит, синусит, холецистит, панкреатит и др.), сопутствующие эндокринные нарушения (тиреотоксикоз, синдром Иценко-Кушинга, акромегалия, феохромоцитома), инфаркт миокарда, инсульт, травмы, хирургические вмешательства, медикаментозная терапия (глюкокортикоиды, эстрогены, в том числе пероральные контрацептивы), беременность, стрессы (во всех этих случаях увеличение потребности в инсулине обусловлено увеличением концентрации контринсулярных гормонов – адреналина, кортизола, глюкагона и СТГ, а также резистентностью тканей к инсулину).
Вследствие нарастающего дефицита инсулина в организме происходит обеднение печени гликогеном, увеличение гликонеогенеза, и понижение утилизации глюкозы тканями. Нарастанию дефицита инсулина в немалой степени способствует и одновременно происходящее уменьшение количества рецепторов и их чувствительности к инсулину и в периферических тканях. Это приводит к значительной гипергликемии и глюкозурии. Развитие гипергликемии обусловлено не только дефицитом инсулина в организме, но и избыточной секрецией глюкагона, стимулирующего гликонеогенез и гликогенолиз. Вследствие гипергликемии увеличивается осмотическое давление во внеклеточной жидкости и развивается процесс клеточной дегидратации. Уменьшение содержания гликогена в печени обусловливает усиление мобилизации жира из депо с последующим поступлением его в печень. Это в конечном итоге приводит к жировой инфильтрации печени, а в последующем – к кетозу, который усугубляет дефицит инсулина. Следствием гиперкетонемии и кетонурии является нарушение водно-солевого обмена – понижение содержания натрия, фосфора, кальция, калия, магния и хлоридов в крови. Уровень калия в крови вначале повышен, а затем понижен, что связано с усиленным выведением его с мочой. Иногда возможна ранняя гипокалиемия, которая обусловлена массивной деструкцией клеток, потерей ими калия и интенсивной экскрецией его с мочой. Это, в свою очередь, ведет к дегидратации и сдвигу КОС в сторону ацидоза
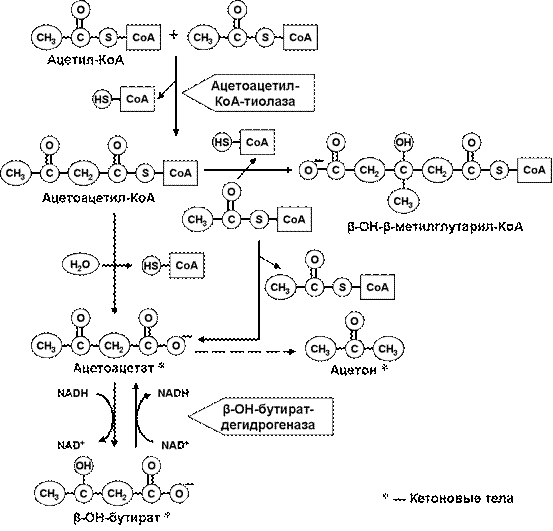
Рис.11. Механимз развития кетоацидоза.
Роль контринсулярных гормонов:
– адреналин, кортизол и СТГ подавляют опосредованную инсулином утилизацию глюкозы мышечной тканью;
– адреналин, глюкагон и кортизол усиливают гликогенолиз и глюконеогенез;
– адреналин и СТГ усиливают липолиз и подавляют остаточную секрецию инсулина.
Самые частые симптомы – полидипсия, полиурия, слабость; выраженность этих симптомов зависит от степени и продолжительности гипергликемии. Больные могут жаловаться на отсутствие аппетита, тошноту, рвоту, связанные с кетонемией боли в животе, которые могут имитировать различные хирургические заболевания. Гипокалиемия и гипокалигистия может вызвать атонию гладкой мускулатуры желудочно-кишечного тракта, и, как следствие – кишечную непроходимость и острое расширение желудка, что приводит к тяжелой рвоте.
Характерна также гипервентиляция за счет увеличения глубины дыхания, при падении рН ниже 7,2 обычно возникает дыхание Куссмауля, сопровождающееся запахом ацетона. Часто возникает тахикардия. При отсутствии выраженной дегидратации гипотония отсутствует. Обычно наблюдается гипотермия. Может отмечаться гипорефлексия, вызванная гипокалиемией. При тяжелом течении диабетического кетоацидоза наблюдаются артериальная гипотония, сопор, кома.
Другая причина кетоацидоза – 2 стадия голодания. Со 2-го – 3-го дня полного голодания в связи с мобилизацией больших количеств жира из депо и образованием кетоновых тел возникает транзиторный кетоз, не требующий лечения, так как в условиях гипогликемии и гипоинсулинемии клетки начинают использовать кетоны в качестве основного энергетического субстрата. Могут проявляться признаки ацидоза – головная боль, головокружение, тошнота, слабость, инсомния. При лечебном голодании в этом случае назначают энтерально щелочные растворы.
Алкогольный кетоацидоз наступает у больных хроническим алкоголизмом после резкого прекращения приема этанола. Обычно он обусловлен рвотой, недостаточным питанием вследствие анорексии, гиповолемией (уменьшением объема внеклеточной жидкости). При острых алкогольных интоксикациях и хроническом алкоголизме также могут активироваться процессы β-окисления жирных кислот. Вследствие увеличения соотношения НАДФ/НАД в крови накапливаются кетоновые тела, преимущественно β-гидроксибутират (по этой же причине возможен незначительный лактоацидоз), который затем превращается в ацетоуксусную кислоту.
Нарушения КОС при метаболическом ацидозе обусловлены перемещением ионов из клетки в интерстициальный сектор и обратно. Более 90% перемещений касаются ионов калия, натрия, хлора, водорода, бикарбоната.
В ответ на повышение концентрации протонов плазмы крови и, соответственно, уменьшение значения рН, избыток протонов связывается бикарбонатным и белковым буферными системами. Ионы водорода перемещаются внутрь клетки, где белковый (в т.ч. гемоглобиновый) буфер является акцептором протонов. Высвобождаемый буфером калий выходит в плазму (феномен биологической травмы клеток), возникает транзиторная гиперкалиемия с сопутствующей прогрессирующей гипокалигистией. Калий интенсивно выводится с мочой, суточная гиперкалийурия может превышать норму в 4-5 раз. За счет этого в течение 4-5 дней при условиях наличия ацидоза содержание калия в плазме нормализуется, затем развивается гипокалиемия.
На каждые 3 иона калия, выходящего из клетки, в нее перемещаются 2 иона натрия и один ион водорода (трансминерализация клетки). Это приводит к усугублению клеточного ацидоза и перестройке ферментных систем. Гипернатриемия вызывает клеточную гипергидратацию.
Механизмы компенсации при метаболическом ацидозе направлены на уменьшение концентрации ионов водорода и осуществляются вне- и внутриклеточными буферными системами, легкими и почками. В плазме снижается содержание бикарбоната за счет истощения бикарбонатного буфера.
Повышение концентрации протонов вызывает стимуляцию дыхательного центра, развивается гипервентиляция и тахипноэ, рСО2 внеклеточной жидкости снижается до тех пор, пока не станет достаточным для выравнивания Н2СО3/НСО3- (при снижении НСО3- на 2 мЭкв/л рСО2 компенсаторно снижается на 1,3 мм рт.ст.). При снижении рН менее 7,2 может развиваться дыхание Куссмауля. Однако дыхательная компенсация не может полностью нормализовать концентрацию протонов, так как именно высокий уровень [Н+] стимулирует дыхательный центр. Кроме того, усиленная работа дыхательной мускулатуры способствует дополнительному образованию углекислого газа. В случае несостоятельности респираторных механизмов (заболевания органов дыхания, нарушения центральной регуляции дыхания и др.) быстрая компенсация невозможна, развивается тяжелый смешанный ацидоз с резким уменьшением рН и почти неизмененным содержанием бикарбоната.
Почечный механизм компенсации метаболического ацидоза включается позднее, спустя 16-18 часов от начала воздействия повреждающего фактора. Механизм направлен на усиление экскреции протонов и играет важную роль только у больных с неизмененной функцией почек. В почках усиливаются процессы ацидо- и аммониогенеза, а также восполнения дефицита бикарбоната плазмы за счет его образования и реабсорбции. Усиленная реабсорбция ионов бикарбоната приводит к активной экскреции хлора (ионы НСО3ˉ Сl- являются реципрокными), развивается гипохлоремия.
В печени активируются процессы дезаминирования аминокислот, вовлекаются в метаболизм лактат и пируват, тем самым уменьшается уровень кислореагирующих продуктов.
Лабораторные показатели метаболического ацидоза
- снижение рН плазмы
- уменьшение значений рСО2, АВ, SВ, ВВ
- сдвиг ВЕ в отрицательную сторону
- резкое снижение рН мочи (ниже 4,0)
- гиперкалиемия (в начальной стадии), сменяющаяся в последующем гипокалиемией
- гипохлоремия
- гипернатриемия
Терапия метаболического ацидоза включает прежде всего устранение причин, приводящих к дыхательной гипоксии (борьба с гиповентиляцией, оксигенотерапия, вспомогательное дыхание, при необходимости – интубация и перевод больного на ИВЛ).
Следующим важным моментом является борьба с расстройствами кровообращения (ликвидация гиповолемии, анемии, улучшение реологических свойств крови, микроциркуляции, лечение сердечной недостаточности).
Внутривенно вводя щелочные растворы: бикарбонат натрия, лактат натрия, лактасол, трисамин, ацесоль. Бикарбонат натрия применяют при тяжелом ацидозе (рН ниже 7,2) для улучшения сократимости миокарда и повышения утилизации лактата. Однако, поскольку бикарбонат натрия активирует фосфофруктокиназу, то при его применении возможно парадоксальное усугубление ацидоза за счет увеличения продукции лактата.
Расчет количества бикарбоната натрия производят по формуле дефицита буферных оснований (ДБО).
ДБО = 0,3 ВЕ масса тела (ммоль)
Вопрос о применении щелочных растворов при умеренном ацидозе до сих пор не решен. Введение бикарбоната натрия может приводить к артериальной гипертензии и отеку легких в связи с повышением тонуса вен и олигурией. Если удается устранить причину ацидоза,.то введение бикарбоната может привести к развитию алкалоза.
До сих пор не решен вопрос о целесообразности применения бикарбоната для устранения ацидоза при ДКА, так как при его использовании возникают нежелательные эффекты:
– При ДКА из-за потери фосфора снижается уровень 2,3-дифосфоглицерата в эритроцитах, и в результате кривая диссоциации оксигемоглобина сдвигается влево (кислород прочнее связывается с гемоглобином). Ацидоз сдвигает кривую диссоциации вправо (эффект Бора), так что снабжение тканей кислородом не нарушается. Бикарбонат вновь сдвигает кривую диссоциации влево, и ткани получают меньше кислорода.
– При правильном лечении (инфузионная терапия плюс инсулин) кетоновые тела превращаются в бикарбонат и введение дополнительного бикарбоната может вызвать алкалоз.
– Имеющиеся в продаже растворы бикарбоната гиперосмолярны и могут увеличивать и без того высокую осмоляльность плазмы.
– Лечение бикарбонатом может вызвать неврологические осложнения - от спутанности сознания до комы. Анионы HCO3-, соединяясь с ионами H+, образуют угольную кислоту. При ее диссоциации образуются CO2 и вода. CO2 легко проникает через гематоэнцефалический барьер и вызывает закисление спинномозговой жидкости (сам бикарбонат в нее практически не проникает). Поэтому нормализация pH плазмы может сопровождаться парадоксальным ацидозом в ЦНС, который и приводит к неврологическим нарушениям.
Применение бикарбоната оправдано в следущих случаях:
– если ДКА осложняется тяжелым лактацидозом;
– если имеется тяжелый ацидоз (pH менее 6,9), особенно осложненный шоком, который не поддается инфузионной терапии, направленной на повышение сердечного выброса (0,9% раствор NaCl, плазма, альбумин).
При повышении pH до 7,1-7,15 бикарбонат отменяют.
Трисамин используется при избытке в крови натрия и неизменной функци почек. Эффект трисамина основан на свободном проникновении препарата в клетку и коррекции внутриклеточного ацидоза. Имеет побочные дейсвия: способствует миграции калия из клетки, может вызвать гипогликемию и гипокальциемию.
Расчет производят по формуле:
Кол-во р-ра= масса тела (кг) ВЕ
Реже используется лактат. Его использование будет эффективным, если у больного сохранены окислительные процессы в клетке. Если имеется гипоксия, то в крови будет накапливаться молочная кислота.
Одна из важных проблем лечения метаболического ацидоза – коррекция электролитных нарушений, в частности обмена калия и хлора. По мере устранения ацидоза путем инфузионной терапии и введения инсулина при ДКА калий поступает обратно в клетки и его уровень в сыворотке снижается, что может вызвать гипокалиемию. Гипокалиемия вызывает тяжелые осложнения (например, угрожающие жизни желудочковые аритмии). Если нет задержки мочи, восполнение калия начинают одновременно с инфузионной терапией. Если уровень калия исходно повышен, его назначают только после того, как его концентрация в сыворотке нормализуется. Дозы калия корректируют на основании данных ЭКГ и клинических и лабораторных показателей гипокалиемии
У мужчины 22 лет, в течение 15 лет страдающего инсулин-зависимым сахарным диабетом, в течение трех дней были тошнота и рвота. Он жаловался на выраженную жажду и частое мочеиспускание. У пациента наблюдалось дыхание Куссмауля.
рН 7,15
рО2 94 мм Hg
рСО2 25 мм Hg
SB 6,8 ммоль/л
ВВ 25,0 ммоль/л
ВЕ -23,0
Уровень глюкозы в крови 23,0 ммоль/л.
Клинические и лабораторные данные типичны для диабетического кетоацидоза в стадии декомпенсации. Низкая концентрация бикарбоната, выраженный сдвиг буферных оснований в отрицательную сторону, гипервентиляция с резким снижением рСО2 свидетельствуют о наличии метаболического ацидоза с частичной дыхательной компенсацией.
 2015-10-13
2015-10-13 4679
4679
