Согласно законам Фарадея:
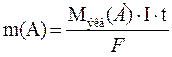 , (1)
, (1)
где m(А) - масса вещества, окисленного или восстановленного на электроде (г); Mэкв(А) – молярная масса эквивалента вещества А (г/моль·экв); I – сила тока (А); t – продолжительность электролиза (с); F – число Фарадея (F ≈ 96500 Кл/моль).
Молярная масса эквивалента меди равна
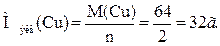
Подставив в формулу ( 1 ) значения Mэкв(Cu), получим:
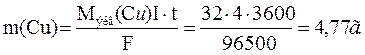
Пример 2. Вычислите молярную массу эквивалента металла, зная, что при электролизе раствора хлорида этого металла затрачено 3880 Кл электричества и на катоде выделилось 11,742 г металла.
 2015-10-14
2015-10-14 434
434








