План
1. Загальні відомості про процес.
2. Рівновага фаз.
3. Основне рівняння масопередачі.
4. Загальні відомості про процес адсорбції.
5. Види адсорбентів.
1. Масообміни – це процеси, сутність яких складає перенос речовини з однієї фази в іншу.
Кожна речовина складається з фаз.
Фаза – це визначна кількість речовини, однорідної за всією масою.
Системи можуть бути однофазними (вода у вигляді рідини), двофазними (вода та її пара) та багатофазними (вода, крига та пара).
Фази у системі відокремлюються одна від одної поверхнями розділу.
Системи, які складаються з декількох фаз, називаються гетерогенними або неоднорідними.
Перехід речовини з однієї фази в іншу при масообміні здійснюється шляхом дифузії.
2. Основною умовою протікання масо обмінного процесу є порушення рівноваги між фазами, яке може відбутися при зміні температури (t), тиску (Р) або складу хоча б однієї з фаз. Процес при цьому буде проходити до тих пір, поки знову не встановлюється рівновага.
Для того, щоб процес протікав, фази повинні бути приведені в контакт, і чим більше поверхня контакту фаз і концентрація відрізняється від рівноважної, тим більше буде швидкість масообмінного процесу. При наближенні системи до стану рівноваги рухома сила, а слід, і швидкість процесу зменшуються.
3. Кількість речовини, що продифундувала крізь деяку поверхню, може бути розрахована за допомогою рівняння масопередачі:
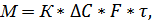
де: М – маса речовини, що переходе з однієї фази в іншу, кг;
К – кінематичний коефіцієнт, який враховує опір в процесі переносу;
∆С - середня різниця концентрації, кг/кг, кмоль/кмоль, кг/м3 тощо;
F – площина між фазової поверхні, крізь яку здійснюється перенос речовини, м2;
τ – тривалість процесу, с.
Коефіцієнт масопередачі. Розмірність його залежить від розмірності, прийнятої для концентрації. Наприклад, якщо
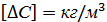 , то
, то 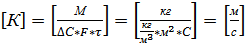
якщо кг/кг
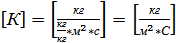
Фізична сумісність коефіцієнта К: коефіцієнт масопередачі показує, яка кількість речовини переноситься крізь 1м2 поверхні фазового розділу за 1 с при різниці концентрацій = 1.
К не залежить від площини поверхні, часу і концентрацій. Він залежить від властивостей речовин, які приймають участь у процесі, та характеру взаємодіє фаз.
4. Адсорбція – процес вибіркового поглинання компонента газу, пари або розчину поверхнею твердої речовини.
Для того, щоб процес був ефективним, поверхня поглинання повинна бути великою. Тому для адсорбції застосовують пористі речовини, які володіють величезною поверхнею.
Тверде тіло, на поверхні пор якого конденсується вбирана речовина, називається адсорбентом, вбирана речовина – адсорбтивом, вона ж у концентрованому вигляді на повехні адсорбенту – адсорбентом.
Розрізняють фізичну адсорбцію та хімічну (хемосорбцію).
Фізична адсорбція пояснюється взаємним притяганням молекул адсорбенту і адсорбтиву. При цьому не виникає хімічної взаємодії. Фізична адсорбція оборотня, при зміненні умов (t, Р) процес може розвиватися у протилежному напрямку і виникає десорбція – виділення раніше адсорбованої речовини з адсорбенту.
У випадку хемосорбції між молекулами адсорбенту та адсорбтиву відбувається хімічна реакція та виникає хімічний зв’язок.
В харчовій промисловості адсорбція застосовується на стабілізації вин, освітленні соків у консервному виробництві, рафінації рослинної олії, стабілізації пива.
5. Адсорбенти повинні володіти надзвичайно розвинутою поверхнею, що досягається за рахунок утворення великої кількості пор в твердому тілі.
1) Активоване вугілля – найбільш поширений адсорбент. Активна поверхня 1 г активованого вугілля складає від 600 до 1700 м2. Розміри частинок активного вугілля від 1 до 5 мм.
Переваги: краще поглинає пари органічних речовин, ніж пари води.
Недоліки: мала механічна міцність та горючість.
2) Костяне вугілля – його отримують із знежирених кліток крупних тварин шляхом пропікання їх в реостатах без допуску повітря. Розмір частинок приблизно 3 мм. Поверхня пор вкрита дуже тонким шаром вуглецю, який має дуже високу адсорбційну поверхню.
3) Силікагель – зневоднений гель кремнієвої кислоти. Розмір гранул від 0,2 до 7 мм. Сумарна площа поверхні 1 г – 400-770 м2. Селікагелі здатні поглинати до 50 % свої маси.
Переваги: поглинає пари органічних речовин, вологу з повітря та газів. Негорюч, має велику механічну міцність.
Також застосовують штучні адсорбенти: цеоліти, іоніти (аніоніти та катіоніти).
В якості природних адсорбентів в харчовій промисловості (для освітлення вин) застосовують дрібнодисперсні глини, бетоніт, каолін. Також застосовують риб’ячий клей (желатин).
4) Целюлозна маса має меншу питому поверхню, ніж вугілля і силікагель. Застосовується при освітленні соків і пива.
Д/з [1] c. 237-241, [2] c. 240-242.
Абсорбція
План
1. Теоретичні відомості про процес
2. Абсорбери
1. Абсорбцією називають процеси поглинання газів або пари рідиною. Для більшості випадків цей процес оборотний, тобто в певних умовах, наприклад при нагріванні, можна виділити газ з рідини. Такий процес називають десорбцією. Поєднання абсорбції і десорбції дозволяє створити безперервні промислові виробництва з багатократним використовуванням рідкого поглинача і виділенням в чистому виді речовини, поглиненої з парогазовой суміші. В харчових виробництвах процеси абсорбції займають значне місце. Наприклад, при виробництві спирту з що утворюється в результаті бродіння вуглекислого газу абсорбцією уловлюють пари спирту, а потім обчищений газ зріджують для використовування в інших виробництвах.Процес насичення мінеральної води і інших численних напоїв вуглекислим газом, в спеціальній технології званий сатурацией, насправді служить класичним прикладом процесу абсорбції.
Закон Генрі. Рівновага при абсорбції. Кількість газу, яка може
поглинути рідину, залежить від властивостей газу в рідині, температури і парціального тиску поглинального газу в газовій суміші над поверхнею абсорбції. Для прикладу розглянемо розділення бінарної газової суміші, що складається з компонентів А і В хай рідина поглинає компонент А. Определить число ступенів свободи для цієї системи, скориставшися правилом фаз
Ф + С = К + 2,
где Ф – число фаз;
С – число ступенів свободи;
К – число компонентов.
Для нашого прикладу Ф = 2, оскільки в процесі беруть участь дві фази: газ і рідина. Число компонентів До = 3, газові компоненти А і В і третій - поглинає рідину. Тоді число ступенів свободи З = 3 + 2 - 2 = 3
Три ступені свободи тут - три змінні параметри: температура, тиск і концентрація. Зміна будь-якого з них порушує сталу рівновагу. В стані рівноваги, при постійних температурах і загальному тиску, концентрації компоненту А в газовій суміші відповідає певна концентрація цього компоненту в рідині. Цей закон, відомий як закон Генрі, записується наступним рівнянням:
РА = УхА
тут замість концентрації компоненту А в газовій суміші у використовується пропорційне їй парціальний тиск цього компоненту в суміші РА, Па;
Е - коефіцієнт пропорційності, званий коефіцієнтом або
константою Генрі;
х - концентрація компоненту А в рідини, молярні частки.
Величина константи Генрі залежить від властивостей газу і рідини, їх температури і не залежить від загального тиску.Для ідеальних розчинів на діаграмі р - х залежність рівноважних концентрацій від тиску зображається прямою лінією з кутовим коефіцієнтом, рівним Е.
При незмінному загальному тиску і концентрації компоненту константа Е збільшується з підвищенням температури, що веде до зменшення розчинності газу в рідині.
Це слідство із закону Генрі демонструється кожного разу в побуті при підігріві води. З холодної води в каструлі, поставленій на вогонь, спочатку виділяються пухирці газу, які можна легко помітити на стінках каструлі. Подібно з свіжіше водопровідної води, налитої в стакан, інтенсивно виділяються гази, роблячи воду спочатку непрозорою. Це було пов'язано з різким зменшенням тиску у воді. В міській водопровідній мережі підтримується тиск на рівні (2...4) 105 а тиск води в стакані рівно атмосферному. Зменшення загального тиску веде до зменшення парціального тиску компонентів,
що відповідає закону Дальтона:
Р = РА + РВ
Общее давление газовой смеси равно сумме парциальных давлений составляющих смесь компонентов.
Из закона Дальтона следует, что парциальное давление компонента пропорционально общему давлению и его концентрации:
РА = РУА
Закон Генрі може бути представлений в наступному записі:
УА = mxA
Графічно рівняння є прямою, що проходить через початок координат у - х з кутовим коефіцієнтом т. Чисельне значення т і, отже, кут нахилу прямої рівноваги залежать від температури і тиску в системі. Із зростанням тиску m зменшується, а з підвищенням температури - збільшується. Відповідно розчинність газів збільшується із зростанням тиску і пониженням температури.
Якщо рівноважна система складається з рідини і суміші газів, закону Генрі може слідувати кожний з компонентів суміші окремо.Закону Генрі підкоряються гази, критичні температури яких вище за температуру розчину. З другого боку, закону Генрі справедливий для ідеальних розчинів і з достатньою точністю йому слідують сильно розбавлені розчини. Для систем що не підкоряються закону Генрі, коефіцієнт m в рівнянні - величина змінна, а криву рівноваги для них будують за досвідченими даними.
2. Абсорбери. В харчових виробництвах застосовують наступні групи абсорберів: з механічним перемішуванням, поверхневі, распылительные, плівкові і барботажные. На крупних підприємствах використовують колони з барботажными тарілками і насадочные.
Абсорбери з механічним перемішуванням використовують для насичення вуглекислим газом мінеральних вод і інших напоїв на установках невеликої продуктивності. В такому абсорбері (мал. 1) рідина подається в нижню частину апарату, звану ванною а що обертаються на горизонтальному валу перфоровані диски захоплюють рідину і піднімають її вгору. Рідина заповнює отверствия в дисках і утворює плівки на їх поверхні. Під дією відцентрової сили з дисків зриваються крапельки і заповнюють простір апарату над рівнем рідини. Газ подається у верхню частину апарату і вступає в контакт з крапельками і плівками рідини. Для підтримки високої швидкості поглинання газу апарати забезпечують сорочками, куди подають охолоджуючу воду.
.
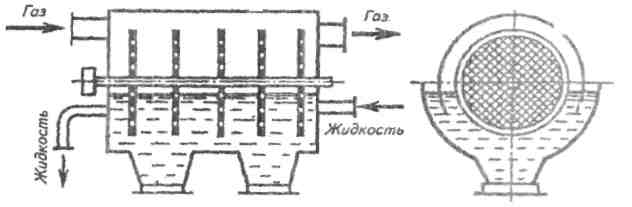
Рис. 1. Абсорбер с механическим перемешиванием
Плівковий трубчастий абсорбер (мал. 2) нагадує кожухотрубный теплообмінний апарат. Охолоджуюча вода подається в міжтрубний простір. Поглинаюча рідина поступає на верхні трубні грати і у вигляді плівки стікає по внутрішній поверхні труб. Газ підводиться під нижніми трубними гратами і по трубах проходить вгору..
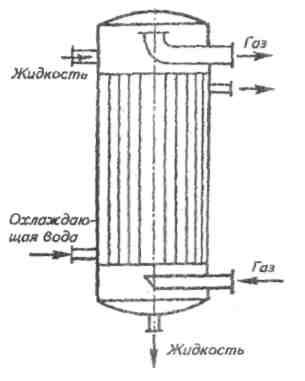
Рис. 2. Пленочный трубчатый абсорбер
Розпилюючий абсорбер був влаштований аналогічно распылительному конденсатору (мал. 3). Газ подається знизу, а поглинаюча рідина розпиляла по зонах за допомогою спеціальних сопл. Обчищений газ відводиться зверху, а рідина - знизу
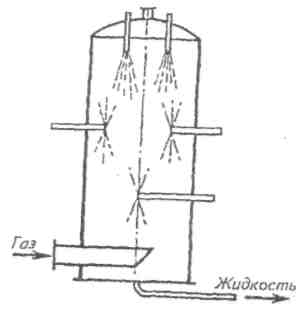
Рис. 3. Распылительный абсорбер
. Колони абсорбції з псевдозрідженим шаром - сучасні високоефективні апарати (мал. 4). Колона була розділена по висоті ситчатыми тарілками (мал. 4). Нижня тарілка - опорна для шару кулястої насадки з оргстекла або іншого полімерного матеріалу. Густина насадки не повинна перевищувати густини поглинаючої рідини, тому часто кулі діаметром від 7 до 75 мм роблять порожнистими. При певній швидкості газу, що подається під нижню тарілку, шар насадки переходить в стан псевдокипіння, забезпечуючи досконале перемішування фаз. Поглинаючу рідину розпиляли над верхньою тарілкою з шаром псевдокиплячої насадки. Обчищений газ відводиться з колони зверху, а рідина - знизу. Колони з псевдозрідженим шаром насадки мають більш високі КПД, або барботажные колони з колпачковыми тарілками.
.
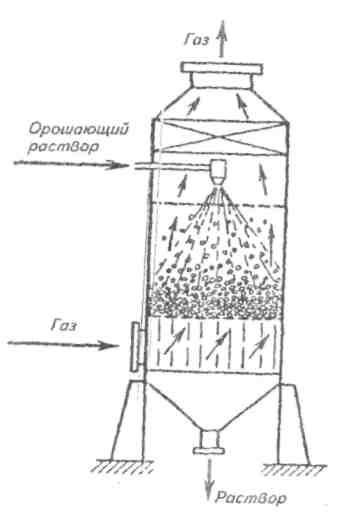
Рис. 4. Абсорбционная колонна с псевдоожиженным слоем
Д/з [1] с. 164-170, [2] с. 160-170
Екстрагування
План
4. Екстрагування із твердого тіла
5. Апарати та установки для екстрагування з твердих тіл
6. Рідинна екстракція
7. Апарати рідинної екстракції
1. Екстрагування із твердого тіла
Екстрагуванням називають процес добування із твердих тіл або рідких сумішей одного чи кількох компонентів за допомогою розчинника з вибірковою розчинністю. Процес відбувається в апаратах, які називають екстракторами.
В екстрактори подають сировину, з якої добувають цільовий компонент, і розчинник (екстрагент). З екстракторів періодично чи безперервно відводять екстраговану речовину (екстракт).
Технологічні процеси виготовлення багатьох видів харчової продукції пов'язані з переробкою сировини рослинного походження. Вона має капілярно-пористу структуру, сформовану клітинами різної будови, у вакуолях яких міститься цільовий компонент. У розчиненому вигляді він є в цукрових буряках, плодах і ягодах, у твердому вигляді – у висушених плодах, ягодах, травах, листі тощо.
У різних галузях харчової промисловості екстрагентом є вода, спирт, бензин, бензол, дихлоретан тощо. Щоб одержати чисті цільові компоненти, екстракти, добуті за допомогою різних екстрагентів, піддають додатковому очищенню від нехарчових домішок, інколи їх згущують.
Частинки рослинної сировини, з яких екстрагують цільовий компонент, умовно зараховують до твердих тіл. Залежно від стану сировини (суха, волога) процес екстрагування поділяють на різну кількість послідовних стадій. У спрощеному вигляді для екстрагування висушеної сировини існують такі стадії: а) проникнення розчинника в пори частинок сировини; б) розчинення цільового компонента; в) молекулярне перенесення розчиненої речовини до поверхні поділу фаз; г) перенесення екстрагованої речовини з поверхні частинок сировини в масу екстрагенту. При екстрагуванні цільових компонентів із сировини, в якій вони містяться в розчиненому стані, перших двох стадій немає.
Залежно від фазових станів сировини та екстрагенту процес поділяють на екстрагування в системах: а) тверде тіло – рідина; б) рідина – рідина.
Екстрагування в системі тверде тіло – рідина є одним з основних технологічних процесів при добуванні цукрози з буряків, олії з насіння соняшнику, бавовнику, сої, ефірної олії, при одержанні ферментів з культур плісеневих грибів, у виробництві вин, пива, лікеро-горілчаних виробів, крохмалю, розчинної кави, чаю та різних плодових екстрактів.
Рідинну екстракцію застосовують у виробництвах спирту, вина, олії, антибіотиків та інших харчових продуктів.
2. Апарати та установки для екстрагування із твердих тіл
Екстракційні апарати класифікують залежно від таких ознак:
- режим роботи – апарати періодичної і безперервної дії;
- вид процесу – протитечійні, прямотечійні, з комбінованим процесом;
- вид циркуляції – з одноразовим проходженням фаз і рециркуляцією екстрагенту;
- складність конструкції – екстракційні установки, до складу яких входять кілька машин і апаратів, і власне апарати, в яких усі стадії процесу екстрагування проходять в одній місткості, обладнаній всіма необхідними пристроями;
- конструкція основних складових частин – ротаційні, колонні (одно- і багатоколонні) установки, апарати похилого типу (одно- та двошнекові);
- конструкція пристроїв для пересування твердої фази – лопатеві, шнекові, ковшові, ланцюгові, стрічкові;
- тиск в екстракторах – атмосферні, вакуумні та ті, що працюють під тиском;
- гідродинамічний характер процесу – з нерухомим шаром твердих частинок, з рухомим об'ємом сокостружкової суміші, з киплячим шаром твердої фази та зрошувальні.
Розглянемо схематичну будову та принцип дії найпоширеніших у різних виробництвах екстракторів.
 2015-10-22
2015-10-22 1861
1861








