Кисень — безбарвний газ без запаху і смаку. При низьких температурі скраплюється в рідину солубого кольору. Молекула кисню складається з двох атомів. Хімічний зв'язок ковалентний. Спрощена структурна формула: O = O. Маючи у зовнішній електронній оболонці шість електронів, атоми Оксигену енергійно приєднують від атомів інших елементів два електрони, яких їм бракує для завершення валентної оболонки, і перетворюються в негативні двовалентні йони: O + 2e = O2-
При цьому Оксиген проявляє свої окиснювальні властивості. Серед усіх хімічних елементів він є одним з найсильніших окисників і поступається тільки фтору. 
Кисень добре розчинний в органічних розчинниках, поглинається тонкими порошками металів, вугілля. Утворює сполуки з усіма елементами. Він легко окиснює органічні сполуки. 
У лабораторіях кисень звичайно одержують термічним розкладанням деяких пероксидів, солей деяких оксигеновмісних кислот 2KClO3 =400= 2KCl + 3O2 ↑ Дуже чистий кисень добувають електролізом водного розчину гідроксиду натрію NaOH з застосуванням нікелевих електродів. Окислює всі Ме крім благор. 4Ag+3O2=Al2O3? Не Ме. 4P+502=2P2O5. Зі оксидами 2CO+O2=2CO2↑. Між молекулами Н2О2 виникають міцні водневі зв’язки, Гідроген пероксид може виступати як у ролі окисника, так і в ролі відновника, тому що атоми Оксигену в цій сполуці перебувають у проміжному ступені окиснення -1
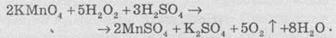 А з більш слабкими окисниками він виступає в ролі окисника:
А з більш слабкими окисниками він виступає в ролі окисника:  .
.
 2018-01-21
2018-01-21 610
610








