| 16 |
В ряду химических элементов Li 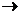 Na
Na 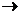 K происходит увеличение (усиление)
K происходит увеличение (усиление)
| 1) | числа электронов на внешнем энергетическом уровне |
| 2) | числа электронных слоёв в атомах |
| 3) | металлических свойств |
| 4) | степени окисления в высших оксидах |
| 5) | кислотного характера свойств высших оксидов |
| Ответ: |
| B2 |
Для этана верны следующие утверждения:
| 1) | относительная молекулярная масса равна 26 |
| 2) | является газообразным веществом (при н.у.) |
| 3) | атомы углерода в молекуле соединены двойной связью |
| 4) | вступает в реакцию с хлором |
| 5) | сгорает с образованием угарного газа и водорода |
| Ответ: |
При выполнении заданий 18, 19 к каждому элементу первого столбца подберите соответствующий элемент из второго столбца. Запишите в таблицу выбранные цифры под соответствующими буквами. Цифры в ответе могут повторяться.
| 18 |
Установите соответствие между парой веществ и реактивом, с помощью которого можно различить эти вещества.
|
|
|
| ВЕЩЕСТВА | реактив |
| А) Na2SO4 и NaI | 1) фенолфталеин |
| Б) BaCl2 и NaCl | 2) AgNO3 |
| В) Zn(NO3)2 и NaNO3 | 3) NaOH |
| 4) Al2(SO4)3 |
| Ответ: | А | Б | В |
| 19 |
Установите соответствие между названием вещества и реагентами,
с которыми это вещество может взаимодействовать.
| НАЗВАНИЕ ВЕЩЕСТВА | РЕАГЕНТЫ | |||||||||||||||
|
|
| Ответ: | А | Б | В |
Часть 2
Для ответов на задания 20–22 используйте отдельный лист. Запишите сначала номер задания (20, 21 или 22), а затем развёрнутый ответ к нему. Ответы записывайте чётко и разборчиво.
| 20 |
Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой
SO2 + Br2 + H2O → HBr + H2SO4.
Определите окислитель и восстановитель.
| 21 |
При пропускании 5,6 л аммиака (н.у.) через раствор серной кислоты с массовой долей 7% образовался сульфат аммония. Вычислите массу исходного раствора серной кислоты.
| 22 |
Даны вещества: Zn, Zn3(PO4)2, CuCl2, Ba(NO3)2, AgNO3, NaOH.
Используя воду и необходимые вещества только из этого списка, получите в две стадии нитрат цинка. Опишите признаки проводимых реакций. Для реакции ионного обмена напишите сокращённое ионное уравнение реакции.
ВАРИАНТ 4
Часть 1
 2018-03-09
2018-03-09 143
143








