1 Понятие и виды коррозионных разрушений при напряжении.
2 Влияние внутренних напряжений на коррозию
3 Атмосферная коррозия в агрессивных средах.
4. Действие каких факторов вызывает коррозионное растрескивание
5 Характеристика коррозионного растрескивания при напряжении (КПРН)
6 Причины КРПН
7 КРПН под воздействием хлорида
8 Коррозийное растрескивание под напряжением вызываемое H2S
9 Способы сокращения КРПН
Лабораторная работа №4 Изучение влияния различных факторов на скорость коррозии
Цель работы: построит зависимости влияния различных факторов на скорость коррозии, объяснить характер хода кривых и сделать практические выводы
Теоретическая часть
К внешним факторам электрохимической коррозии металлов относятся:
1. состав коррозионной среды;
2. условия коррозии:
- температура,
- давление,
- скорость давления среды и др.
Состав коррозионной среды определят водородный показатель рН, который влияет на скорость электрохимической коррозии, изменяя потенциал катодных деполяризационных реакций.
Коррозия большинства металлов в нейтральных растворах (воде и водных растворах солей) протекает с кислородной деполяризацией и её скорость сильно зависит от скорости протекания катодных реакций ионизации кислорода и подвода кислорода к корродирующей поверхности металла.
Скорость электрохимической коррозии металлов в растворах солей так же, как и в кислых растворах, зависит от природы растворённой соли и ёё концентрации, причём это зависимость может быть различной.
Водные растворы гидролизующихся солей влияют на скорость коррозионного процесса в зависимости от того, уменьшают они рН раствора или увеличивают.
Соли, образующие с ионом корродирующего металла комплекса, сильно смещают потенциал анодного процесса в отрицательную сторону и обеспечивают протекание анодного процесса, уменьшая концентрационную поляризацию, что приводит к увеличению скорости коррозии до некоторого предела.
С ростом концентрации солей увеличивается концентрация ионов хлоре, сульфата и амония, активирующих и облегчающих анодный процесс, и уменьшается растворимость деполяризаторе – кислорода, что затрудняет протеканию катодного процесса.
В каком – то интервале концентраций сильнее сказывается первый эффект, а затем преобладает второй (рисунок 5)
Влияние скорости движения электролита на электрохимическую коррозию металлов имеет сложный характер.
Особенно большое влияния этот фактор оказывает на коррозию металлов в нейтральных электролитах, протекающую с кислородной деполяризацией.
Он облегчает диффузию кислорода и зачастую изменяет характер процесса и его контролирующую стадию.
Так, при коррозии железа и стали в водопроводной воде начальное увеличение скорости движения воды, облегчающее диффузию кислорода к поверхности корродирующего металла вследствие уменьшения толщины диффузионного слоя электролита, приводит к заметному возрастанию скорости коррозии. Дальнейшее увеличение скорости движения воды приводит к снижению скорости коррозии, вызываемому наступлением пассивности (образованием защитной плёнки) при достаточно обильном поступлении кислорода

Концентрация соли, m,
Рисунок 5- Влияние концентрации соли КCl (С) на скорость коррозии низкоуглеродистый стали (убыль массы, г/м2)..
При очень больших скоростях движение воды вновь наблюдается увеличение скорости коррозии металла, обусловленное явление механического (эрозионного и кавитационного) разрушение защитной плёнки и самого металла (рис. 6)
При высокой шероховатости образца прочность закрепления окисной плёнки небольшая и при увеличении скорости потока происходит смыв плёнки, увеличивается доступ кислорода, и скорость коррозии несколько увеличивается.
Для,,чистых’’ образцов такое увеличении скорости не наблюдается.
В электролитах, затрудняющих или исключающих наступление пассивности (морская вода), снижение скорости коррозии металла с увеличением скорости движения электролита не наблюдается (рис. 7)
На коррозию металлов в кислых средах, которая протекает в водородной деполяризацией, скорость движения электролита оказывает меньшее влияние, чем в нейтральных средах.
Выполнение работы
Суть работы в том, что бы на основании литературных опытных данных построит зависимости влияния различных факторов на скорость коррозии, затем объяснить характер хода кривых и сделать практические выводы.
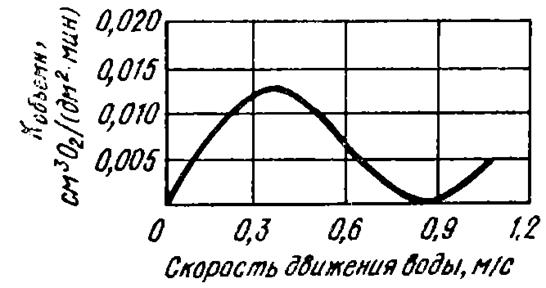
Рисунок 5- Влияние скорости движения насыщенной кислородом водопроводной воды на скорость коррозии.
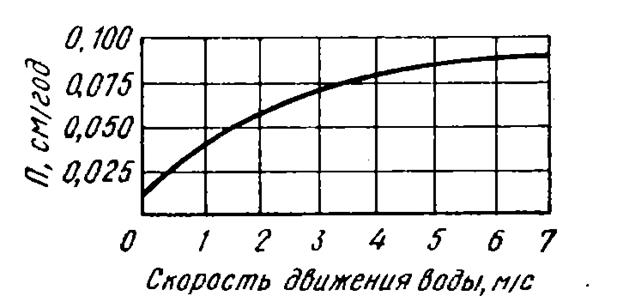
Рисунок 7 - Влияние скорости раствора электролита (морской воды) на скорость коррозии
Выполнение работы.
1. Установление влияния состава коррозионной среды (Na Cl) на скорость электрохимической коррозии.
Т а б л и ц а 7 Данные к работе:
| % Na Cl | Vкор. гр/м2 •г |
| 0 3 5 10 15 20 25 | 1.5 2.2 1.8 1.6 1.1 0.7 0.25 |
1.1. Объясните, почему с повышением концентрации раствора скорость коррозии вначале растёт, а затем падает. Связать этот процесс с явление кислородной деполяризацией анодного процесса.
1.2 Постройте график зависимости скорости коррозии от концентрации раствора Na Cl.
1.3.Сделайте практические выводы и рекомендации.
2. Установление влияния скорости потока водопроводной воды на скорость коррозии.
Т а б л и ц а 8 Данные к работе
| Скорость потока, м/с | Скорость коррозии мм/год | ||
| образец I | образец II | образец I | образец II |
| 0 0.2 0.4 0.81 1.5 2.2 | 0 0.1 0.3 0.6 1.2 2.1 | 0.35 0.75 1.0 0.60 0.63 0.65 | 0.51 0.7 0.5 0.45 0.35 0.24 |
Примечания. Образец I – высокая шероховатость, образец II – низкая шероховатость.
2.1. Постройте график зависимости скорости коррозии от скорости потока водопроводной воды.
2.2 Объясните характер изменений скорости коррозии от скорости потока вода для образцов I и II.
2.3 Сделайте практические выводы и рекомендации.
3. Установление влияния скорости потока воды на скорость коррозии.
Т а б л и ц а 9 Данные к работе
| Скорость потока, м/с | Скорость коррозии мм/год |
| 0 0.25 1.0 2.0 3.0 4.0 5.0 6.0 7.0 7.5 8.0 | 0.14 0.25 0.40 0.65 0.75 0.80 0.85 0.88 0.89 0.9 0.95 |
3.1. Постройте график зависимости скорости коррозии от скорости потока морской воды.
3.2. Объясните характер изменения скорости коррозии от скорости потока морской воды.
3.3 Сделайте практические выводы и рекомендации.
 2020-06-12
2020-06-12 170
170








