10. Две свободные  имеет атом:
имеет атом:
1) 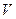 2)
2)  3)
3) 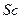 4)
4) 
11. Электронная формула иона  соответствует атому:
соответствует атому:
1)  2)
2)  3)
3)  4)
4) 
12. Атому  в возбужденном состоянии соответствует формула
в возбужденном состоянии соответствует формула
1)  3)
3) 
2)  4)
4) 
13. Низшая степень окисления для элемента с электронной формулой  равна:
равна:
1)  2)
2)  3)
3)  4)
4) 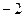
14. Вещества с ковалентной неполярной связью это:
1) водород 3) фтороводород
2) алюминий 4) вода
15.  − гибридизация в следующей частице:
− гибридизация в следующей частице:
1) 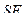 2)
2)  3)
3) 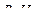 4)
4) 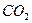
16. Более устойчивый оксид:
1) ½ О2 + Mg → MgО, ∆H= – 600 КДж/Моль
2) ½ О2 + Zn → ZnО, ∆H= – 357 КДж/Моль
3) ½ О2 + Cu → CuО, ∆H= – 155 КДж/Моль
4) ½ О2 + Hg → HgO, ∆H= – 88,2 КДж/Моль
17. Кислотные свойства преобладают в большей степени у оксида (подтвердите расчётами):
1) Al2O3 + CaO → Ca(AlO2)2
∆G0 КДж/Моль – 1582 – 604,2 – 2210
2) В2O3 + CaO → Ca(ВO2)2
∆G0 КДж/Моль – 1184 – 604,2 – 1924
18. Если температурный коэффициент скорости химической реакции равен 3, то при повышении температуры от 20оС до 60оС скорость реакции _________
1) увеличивается в 81 раз 3) увеличивается в 27 раз
2) уменьшается в 12 раз 4) уменьшается в 9 раз
19. Для смещения равновесия в системе СаСО3 (к) ↔ СаО(к) + СО2 (г) ∆Н > 0
в сторону продуктов реакции необходимо ______________________________
1) понизить температуру 3) ввести катализатор
2) повысить концентрацию СО2 4) повысить температуру
20. При повышении давления в 3 раза скорость реакции 2NO(г)+Cl2(г)→2NOCl(г) увеличивается
1) в 81 раз 3) в 9 раз
2) в 27 раз 4) в 3 разa
ВАРИАНТ № 3
Часть А. Дайте полное решение заданий
Укажите номер правильного ответа:
1. Электронная формула 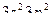 соответствует атому:
соответствует атому:
1)  2)
2) 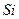 3)
3) 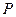 4)
4) 
2. Пространственная конфигурация молекулы – линейная соответствует частицам (два варианта ответа):
1)  2)
2) 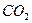 3)
3)  4)
4) 
3. Тепловой эффект реакции:
. 2РbS + 3О2 → 2РbО + 2SО2
∆Н0обр КДж/Моль –94,28 0 −217,86 −296,9
1) ∆Нх.р.= − 840,96 КДж 3) ∆Нх.р.= + 420,00 КДж
2) ∆Нх.р.= + 840,96 КДж 4) ∆Нх.р.= − 420,00 КДж
4. Если энтальпия образования SO2 равна (− 297 КДж/моль), то количество теплоты, выделяемое при сгорании 16 г серы, равно ________________КДж
1) 74,25 2) 148,5 3) 297 4) 594
5. При проведении обратимой реакции 2СО (г) + О2 (г) ↔ 2СО2 (г)
начальные концентрации СО и О2 были соответственно равны 0,8 и 0,5 моль/л, а в состоянии равновесия концентрация СО2 составила 0,2 моль/л, тогда константа равновесия равна _____________________________________
1) 0,27 2) 4,56 3) 5,01 4) 6,03
 2020-10-10
2020-10-10 142
142








