КОРРОЗИЯ МЕТАЛЛОВ
| Биохимическая коррозия | Химическая коррозия | Электрохимическая коррозия |
► На поверхности Ме и сплавов образуется множество микрогальванопар. Участок с меньшим значением потенциала служит анодом, а участок с большим значением потенциала служит катодом.
► При возникновении микрогальванопары силавозникающего электрического тока тем больше, чем дальше друг от друга стоят контактирующие металлы в ряду напряжения.
► При этом поток (е-) от более активного металла идет к металлу менее активному. Окислительно-восстановительный процесс в отличии от химической коррозии протекает на различных участках поверхности. Анодный участок поверхности (окисляется), а на катоде восстанавливается окислитель из окружающей среды.
► Электрохимическая коррозия имеет большую скорость, чем химическая коррозия.
► ПРИЧИНЫ ВОЗНИКНОВЕНИЯ КОРРОЗИИ:
► 1. энергетическая неоднородность поверхности Ме;
► 2. неоднородность химического и фазового состава;
► 3. наличие примесей в Ме;
► 4. характер поверхности (шероховатость, излом);
► 5. наличие дефектов кристаллической решетки Ме;
► 6. неодинаковая концентрация окислителя на различных участках поверхности Ме.
Скорость коррозии определяется:
► 1. по глубинному показателю (в потере толщины Ме в год);
► 2. по массовому показателю (потеря массы Ме в ед. времени).
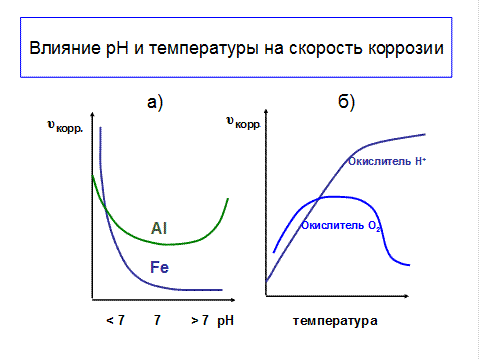
ФАКТОРЫ ВЛИЯЮЩИЕ НА СКОРОСТЬ:
► 1. внутренние (природа Ме, наличие примесей, дефектов кристаллической решетки Ме);
► 2. внешние (рН раствора, окружающая среда, температура).
Пример. Уравнение процесса, протекающего на катоде при электрохимической коррозии железных изделий в нейтральной среде, имеет вид …
1)O2 + 4H+ + 4e → 2H2O
2) 2H+ + 2e → H2
3)Fe2+ + 2e- → Fe0
4)O2 + 2H2O + 4e → 4OH-
Пример. Уравнение процесса, протекающего на аноде при электрохимической коррозии железных изделий в нейтральной среде, имеет вид …
1) Fe2+ + 2e- → Fe0 2) 2H+ + 2e → H2
3) Fe0 − 2e- → Fe2+ 4) O2 + 2H2O + 4e → 4OH‾

 2014-02-03
2014-02-03 1822
1822
