В указанных выше субстратах есть еще СН-кислотный центр у β-углеродного атома. Если у нуклеофила основные свойства значительны, он может вытолкать уходящую группу и оторвать подвижный протон c α-положения..


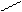
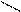 Н Н
Н Н



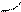
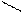
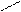 Н – С – С – Х С = С + ВН+ + Х-
Н – С – С – Х С = С + ВН+ + Х-

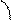 Н Н
Н Н
В:
Одной из реакций элиминирования, имеющих биологическое значение, является дегидратация.

 СН3 – СН – СН3 СН3 – СН = СН2 + Н2О
СН3 – СН – СН3 СН3 – СН = СН2 + Н2О
ОН
Водород отщепляется (правило Зайцева) наименее гидрогенизированного углерода. Механизм реакции:
Быстро tкип


 СН3 – СН – СН3 + Н2SО4 СН3 – СН – СН3 + НSО4-
СН3 – СН – СН3 + Н2SО4 СН3 – СН – СН3 + НSО4-
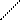
 :ОН О+
:ОН О+
Н Н
медленно

 СН3 – СН – СН3 СН3 - +СН – СН3 + Н2О
СН3 – СН – СН3 СН3 - +СН – СН3 + Н2О

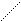 О+
О+
Н Н
 СН3 - +СН СН3 + Н2О СН3 – СН = СН2 + Н3+О
СН3 - +СН СН3 + Н2О СН3 – СН = СН2 + Н3+О
Дегидратация характерна для соединений живой природы содержащих ОН и СН кислотный центр. Примером может служить реакция превращения яблочной кислоты в фумаровую.

 СООН СООН Н
СООН СООН Н

 НО – С – Н tо фумараза С = С
НО – С – Н tо фумараза С = С
 Н – С – Н -Н2О Н СООН
Н – С – Н -Н2О Н СООН
СООН
Яблочная фумаровая кислота
Фумараза не катализирует Д-яблочную кислоту
Поли- и гетерофункциональные соединения
План лекции.
1. Поли- и гетерофункциональность, как фактор повышающий реакционную способность органических соединений.
2 Специфические свойства поли- и гетерофункциональных соединений:
а) амфотерность образование внутримолекулярных солей.
б) внутримолекулярная циклизация гамма, β, ξ – гетерофункциональных соединений.
в) межмолекулярная циклизация (лактиды и декетопипирозины)
г) хелатообразование.
д) реакции элиминирования бета – гетерофункциональных
соединений.
е) таутомерия кето–енольная. Фосфоенолпируват, как
макроэргическое соединение.
ж) декарбоксилирования.
з) стереоизомерия
Поли- и гетерофункциональность, как причина появления специфических свойств у гидрокси-, амино- и оксокислот.
Наличие в молекуле нескольких одинаковых или разных функциональных групп составляет характерную черту биологически важных органических соединений. В молекуле может быть две и более гидроксильных групп, аминогрупп, карбоксильных групп.


 НО – СН2 – СН2 – ОН – этиленгликоль, СН2 – СН – СН2
НО – СН2 – СН2 – ОН – этиленгликоль, СН2 – СН – СН2
ОН ОН ОН
 2014-02-13
2014-02-13 918
918








