Тема 2. Энтропия. Жидкости.
Лекция №12
1. Энтропия, второе начало термодинамики, пример расчёта.
3. Поверхностное натяжение в жидкостях, смачивание.
1.Энтропия, второе начало термодинамики, пример расчёта.
Мы убедились, что КПД необратимого кругового процесса всегда меньше, чем КПД при обратимом цикле. Этот результат можно сформулировать в следующем виде:
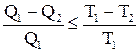 .
.
Знак равенства соответствует случаю обратимых процессов. Отсюда нетрудно получить соотношение, которое играет важную роль в термодинамике:
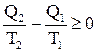 . (1)
. (1)
Определение 1.
Функция состояния системы, определяемая как отношение количества теплоты, сообщаемого системе, к абсолютной температуре последней называется энтропией, то есть 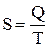 .
.
Энтропия, как видно из полученного соотношения, при обратимом процессе остается неизменной 
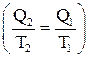 и возрастает
и возрастает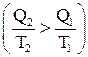 , если термодинамический процесс необратим.
, если термодинамический процесс необратим.
Энтропия — важная термодинамическая характеристика системы, позволяющее сформулировать второе начало термодинамики:
«При необратимых процессах энтропия замкнутой системы может только возрастать.»
Возрастание энтропии системы при необратимом процессе выражает тот факт, что тепло само по себе не может переходить от менее нагретых к более нагретым телам. Последнее утверждение можно рассматривать также как пример формулировки второго начала термодинамики.
Из изложенного следуют важные выводы.
 2014-02-18
2014-02-18 321
321







