1. Решетки Бравэ
Упорядоченное или строго регулярное пространственное расположение атомов вещества характеризуется тем, что существуют такие три вектора a, b, c, образующие между собой углы α, β, γ (рис. 1), что любое трансляционное смещение
 r = n a + m b + l c (1)
r = n a + m b + l c (1)
Рис. 1. Элементарный параллелепипед
где n, m, l – произвольные целые числа, приводит к полному совмещению с исходной кристаллической решёткой. Различают 7 различных систем взаимного расположения базисных векторов (сингоний) и 4 типа элементарных кристаллических ячеек (таблица 1). Сингонии определяются в соответствии с соотношением длин базисных векторов a, b, c и значениями углов α, β, γ. Наименее симметричной является триклиная сингония: 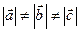 и
и 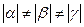 , а наиболее симметричная кубическая сингония: (
, а наиболее симметричная кубическая сингония: (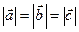 ,
, 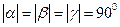 ). Далее по мере потери элементов симметрии следуют тетрагональная (
). Далее по мере потери элементов симметрии следуют тетрагональная (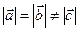 ,
, 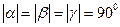 ) и орторомбическая (
) и орторомбическая (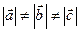
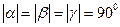 ) сингонии. Для гексагональной сингонии
) сингонии. Для гексагональной сингонии 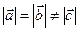 ,
, 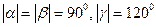 , тригональной
, тригональной 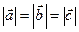 ,
, 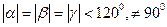 и для моноклинной
и для моноклинной 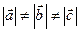 ,
, 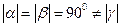 .
.
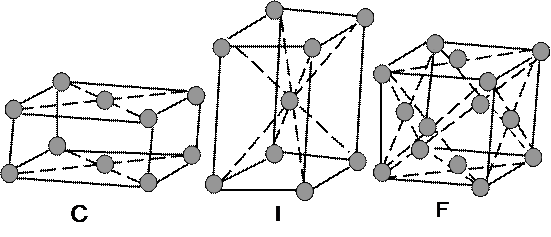
В каждой сингонии в зависимости от ее симметрии можно построить не более 4-х типов элементарных ячеек кристаллической решетки (рис. 2). У всех элементарных ячеек, построенных на базисных векторах a, b, c, в каждой из восьми вершин должен находиться атом. Кроме того каждый атом данной элементарной ячейки также входит в состав еще восьми смежных элементарных ячеек. Поэтому для самой простой (примитивной, обозначаемой далее Р) элементарной ячейки, в которой атомы располагаются только в ее вершинах, считается, что на одну элементарную ячейку приходится только один атом. Такую примитивную элементарную ячейку можно построить для всех типов сингоний.
В объемно-центрированной элементарной ячейке (обозначается буквой I) кроме вершинных атомов имеется еще один дополнительный атом в центре ячейки, который не входит в состав никакой другой смежной ячейки. Поэтому на каждую объемно-центрированную элементарную ячейку приходится 2 атома. Объемно-центрированную элементарную ячейку можно построить для кубической, тетрагональной и орторомбической сингоний.
В гранецентрированной элементарной ячейке (обозначается буквой F) дополнительные атомы располагаются в центре каждой из шести граней и при этом каждый такой атом принадлежит сразу двум элементарным ячейкам. Таким образом, на каждую гранецентрированную элементарную ячейку приходится 4 атома. Гранецентрированную элементарную ячейку можно построить для кубической и ромбической сингоний.
Наконец, можно построить базоцентрированную ячейку с двумя дополнительными атомами в верхней и нижней гранях (обозначается буквой С) для орторомбической сингонии и с двумя дополнительными атомами в двух боковых гранях (обозначается буквой В) для моноклинной сингонии. Базо-центрированные элементарные ячейки содержат два атома.
Итак, в целом мы получили 14 типов кристаллических решеток, которые называют решетки Бравэ.
Таблица
Кристаллические сингонии и их характеристики
| Сингония | Ребра | Углы | Типы решеток |
| Кубическая | a = b = с | α = β = γ = 900 | P, I, F |
| Тетрагональная | a = b ≠ c | α = β = γ = 900 | P, I |
| Ромбическая | a ≠ b ≠ c | α = β = γ ≠ 900 | P, I, F, C |
| Гексагональная | a = b ≠ c | α = β = 900, γ = 1200 | P |
| Тригональная | a = b = c | α = β = γ < 1200, ≠ 900 | P |
| Моноклинная | a ≠ b ≠ c | α = β = 900 ≠ γ | P, B |
| Триклинная | a ≠ b ≠ c | α ≠ β ≠ γ | P |
 | |||
 |
Рис. 2. Типы кристаллических решеток: а) примитивная (P), б) базоцентрированная (С), в) объемно-центрированная (I), г) гранецентрированная (F).
Для двухмерного случая, т.е. регулярного расположения атомов на плоскости существует 5 различных решёток Бравэ, каждая из которых имеет свою элементарную ячейку (рис. 3).
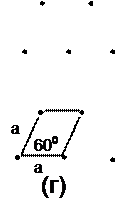 | |||||||||
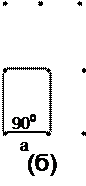 | 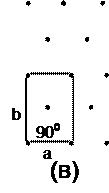 | ||||||||
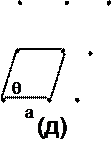 | |||||||||
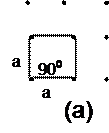 | |||||||||
Рис. 3. Пять решеток Бравэ для двумерного случая с выделенной элементарной ячейкой: квадратная (а), простая прямоугольная (б), центрированная прямоугольная (в), гексагональная (г), косоугольная (д).
Ячейка Вигнера-Зейтца
Существует еще один способ построения примитивной элементарной ячейки кристаллической решетки, которая содержит один единственный атом и представляет собой многогранник. Такие элементарные ячейки все вместе полностью заполняют все пространство. Такая элементарная ячейка называется ячейкой Вигнера-Зейтца и строится она следующим образом. Берется произвольный атом, от него проводятся линии ко всем ближайшим атомам и через середину этих линий проводятся перпендикулярные им плоскости. Пересечение этих плоскостей образует многогранник, который и называется элементарной ячейкой Вигнера-Зейтца данной кристаллической решетки. На рис. 4 показаны ячейки Вигнера-Зейтца для объемно-центрированной и гранецентрированной кубической решетки. Они представляют собой тетракондекаэдр (усеченный правильный октаэдр) и ромбический додекандер соответственно.

Рис. 4. Ячейки Вигнера-Зейтца ОЦК (а) и ГЦК (б) кристаллических решеток.
2. Обратная решетка
При рассмотрении электронных свойств и колебательных возбуждений кристалла, а также при рассмотрении отражения рентгеновского излучения большую роль играет понятие обратной решетки, которая строится в пространстве, сопряженном координатному. Размерностью обратного пространства является единица обратная длине. В таком обратном пространстве каждой решетке Бравэ с базисными векторами (1) ставится в соответствие обратная решетка с базисными векторами, определяемыми векторными произведениями
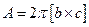 ,
, 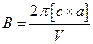 ,
, 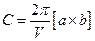
где 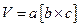 - объем элементарного параллелепипеда, образованного базисными векторами (1).
- объем элементарного параллелепипеда, образованного базисными векторами (1).
Легко убедиться, что для базисных векторов прямой и обратной решеток выполняются соотношения
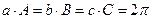
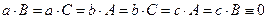
Таким образом, производный вектор обратной решетки
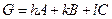
перпендикулярен плоскости прямой решетки, определяемой индексами 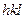 и соответственно длина этого вектора равна обратной величине расстояния между двумя ближайшими такими плоскостями. Следовательно, каждой плоскости прямой решетки с индексами
и соответственно длина этого вектора равна обратной величине расстояния между двумя ближайшими такими плоскостями. Следовательно, каждой плоскости прямой решетки с индексами 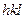 отвечает узел обратной решетки с координатами
отвечает узел обратной решетки с координатами 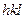 . Поэтому если рассматривать отражение рентгеновских лучей от семейства параллельных плоскостей кристаллической решетки, то направления распространения лучей определяют формулой Вульфа-Брэгга.
. Поэтому если рассматривать отражение рентгеновских лучей от семейства параллельных плоскостей кристаллической решетки, то направления распространения лучей определяют формулой Вульфа-Брэгга.
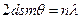
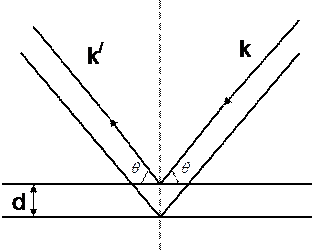 | где 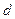 - расстояние между параллельными плоскостями данного семейства, - расстояние между параллельными плоскостями данного семейства, 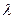 - длина волны рентгеновских лучей, - длина волны рентгеновских лучей, 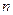 - произвольное целое число. - произвольное целое число. |
Таким образом, каждый узел обратной решетки соответствует определенному разрешенному направлению отражения рентгеновских лучей от плоскостей прямой решетки.
Принцип плотной упаковки
Теперь поговорим о том, каким образом формируется та или иная регулярная кристаллическая решетка твердого тела. Наверно устойчивость кристаллической структуры будет определяться минимумом потенциальной энергии взаимодействия атомов и молекул. Рассмотрим простейшую модель, в которой атомы представляются в виде твердых шаров. Такая модель достаточно хорошо описывает кристаллическую решетку металлов, где положительно заряженные ионы «стягиваются» в плотноупакованную структуру за счет взаимодействия с отрицательно заряженным электронным газом. Сами же ионы отталкиваются друг от друга за счет кулоновского взаимодействия. Так как и притяжение, и отталкивание атомов в этом случае является изотропным, то модель твердых шаров является вполне адекватной. Минимум потенциальной энергии будет достигаться, если шары будут заполнять большую часть свободного пространства, и каждый шарик должен при этом взаимодействовать как можно с большим числом других шаров.
Наиболее плотная упаковка одинаковых шаров на плоскости достигается при их расположении по узлам двумерной гексагональной решётки. Второй гексагональный слой наиболее эффективно располагается над первым, если произвести смещение исходной решётки
Третий слой можно расположить двумя различными способами. Первый способ – совместить решётку третьего слоя с решёткой первого. Тогда получается гексагональная решётка с гексагональной плотноупакованной структурой (ГПУ). Второй способ опять сместив решётку третьего слоя относительно решётки второго.В этом случае получается гранецентрированная кубическая решётка.
Для ГПУ кристаллической решётки твёрдых шаров имеются пустоты, в которые можно поместить шарики меньшего размера, причём имеются два типа вакансий.
Центр вакансий одного типа является равноудалённым от шести шаров и называется октаэдрическим положением. Радиус шарика, который можно поместить в эту вакансию равен
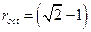
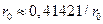
Другой тип вакансии называется тетраэдрическим положением и его центр равноудалён от четырёх близлежащих шаров, а радиус шарика, который можно поместить в эту вакансию, равен
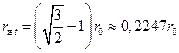
Нетрудно понять, что число октаэдрических позиций в решётке равно числу шаров, а число тетраэдрических – вдвое больше. Это означает, что можно рассматривать структурную организацию алмаза в виде твердых шаров, диаметр которых равен длине одинарной С-С связи, т.е. порядка 1,4 Å, центры которых располагаются в узлах гранецентрированной кубической решетки (длина ребра куба равна примерно 3,6 Å) и в центрах четырёх (расположенных в шахматном порядке) октантов куба. Таким образом, четыре атома, пронумерованные на рис. 1 цифрами являются ближайшими к атому (на рисунке не показан), расположенному в центре правого верхнего октанта. На следующем рис. 4 этот октант показан отдельно. На рисунке также показан координа тетраэдр алмазоподобной структуры.
1. Наночастицы с ГЦК
Металлы и благородные газы как правило кристаллизуются в плотноупакованные решётки. Это, например, металлы Ag, Au, Al, Co, Cu, Pb, Pt, Ph и благородные газы Nl, Ar, Kr, Xl.
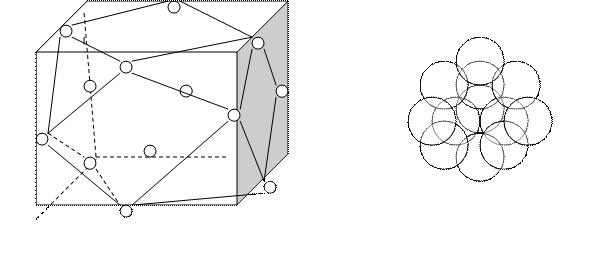
14-гранник, называемый кубооктаэдром.
Это есть наименьшая из возможных наночастиц. Если нарастить на неё ещё один слой из 42 шариков, то получится следующая стабильная Нч, состоящая из 55 атомов.
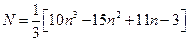
| Nобл. | Диаметр | N | Nповер. | % |
| … … … | 1d 3d 19d 99d 199d | 1(1) 13 (13) 55(57) 147(153) 309(321) 4 105 3,28 106 | 2,4 104 9,8 104 | 92,3 28,3 5,9 |
Полученный ряд чисел называется структурными магическими числами. Однако в ряде случаев существенную роль в минимизации энергии НЧ играют валентные электроны. Тогда устойчивые кластеры имеют другой ряд магических чисел (т.н. электронные магические числа). Например, для Na этот ряд имеет вид 3, 9, 20, 36, 61, ….., 1220 (n=15).
2. Полупроводниковые структуры
1) Некоторые оксиды и сульфиды, например Zn+~0,074, Cd+~0,097, (S-~0,184, O-2~0,132), MgO, MgS, MnO, MnS
Большие анионы располагаются в ГЦК решётке, а маленькие катионы занимают октаэдрические позиции, такие решётки называются типа NaCl.
2) Полупроводники типа ZnS (сфалерит) цинковая обманка
Электронная структура кристаллических твёрдых веществ.
 2014-02-09
2014-02-09 2232
2232
