Кинетика ферментативных процессов (продолжение)
Молекула каждого фермента содержит несколько кислотных и оснόвных групп. В нейтральной области рН бόльшая часть этих групп либо полностью депротонирована (аспартат и глутамат), либо полностью протонирована (аргинин и лизин). В молекуле фермента всегда имеется несколько групп со значениями рКа в интервале от 5 до 9 (рКа – показатель кислотной константы диссоциации). Молекула фермента непременно содержит несколько групп, состояние ионизации которых меняется при изменении рН среды. Этим объясняется то, что ферменты активны в водном растворе с определенной значением рН. За немногими исключениями (пепсин и щелочная фосфатаза), наиболее изученные ферменты активны в водном растворе при значениях рН в интервале от 5 до 9.
Для описания поведения многих ферментов при изменении рН может быть использована модель, в которой принимаются во внимание только две ионизируемые группы. Ее впервые использовал Михаэлис. В соответствии с ней фермент рассматривается как двухосновная кислота (HEH) с двумя разными кислыми группами (1.46):
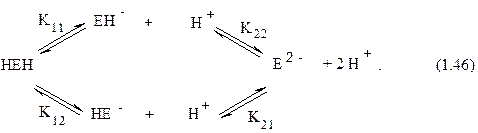
Для каждой стадии ионизации на схеме указана соответствующая константа диссоциации. В равновесных условиях концентрации всех форм фермента будут связаны с [H+] соотношениями:
[EH−] = [HEH] ∙ K11 / [H+];
[HE−] = [HEH] ∙ K12 / [H+];
[E2−] = [HEH] ∙ K11 ∙ K22 / [H+]2 = [HEH] ∙ K12 ∙ K21 / [H+]2. (1.47)
Константы К11 и К21 характеризуют отщепление протона от одной и той же группы, К11 должна быть больше К21, поскольку форма HE− имеет на один отрицательный заряд больше, чем форма НЕН и является менее сильной кислотой. Точно так же К12 > К22. Выражение для концентрации формы E2− должно иметь один и тот же вид независимо от того, приходим мы к нему от НЕН через EH− или через HE−. Поэтому два выражения для [E2−] в уравнении (1.47) должны быть эквивалентны друг другу, и, следовательно, K11 ∙ K22 = K12 ∙ K21.
Учитывая, что полная концентрация фермента [Е]О равна сумме концентраций всех его форм ([HEH] + [EH−] + [HE−] + [E2−]), получаем:
[Е]О
[HEH] = —————————————————, (1.48)
1 + (K11 + K12) / [H+] + (K11 ∙ K22) / [H+]2
[Е]О ∙ К11 / [H+]
[EH−] = —————————————————, (1.49)
1 + (K11 + K12) / [H+] + (K11 ∙ K22) / [H+]2
[Е]О ∙ К12 / [H+]
[HE−] = —————————————————, (1.50)
1 + (K11 + K12) / [H+] + (K11 ∙ K22) / [H+]2
[Е]О ∙ К11 ∙ K22 / [H+]2
[E2−] = —————————————————. (1.51)
1 + (K11 + K12) / [H+] + (K11 ∙ K22) / [H+]2
Типичные зависимости [HEH], [EH−], [HE−], [E2−] от рН при произвольных значениях констант диссоциации представлены на рисунке 1.11.
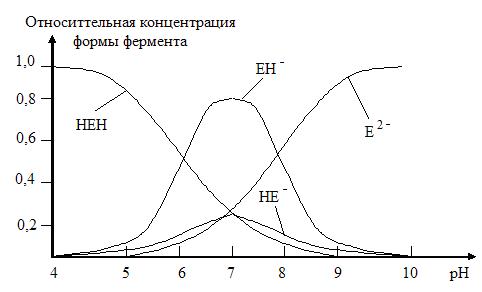
Рис. 1.11. Зависимость относительных концентраций форм фермента от рН для фермента НЕН, содержащего две ионизируемые группы.
В реальном эксперименте получить подобные кривые с высокой степенью точности невозможно, поскольку трудно определить одновременно все четыре константы диссоциации. Следовательно, невозможно определить, какой вклад в данное свойство фермента дает каждая из этих форм. Поэтому необходимо рассматривать EH− и HE− как единую форму, концентрация которой определяется выражением (1.52):
[Е]О
[EH−] + [HE−] = ——————————, (1.52)
1 + [H+] / К1 + К2 / [H+]
где: К1 = K11 + K12 = ([EH−] + [HE−]) ∙ [H+] / [HEH],
К2 = K11 ∙ K22 / (K11 + K12) = [E2−] ∙ [H+] / ([EH−] + [HE−]).
Константы K1 и K2 называют молекулярными константами диссоциации, чтобы отличить их от констант диссоциации, характеризующих ионизацию индивидуальных групп K11, K12, K21, K22. С практической точки зрения константы K1 и K2 имеют то преимущество, что их можно измерить, в то время как константы K11, K12, K21, K22 экспериментально определить не удается, поскольку невозможно оценить величину K12 / K11.
Выражение для [HEH] и [E2−] можно записать с использованием молекулярных констант диссоциации:
[Е]О
[HEH] = —————————————, (1.53)
[H+]2 / К1∙ K2 + [H+] / К2 + 1
[Е]О
[E2−] = —————————————. (1.54)
1 + К1 / [H+] + К1∙ K2 / [H+]2
Уравнение (1.52) описывает колоколообразную форму кривой зависимости активности фермента от рН (рисунок 1.12.).
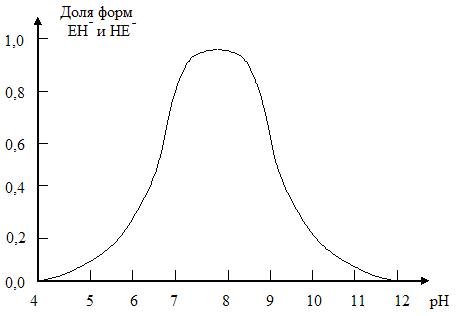
Рис. 1.12. Колоколообразная зависимость относительной концентрации однократно ионизированной формы фермента от рН.
 2014-02-12
2014-02-12 820
820








