Только с чисто формальных позиций можно рассматривать карбоксильную группу как комбинацию карбонильной и гидроксильной функций. Фактически их взаимное влияние друг на друга таково, что полностью изменяет их свойства.
Обычная для карбонила поляризация двойной связи С=0 сильно возрастает за счет дополнительного стягивания свободной электронной пары с соседнего атома кислорода гидроксильной группы:
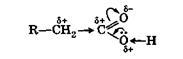
Следствием этого является значительное ослабление связи О—Н в гидроксиле и легкость отщепления атома водорода от него в виде протона (Н+). Появление пониженной электронной плотности (δ+) на центральном углеродном атоме карбоксила приводит также к стягиванию σ-электронов соседней связи С—С к карбоксильной группе и появлению (как у альдегидов и кетонов) пониженной электронной плотности (δ +) на α-углеродном атоме кислоты.
Все карбоновые кислоты обладают кислой реакцией (обнаруживается индикаторами) и образуют соли с гидроксидами, оксидами и карбонатами металлов и с активными металлами:
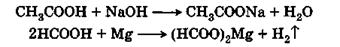 |
Карбоновые кислоты в большинстве случаев в водном растворе диссоциированы лишь в малой степени и являются слабыми кислотами, значительно уступая таким кислотам, как соляная, азотная и серная. Так, при растворении одного моля в 16 л воды степень диссоциации муравьиной кислоты равна 0,06, уксусной кислоты — 0,0167, в то время как соляная кислота при таком разбавлении диссоциирована почти полностью.
Для большинства одноосновных карбоновых кислот рКа = 4,8, только муравьиная кислота имеет меньшую величину рКа (около 3,7), что объясняется отсутствием электронодонорного эффекта алкильных групп.
В безводных минеральных кислотах карбоновые кислоты протонируются по кислороду с образованием карбкатионов:
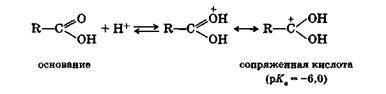
Сдвиг электронной плотности в молекуле недиссоциированной карбоновой кислоты, о котором говорилось выше, понижает электронную плотность на гидроксильном атоме кислорода и повышает ее на карбонильном. Этот сдвиг еще больше увеличивается в анионе кислоты:
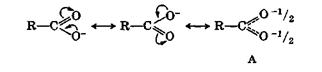
Результатом сдвига является полное выравнивание зарядов в анионе, который фактически существует в форме А - резонанс карбоксилат-аниона.
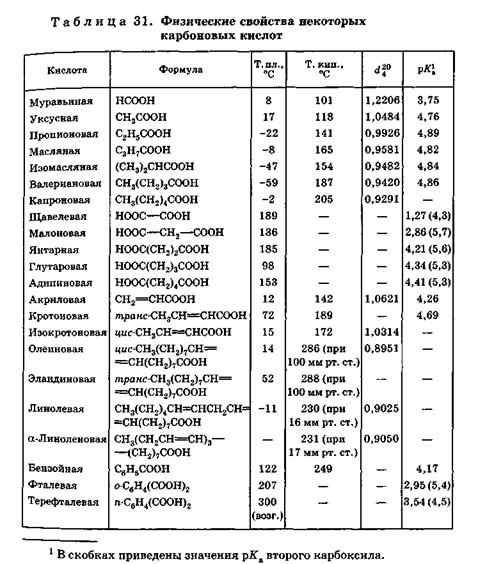
Первые четыре представителя ряда карбоновых кислот — подвижные жидкости, смешивающиеся с водой во всех отношениях. Кислоты, в молекуле которых содержится от пяти до девяти атомов углерода (а также изомасляная кислота), — маслянистые жидкости, растворимость их в воде невелика.
Высшие кислоты (от С10) — твердые тела, практически нерастворимы в воде, при перегонке в обычных условиях они разлагаются.
Муравьиная, уксусная и пропионовая кислоты имеют острый запах; средние члены ряда обладают неприятным запахом, высшие кислоты запаха не имеют.
 |
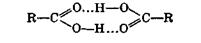 На физических свойствах карбоновых кислот сказывается значительная степень ассоциации вследствие образования водородных связей. Кислоты образуют прочные водородные связи, так как связи О—Н в них сильно поляризованы. Кроме того, карбоновые кислоты способны образовывать водородные связи с участием атома кислорода карбонильного диполя, обладающего значительной электроотрицательностью. Действительно, в твердом и жидком состоянии карбоновые кислоты существуют в основном в виде циклических димеров:
На физических свойствах карбоновых кислот сказывается значительная степень ассоциации вследствие образования водородных связей. Кислоты образуют прочные водородные связи, так как связи О—Н в них сильно поляризованы. Кроме того, карбоновые кислоты способны образовывать водородные связи с участием атома кислорода карбонильного диполя, обладающего значительной электроотрицательностью. Действительно, в твердом и жидком состоянии карбоновые кислоты существуют в основном в виде циклических димеров:
Такие димерные структуры сохраняются в некоторой степени даже в газообразном состоянии и в разбавленных растворах в неполярных растворителях.
 2014-02-13
2014-02-13 1833
1833
