Уравнения первого закона термодинамики в сложных закрытых ТС при двух фиксированных параметрах имеют вид:
- для изохорно-изотермического процесса (T,V =const): 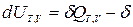 ℒТ,V ;
ℒТ,V ;
- для изобарно-изотермического процесса (T,p =const): 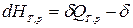 ℒТ,р.
ℒТ,р.
При написании этих уравнений использовалось правило знаков, принятое в термодинамике, т.е. 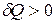 , если теплота подводится к ТС, и
, если теплота подводится к ТС, и 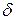 ℒ> 0, если работа совершается термодинамической системой. В термохимии принято противоположное правило знаков для теплоты, т.е. теплота
ℒ> 0, если работа совершается термодинамической системой. В термохимии принято противоположное правило знаков для теплоты, т.е. теплота 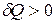 , (положительна), если она отводится от ТС. Тогда для конечных процессов 1-2 уравнение 1-го закона термодинамики будет иметь вид:
, (положительна), если она отводится от ТС. Тогда для конечных процессов 1-2 уравнение 1-го закона термодинамики будет иметь вид:
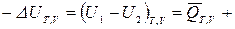 ℒТ,V, (1)
ℒТ,V, (1)
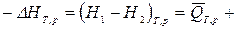 ℒТ,р, (2)
ℒТ,р, (2)
Соотношения (1) и (2) справедливы для любых процессов, обратимых и необратимых.
Для обратимого процесса ℒ=ℒ max, 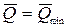 :
:
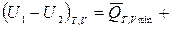 ℒТ,V max,(3)
ℒТ,V max,(3)
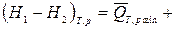 ℒТ,p max,(4)
ℒТ,p max,(4)
Для максимально возможного необратимого процесса ℒ=ℒ min=0, 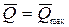 :
:
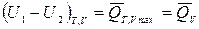 , (5)
, (5)
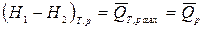 . (6)
. (6)
Соотношения (5) и (6) используются в химической термодинамике для расчета изохорного и изобарного тепловых эффектов химических реакций (ТЭХР). В этом случае работа ℒ max преобразуется в тепловую энергию неупорядоченного движения частиц (в теплоту 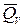 и
и 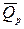 ).
).
В случае обратимого равновесного процесса перераспределения масс (уравнения (3) и (4)) величины 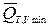 и
и 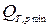 - это количества теплоты, которыми ТС обменивается с окружающей средой в процессах
- это количества теплоты, которыми ТС обменивается с окружающей средой в процессах 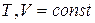 и
и 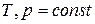 . ℒТ,V max и ℒТ,p max - максимальные количества работы немеханического характера, которые могут быть получены от ТС в процессах
. ℒТ,V max и ℒТ,p max - максимальные количества работы немеханического характера, которые могут быть получены от ТС в процессах 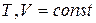 и
и 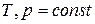 .
.
В случае необратимого процесса перераспределения массы в соответствии со вторым законом термодинамики работа ℒ max преобразуется в теплоту, количество которого равно изменению внутренней энергии 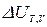 в процессе
в процессе 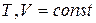 , или изменению энтальпии
, или изменению энтальпии 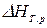 в процессе
в процессе 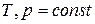 , протекающем в сложных термодинамических системах.
, протекающем в сложных термодинамических системах.
Химические реакции, при которых теплота отводится от термодинамической системы 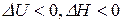 , чтобы конечные продукты имели ту же температуру, что и начальные реагенты, называются экзотермическими химическими реакциями. Химические реакции, сопровождающиеся поглощением теплоты
, чтобы конечные продукты имели ту же температуру, что и начальные реагенты, называются экзотермическими химическими реакциями. Химические реакции, сопровождающиеся поглощением теплоты 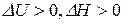 , при T=const, называются эндотермическими химическими реакциями.
, при T=const, называются эндотермическими химическими реакциями.
Рассмотрим два примера: 1. разрядка химического источника электроэнергии (аккумулятор, батарея карманного фонаря) – процесс обратимый: ℒ Т,p max - преобразуется в электрическую энергию, а 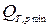 - отводится от системы. 2. Если замкнуть клеммы батареи накоротко, то получим максимально необратимый процесс: ℒ
- отводится от системы. 2. Если замкнуть клеммы батареи накоротко, то получим максимально необратимый процесс: ℒ 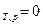 ,
, 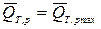 .
.
 2015-01-21
2015-01-21 700
700








