По тепловому механизму после химического взаимодействияпродукты реакции обладают большим запасом кинетической энергии. Эта энергия мо-жет а) рассеиваться в окружающем пространстве при соударениях молекул или в)излучением, а с) также расходоваться на разогрев реагирующей смеси.
Цепной механизм реакции; объясняется 1) перераспределением избыточной энергии, которая реализуется в реакции следующим образом: а)запас химической энергии, сосредоточенный в молекуле продукта первичной реак-ции, в)передается одной из реагирующих молекул, которая переходит в химически активное состояние. Подобные условия более благоприятны для протекания реакции, чем условия, при которых химическая энергия взаимодействия переходит в энергию теплового хаотического движения.
При таком механизме передачи энергии реакция приводит к образова-нию одной или нескольких новых активных частиц – возбужденных молекул, свободных радикалов или атомов. Таковы, например, атомарный водород, кислород, хлор, радикалы и гидроксил, и т.д. Все эти вещества, являясь хи-мически ненасыщенными, отличаются высокой реакционной способностью и могут реагировать с компонентами смеси, образуя в свою очередь, свобод-ные радикалы и атомы.Так образуется цепочка последовательных реакций.
|
|
|
Цепная реакция протекает различно, в 1).зависимости от того, сколько активных вторичных центров образуется на каждый израсходованный активный центр – один или больше одного. В первом случае общее число активных центров остается неизменным, и реакция протекает с постоянной (при данных температуре и концентрации) скоростью, т.е. стационарно. 2) Во втором случае число активных центров непрерывно возрастает, цепь разветвляяется и реакция самоускоряется.
Это неограниченное, до полного израсходования реагирующих компо-нентов, самоускорение воспринимается как самовоспламенение. Внешне ре-акция протекает так же, как и при тепловом самовоспламенении. Различие состоит в том, что при тепловом механизме в реагирующей смеси накапливается тепло,а при цепном механизме – активные центры. Оба фактора ведут к ускорению реакции. Цепное воспламенение принципиально может осуществляться при постоянной температуре без заметного разогрева смеси.
Типичным примером цепной разветвленной реакции является процесс окисления водорода (взрыв гремучего газа).
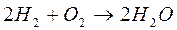
Реакция протекает по схеме:
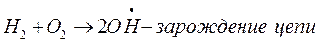
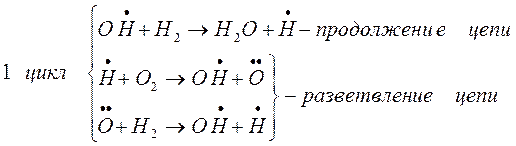
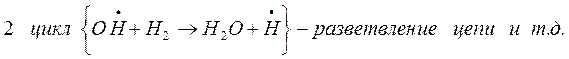
Разветвление цепи проходит при следующих реакциях:
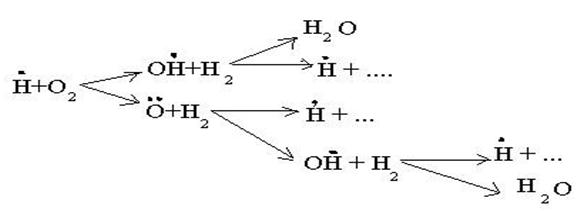
когда за один цикл превращений каждый вступающий в реакцию атом водо-рода вызывает образование двух молекул воды и трех новых атомов водоро-да.
|
|
|
Обрыв цепей проходит либо на стенке:
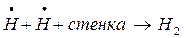 ,
,
либо в объеме: 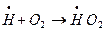 с образованием малоактивного радикала НО2.
с образованием малоактивного радикала НО2.
Причинами обрыва цепи в объеме смеси является:
1) побочная реакция активного центра с примесями, содержащимися в смеси;
2) рассеивание активной частицей избыточной химической энергии при столкновениях с неактивными молекулами.
3).Обрыв цепи на стенках реакционного сосуда объясняется адсорбцией активных центров на его поверхности.
Условием ускорения реакции является в данном случае превышение числа разветвления цепей над числом их обрывов. Цепные реакции могут протекать и при полном отводе тепла, т.е. в изотермических условиях, тогда как при тепловом механизме реакция должна была бы затухнуть. По цепной теории появление тепла – только следствие процесса, а не причина возникно-вения горения.
 2015-01-30
2015-01-30 480
480








