Молекула – наименьшая частица вещества, обладающая его химическими свойствами.
Согласно теории химической связи, устойчивому состоянию элемента соответствует структура с электронной формулой внешнего уровня s2p6 (аргон, криптон, радон, и другие).
При образовании химической связи атомы стремятся приобрести такую устойчивую структуру. При этом возможны три типа химической связи.
Ионная связь – осуществляется в результате электростатического взаимодействия противоположно заряженных ионов. При взаимодействии атомов металлических и неметаллических элементов (разность электроотрицательности больше 1,9) атомы металлических элементов отдают лишние электроны внешнего уровня, переходя в положительно заряженные ионы, а атомы неметаллических элементов принимают электроны, достраивая внешний уровень до восьми электронов, переходя в отрицательно заряженные ионы.
Например, 12Mg 1s22s22p63s2 -2e = 1s22s22p6
Mg -2e = Mg2+
8F 1s22s22p5 +e = 1s22s22p6
F +e = F-
Так как электрическое поле иона имеет сферическую симметрию, то при образовании связи между двумя противоположно заряженными ионами возможно электростатическое взаимодействие и с другими ионами. У ионных соединений определяющее значение имеют ненасыщенность и ненаправленность связи. Ионные соединения при обычных условиях являются кристаллическими веществами.
Металлическая связь. Осуществляется за счёт делокализованных электронов. При взаимодействии атомов только металлических элементов (в веществах называемых металлами) «лишние» электроны внешнего уровня способны перемещаться по металлу, но находятся в поле действия положительных ионов. Это взаимодействие подвижных ионов определяет, что соединения с металлической связью при обычных условиях являются кристаллами, которые имеют специфические свойства.
Ковалентная связь осуществляется за счёт электронной пары одновременно принадлежащей двум атомам.
Например: На внешнем уровне атома хлора 7 электронов
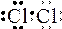
При взаимодействии с другим атомом хлора образуется устойчивая структура молекула Cl2, где у каждого атома на внешнем уровне 8 электронов.
Рассмотрим свойства ковалентной связи с точки зрения метода валентных связей (МВС). Основные положения МВС.
1. В образовании ковалентной связи принимают участие два электрона с противоположными спинами.
2. Образование ковалентной связи происходит за счёт перекрывания атомных орбиталей валентных электронов.
3. Связь образуется по линии максимального перекрывания атомных орбиталей.
Ковалентная связь характеризуется свойствами: насыщаемость, направленность и полярность.
Способность атома к образованию химических связей называют валентностью элемента. Количественной мерой валентности принято считать число электронов способных образовывать химические связи – число валентных электронов.
Для s – элементов валентными электронами является s – электроны внешнего уровня;
Для р – элементов s- и р – электроны внешнего уровня;
Для d – элементов s – электроны внешнего уровня и d – электроны предвнешнего уровня.
Например, 11Na – валентный электрон 3s1
56Ba - 6s2 13Al – 3s23p1 53J – 5s25p5 22Ti – 4s23d2
Большинство соединений с ковалентной связью образовано по обменному механизму, при котором каждый атом поставляет по одному (неспаренному) электрону для образования общей пары.
Насыщаемость – это свойство, которое определяет стехиометрический (определённый) состав устойчивого соединения с ковалентной связью – молекулы. Для соединений образованных по обменному механизму валентность элемента определяется числом неспаренных валентных электронов.
Например, элементы кислород и водород образуют молекулу состава Н2О.
Для
8О валентные электроны 2s
22p
4, которые расположены по орбиталям 2
s p
У атома элемента кислорода имеется два неспаренных валентных электрона, т.е. валентность равна 2.
Для 1Н валентный электрон 1s1, т.е. валентность равна 1.
Однако большинство элементов могут иметь переменную валентность. Это возможно в том случае, если в пределах одного энергетического уровня имеются свободные орбитали.
Например, элемент углерод и кислород образуют СО и СО2
Для
6С валентные электроны 2s
22p
2, которые расположены по орбиталям 2, т.е. в основном состоянии валентность будет
s p
равна 2. В возбуждённом состоянии электрон с s – подуровня поднимается на р – подуровень: 2s
12p
3 2,т.е. валентность будет равна 4.
s p
Исходя из свойств соединений СО и СО2 можно сделать вывод о том, что элемент в возбуждённом состоянии образует более устойчивое соединение.
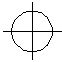 Направленность – это свойство определяющее геометрическую форму молекулы с ковалентной связью. При образовании связи принимают участие атомные орбитали различной формы:
Направленность – это свойство определяющее геометрическую форму молекулы с ковалентной связью. При образовании связи принимают участие атомные орбитали различной формы:
 s – электроны имеют форму орбитали
s – электроны имеют форму орбитали
 р – электроны имеют форму орбитали
р – электроны имеют форму орбитали
Однако, когда атом находится в возбуждённом состоянии в образовании равноценных связей участвуют s- и р– гибридные орбитали.
Различают три типа гибридизации:
1. Один s – электрон и один р – электрон: s р – гибридизация
- -две гибридные связи
2. Один s – электрон и два р – электрона: s р2 – гибридизация
- -три гибридные связи.
3. Один s – электрон и три р – электрона: s р3 – гибридизация
- -четыре гибридные связи.
В зависимости от направления перекрывания атомных орбиталей различают: s - и π – связи.
s -связь возникает при перекрывании орбиталей вдоль оси, соединяющей ядра взаимодействующих атомов. s - связь наблюдается при перекрывании s – s –, р – р – s - р – орбиталей и т.д.
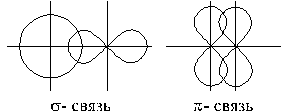
Рис. 3. Перекрывание электронных облаков
при образовании s - и p - связей
π – связь возникает при перекрывании орбиталей по обе стороны от оси соединяющей ядра атомов. Наблюдается при перекрывании р – р орбиталей расположенных перпендикулярно оси, соединяющей ядра атомов.
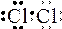
 Направленность – это свойство определяющее геометрическую форму молекулы с ковалентной связью. При образовании связи принимают участие атомные орбитали различной формы:
Направленность – это свойство определяющее геометрическую форму молекулы с ковалентной связью. При образовании связи принимают участие атомные орбитали различной формы: s – электроны имеют форму орбитали
s – электроны имеют форму орбитали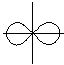
 р – электроны имеют форму орбитали
р – электроны имеют форму орбитали
 2015-01-30
2015-01-30 529
529