Вид 1. Выберите наиболее правильный ответ.
1.1. Молекулярная масса большинства белков находится в пределах ….
а) от 6000 до 10000000 и выше
в) свыше 50000
б) от 30000 и выше
г) свыше100000
1.2. Глутаминовая кислота при рН 10 находится в виде иона ….
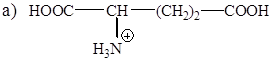 в)
в) 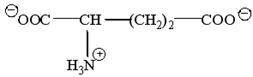
б) 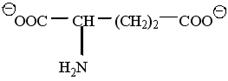 г)
г) 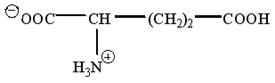
1.3. Смесь аминокислот, содержащая аспартат (pI 3,0) и лизин (рI 9,7), разделяется методом ионообменной хроматографии. В каком порядке будут выходить аминокислоты из колонки, заполненной триметиламинополистерольной смолой, имеющей положительно заряженные группы (анионообменник) при рН 7?
а) асп, лиз
б) лиз, асп
1.4. Детергенты (тритон Х-100, додецилсульфат натрия) при экстракции белков к среде извлечения добавляют для ….
а) повышения устойчивости белков к денатурации
б) перевода белков в изоэлектрическое состояние
в) разрушения белково-липидных комплексов
1.5.Оптическое явление, доказывающее коллоидные свойства белков,- это ….
а) явление светорассеивания – конус Тиндаля
б) вращение плоскости поляризованного света
в) интенсивное светопоглощение при длине волны 280 нм
Вид 2. Установите соответствие.
2.1. Классифицируйте приведенные ионообменные смолы в зависимости от заряда функциональных групп.
1. триметиламинополистирол а. катионообменник
2. диэтиламиноэтилцеллюлоза б. анионообменник
3. карбоксиметилцеллюлоза
4. сульфонированные полистиролы
2.2. В каком направлении будут двигаться в электрическом поле следующие белки при рН 6,3?
1. овальбумин (ИЭТ 4,6) а) останется на старте
2. β-лактоглобулин (ИЭТ 6,3) б) движется к катоду
3. химотрипсин (ИЭТ 9,5) в) движется к аноду
Вид 3. Правильное сочетание ответов.
3.1. Смесь аминокислот, содержащая:
1) глицин
2) аланин
3) лизин
4) глутаминовую кислоту
5) аргинин
подвергли электрофорезу на бумаге при pH=6.
Какие аминокислоты будут двигаться при этом условии к «аноду»?
3.2. Метод разделения белков, основанный на различии размера белковых молекул -
1. кристаллизация
2. диализ
3. ионообменная хроматография
4. гель-фильтрация
5. изоэлектрическое фокусирование
3.3. Электрофоретическая процедура, не зависящая от заряда белка -
1. диск-электрофорез
2. зональный электрофорез
3. изоэлектрическое фокусирование
4. электрофорез в полиакриламидном геле с добавлением детергента (натрия додецилсультата)
5. электрофорез на бумаге
Вид 4. Определите правильность утверждений и связь между ними.
4.1. Очистить раствор белка от низкомолекулярных примесей можно методом гель-фильтрации на сефадексе, потому что с помощью этого метода можно разделить вещества с разной молекулярной массой.
4.2. По степени дисперсности растворы белков являются истинными растворами, а по свойствам – коллоидными, так как белки являются высокомолекулярными соединениями.
 2015-01-07
2015-01-07 1177
1177








