Обозначим начальные концентрации реагирующих веществ [NO] = а, [O2] = в. Согласно закону действующих масс, скорость реакции до изменения объема равна ν1 = kа 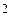 в. После уменьшения объема гомогенной системы в 3 раза концентрация каждого из реагирующих веществ увеличится в 3 раза:
в. После уменьшения объема гомогенной системы в 3 раза концентрация каждого из реагирующих веществ увеличится в 3 раза:
[NO] = 3 a, [O 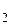 ] = 3 b,
] = 3 b,
при новых концентрациях скорость реакции:
ν2 = k (3 a) 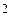 (3 b) = 27 ka
(3 b) = 27 ka 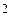 b.
b.
Отсюда
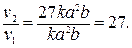
Следовательно, скорость реакции увеличится в 27 раз.
Пример 2. Реакция между веществами А и В протекает по уравнению 2 А + В = С. Начальные концентрации равны [ A ] = 6 моль/л и [ B ] = 3 моль/л. Константа скорости реакции равна 0,6 л 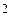 /моль
/моль 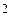 ×с. Вычислите скорость реакции в начальный момент и в момент, когда в реакционной смеси останется 40 % вещества А.
×с. Вычислите скорость реакции в начальный момент и в момент, когда в реакционной смеси останется 40 % вещества А.
 2015-02-27
2015-02-27 613
613








