По табличным данным построим график D = f(C):
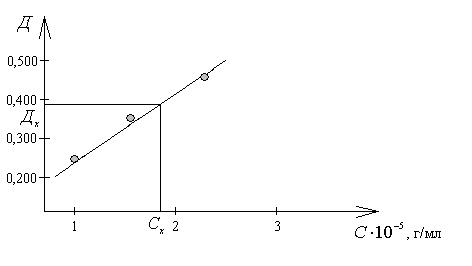
По графику находим Сх, соответствующую оптической плотности (0,390) раствора с неизвестной концентрацией. Эта концентрация равна 1,85∙10 –5 г/мл.
Задачи
341–344 При кислотно-основном титровании 20 мл раствора вещества А раствором вещества В с концентрацией 0,1 н для определения точки эквивалентности по резкому изменению рН получены следующие данные (табл. 14.3). Постройте кривую титрования в координатах рН = f(VB) и определите объем титранта В в точке эквивалентности. Запишите уравнение реакции и рассчитайте нормальную концентрацию раствора А.
345–348 По данным эксперимента, полученным фотоколометрическим методом (табл. 14.4), постройте график зависимости оптической плотности D раствора А от его концентрации и с его помощью определите неизвестную концентрацию раствора А, если измеренная оптическая плотность этого раствора равна Dх.
349–352 Постройте кривую кондуктометрического титрования 30 мл раствора А раствором титранта В с концентрацией 0,5 н в координатах c = f(VB) по данным таблицы 14.5.
Определите объем титранта В в точке эквивалентности и рассчитайте нормальную концентрацию раствора А.
353–356 При полярографировании стандартных растворов свинца (II) получили следующие результаты:
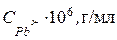 | 0,50 | 1,00 | 1,50 | 2,00 |
| h, мм | 4,0 | 8,0 | 12,0 | 16,0 |
Навеску алюминиевого сплава массой m (г) растворили и раствор разбавили до 50,00 мл. Высота полярографической волны свинца в полученном растворе оказалось равной hX. Вычислите массовую долю (%) свинца в анализируемом образце (см. табл. 14.6).
Таблица 14.6
| Вариант | ||||
| m, г | 2,5000 | 5,134 | 5,300 | 4,518 |
| h, мм | 6,0 | 9,0 | 11,0 | 8,0 |
357 Какую массу образца, содержащего 30 % серы, нужно взять для гравиметрического анализа, чтобы получить 0,300 г осадка BaSO4?
Ответ: 0,137г.
358 Какую массу вещества, содержащего 50 % железа, нужно взять для гравиметрического анализа, чтобы масса прокаленного осадка Fe2O3 была
0,100 г?
Ответ: 0,140 г.
359 Рассчитайте массу образца, содержащего 20 % Р2О5, необходимую для получения 0,300 г Mg2P2O7 в гравиметрическом анализе.
Ответ: 0,960 г.
360 Рассчитайте массу цемента, содержащего 30 % MgO, необходимого для получения 0,500 г осадка оксихинолината магния Mg(C9H6ON)2 в гравиметрическом анализе.
Ответ: 0,150 г.
Таблица 14.3
| № задачи | Раствор вещества А | Раствор вещества В | Объем раствора вещества В, VB (мл) | |||||||
| Объем раствора вещества В, VB (мл) | ||||||||||
| H2SO4 | NaOH | VB, мл | ||||||||
| pH | 1,25 | 1,30 | 1,44 | 1,58 | 1,76 | 1,96 | 2,38 | |||
| VB, мл | ||||||||||
| pH | 3,15 | 8,82 | 10,62 | 11,23 | 11,52 | 11,73 | ||||
| КОН | HCl | VB,, мл) | ||||||||
 |  pH pH | 11,94 | 11,92 | 11,87 | 11,53 | 11,12 | 10,04 | 3,18 | ||
| VB, мл | ||||||||||
| pH | 2,34 | 2,05 | 1,91 | 1,81 | 1,75 | 1,71 | ||||
| CH3COOH | NaOH | VB, мл | ||||||||
| pH | 2,97 | 3,41 | 3,98 | 4,18 | 4,45 | 4,69 | 5,12 | |||
| VB, мл | ||||||||||
| pH | 5,79 | 6,80 | 12,02 | 12,25 | 12,40 | 12,52 | ||||
| NaOH | H2SO4 | VB, мл | ||||||||
| pH | 11,85 | 11,77 | 11,63 | 11,32 | 10,71 | 8,91 | 3,14 | |||
| VB, мл | ||||||||||
| pH | 2,48 | 2,19 | 2,04 | 1,96 | 1,94 | 1,92 |
 |
Таблица 14.4
| № | А | CA – концентрация А, моль/л | Dx | ||||||
| Оптическая плотность D | |||||||||
| NiSO4 | CA | 0,25 | 0,5 | 0,75 | 1,0 | 1,25 | 0,493 | ||
| D | 0,127 | 0,273 | 0,402 | 0,531 | 0,669 | ||||
| Cu(NH3)4SO4 | CA | 0,1 | 0,15 | 0,20 | 0,25 | 0,30 | 0,35 | 0,545 | |
| D | 0,209 | 0,315 | 0,420 | 0,510 | 0,614 | 0,691 | |||
 347 347 | ((CH3)2C2N2OH)2Ni | CA | 0,15 | 0,25 | 0,50 | 0,75 | 1,00 | 1,25 | 0,320 |
| D | 0,075 | 0,112 | 0,207 | 0,291 | 0,382 | 0,479 | |||
| Комплекс Fe (II) с алициловой кислотой | CA ∙10+5 | 1,09 | 1,98 | 3,03 | 3,94 | 5,12 | 0,610 | ||
| D | 0,151 | 0,295 | 0,452 | 0,595 | 0,714 |
 |
Таблица 14.5
| № | A | B | Объем раствора вещества B, VB (мл) | ||||||||
| Удельная электропроводность (c) | |||||||||||
 349 349 | BaCl2 | Na2SO4 | VB | 0,0 | 0,5 | 1,0 | 1,5 | 2,0 | 2,5 | 3,0 | 3,5 |
| c∙103 | 10,01 | 9,62 | 9,31 | 8,78 | 8,35 | 7,80 | 7,48 | 7,96 | |||
| VB | 4,0 | 4,5 | 5,0 | ||||||||
| c∙103 | 8,43 | 8,70 | 9,14 | ||||||||
| HCl | NaOH | VB | 0,0 | 1,0 | 2,0 | 3,0 | 4,0 | 5,0 | 6,0 | 7,0 | |
| c∙103 | 4,95 | 4,02 | 2,89 | 1,72 | 2,05 | 3,01 | 3,90 | 7,43 | |||
| VB | 8,0 | ||||||||||
| c∙103 | 5,78 | ||||||||||
| CH3COOH | NaOH | VB | 0,0 | 1,0 | 2,0 | 3,0 | 4,0 | 5,0 | 6,0 | 7,0 | |
| c∙103 | 1,61 | 1,70 | 1,81 | 1,92 | 2,02 | 2,12 | 2,23 | 3,03 | |||
| VB | 8,0 | 9,0 | 10,0 | ||||||||
| c∙103 | 4,52 | 5,89 | 7,23 | ||||||||
| n -нитроанилин | HClO4 | VB | 0,0 | 1,0 | 2,0 | 3,0 | 3,5 | 4,0 | 4,5 | 5,0 | |
| c∙103 | 1,96 | 2,21 | 2,45 | 2,62 | 3,61 | 5,54 | 7,26 | 9,10 |
 |
ТАБЛИЦА ВАРИАНТОВ
Студент выбирает себе контрольное задание по двум последним цифрам номера студенческого билета
| Вариант | Номер задач | ||||||
| Продолжение таблицы вариантов | |||||||
| Окончание таблицы вариантов | |||||||
 2015-02-27
2015-02-27 1345
1345








