Построение калибровочного графика. В мерные колбы на 50 см3 вносят 0,1; 0,5; 1,0; 1,5; 2,0; 3,0 см3 рабочего стандартного раствора хлорида аммония с концентрацией ионов аммония 0,05 мг/см3 и доводят каждый раствор до метки безаммиачной водой. Концентрации NH4+ в полученных растворах равны соответственно 0,1; 0,5; 1,0; 1,5; 2,0; 3,0 мг/дм3. Добавляют 20-30 см3 безаммиачной воды, 1 каплю раствора сульфата марганца, затем при непрерывном помешивании приливают 0,5 см3 раствора гипохлорита натрия и сразу же 0,6 см3 фенолята натрия, затем доводят объем водой до метки. Энергично взбалтывают 2 мин. Дают постоять 10 мин для развития окраски и измеряют оптическую плотность в кювете 2 см при l = 625 нм (красно-оранжевый светофильтр). Раствор-фон готовят в колбе на 50 см3, используя безаммиачную воду и те же количества реактивов.
Калибровочный график строят в координатах оптическая плотность –концентрация ионов NH4+, мг/дм3.
Определение концентрации ионов аммония. В мерную колбу вместимостью 50 см3 отбирают10 см3 первоначальной пробы воды или раствора, полученного после отгонки аммиака (см. лаб. раб. №14). Этот раствор обрабатывают, как описано выше, и определяют его оптическую плотность. Расчет. Содержание аммонийных ионов (Х) в мг/дм3 находят по формуле:
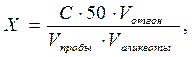 |
где С – концентрация ионов аммония, найденная по графику, мг/дм3;
50– объем раствора, приготовленного для фотометрирования, см3;
Vпробы – объем пробы воды, взятой для анализа или для отгона, см3;
Vотгон – объем, до которого был разбавлен отгон, см3;
Vаликвоты –объем аликвоты отгона, взятой для анализа, см3.
 2015-02-27
2015-02-27 1731
1731








