1. Определение порога коагуляции.
В четыре сухие чистые пробирки пипеткой отмерьте по 10 мл гидрозоля – Fе(ОН)3. Одна пробирка служит для сравнения; три остальных - для определения порога коагуляции.
К коллоидному раствору в первой пробирке градуированной пипеткой по каплям прибавьте двумолярный раствор NаС1. После каждой капли золь перемешивайте. Раствор NаС1 прибавляйте, пока не будет обнаружена явная коагуляция (изменение окраски, помутнение и пр.) по сравнению с исходным золем. Запишите объем затраченного раствора NаС1, принимая объем капли равным приблизительно 0,05 мл.
К золю во второй пробирке, градуированной пипеткой по каплям прибавьте сантимолярный (0,01 М) раствор Nа2SО4, как и в первом случае, до появления явной коагуляции.
К золю в третьей пробирке, градуированной пипеткой по каплям, прибавьте миллимолярный (0,001М) раствор Nа3РО4, как и в предыдущих случаях, до явной коагуляции. Объем прилитого раствора Nа3РО4 запишите.
На основании произведенных измерений найдите порог коагуляции и коагулирующую способность соответствующих для каждого электролита. Измерения и результаты их обработки необходимо занести в таблицу 18 (в таблице указаны примерные данные):
Таблица 18
Коагуляция гидрозоля Fе(ОН)3 электролитами
| № п/п | Электролит | Коагулирующий ион | Nэл, моль/л | Vэл,мл | V в пересчете на 0,001 м р-р,(мл) | П, моль/литр | К |
| NaCl Na2SO4 Na3PO4 | Cl– SO42– PO43– | 2 M 0.01 M 0.001 M | 0,125 | 2,0 0,1 | 0,02 0,5 1,0 |
П= 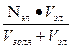
К= 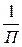 ,где
,где
П- порог коагуляции
Nэл – концентрация электролита
Vэл – объем израсходованного электролита
Vзоля – объем взятого для коагуляции золя
К – коагулирующая способность.
Из таблицы сделайте выводы о зависимости между порогом коагуляции и коагулирующей способностью ионов, с одной стороны, и валентностью коагулирующего иона, с другой стороны.
Путем деления более высокого порога коагуляции на более низкий определить, во сколько раз коагулирующая способность трехвалентного иона выше одновалентного.
 2015-02-04
2015-02-04 1089
1089
