Лейкоциты или белые кровяные шарики обладают полной ядерной структурой. Их ядро может быть округлым, в виде почки или многодольчатым
Размеры лейкоцитов варьируют от 4 мкм до 20 мкм. Продолжительность жизни гранулоцитов и моноцитов от 4-5 дней до 20 дней, лимфоцитов -до 100-120 дней. Количество лейкоцитов в периферической крови колеблется в пределах 4х109/л - 9х109/л в зависимости от баланса гормонов, нервного напряжения, сезона, времени суток. Врачи следят за количеством лейкоцитов, поскольку любое его изменение зачастую является признаком болезни или инфекции. Лейкоциты - это пехота, защищающая организм от инфекции. Эти клетки защищают организм путем фагоцитоза (поедания) бактерий или же посредством иммунных процессов - выработки особых веществ, которые разрушают возбудителей инфекций. Лейкоциты действуют в основном вне кровеносной системы, но в участки инфекции они попадают именно с кровью.
Содержание лейкоцитов может быть увеличено (лейкоцитоз) или уменьшено (лейкопения).
|
|
|
Нейтрофилы составляют60-70%всехлейкоцитовижшно/лсл наиболее важными клетками защиты организма от бактерий и их токсинов. Проникая через стенки капилляров, нейтрофилы попадают в межтканевые пространства, где осуществляется фагоцитоз — поглощение и переваривание бактерий и других инородных белковых тел.
Эозинофилы (1 -4% от общего числа лейкоцитов) адсорбируют на свою поверхность антигены (чужеродные белки), многие тканевые вещества и токсины белковой природы, разрушая и обезвреживая их. Кроме дезинтоксикационной функции эозинофилы принимают участие в предупреждении развития аллергических реакций.
Базофилы составляют не более 0.5% всех лейкоцитов и осуществляют синтез гепарина, входящего в антисвертывающую систему крови. Базофилы участвуют также в синтезе ряда биологически активных веществ и ферментов (гистамин, серотонин, РНК, фосфотаза, липаза, пероксидаза).
Лимфоциты (25-30% от числа всех лейкоцитов) играют важнейшую роль в процессах образования иммунитета организма, а также активно участвуют в нейтрализации различных токсических веществ.
Е. Grawitz (1910) впервые назвал лейкоцитоз, наступающий после мышечной работы, миогенным лейкоцитозом. Он считал, что лейкоцитоз наступает вследствие интоксикации организма продуктами обмена веществ, в частности белкового, а увеличение количества лейкоцитов способствует обезвреживанию этих продуктов. Одним из подтверждений этого положения являлось то, что степень увеличения количества лейкоцитов зависит от мощности работы.
1-яфаза (лимфоцитарная) возникает после относительно небольшой работы. Она характеризуется незначительным лейкоцитозом — (10… 12)х109/л, снижением относительного количества нейтрофилоцитов, абсолютным и относительным увеличением количества лимфоцитов и относительным уменьшением количества эозинофилоцитов.
2-я фаза (нейтрофильная) появляется после сравнительно большой работы. Она характеризуется большим увеличением количества лейкоцитов — (16… 18) x109/л — по сравнению с 1-й фазой, резким увеличением количества нейтрофилоцитов со сдвигом влево, уменьшением количества лимфоцитов и эозинофилоцитов.
3-я фаза (интоксикационная) протекает по 2 типам: регенеративному и дегенеративному. При регенеративном типе происходит значительное увеличение количества лейкоцитов — до (20… 50) X 109/л, увеличение количества нейтрофилоцитов со сдвигом влево, уменьшение количества лимфоцитов (1 %), полное исчезновение эозинофилоцитов. Дегенеративный тип характеризуется такими же изменениями морфологического состава, как и регенеративный, но с менее выраженным лейкоцитозом (10… 15) X 109/л, более резким сдвигом нейтрофилов влево, абсолютной лимфо- и эозинопенией и появлением дегенеративных форм. Интоксикационная фаза миогенного лейкоцитоза свидетельствует о чрезмерности нагрузки.
Таким образом, появление в периферической крови лимфоцитарной фазы миогенного лейкоцитоза в ответ на значительную нагрузку является положительным прогностическим признаком высокого функционального состояния спортсмена, и наоборот, появление нейтрофильной или интоксикационной фазы после относительно небольшой нагрузки свидетельствует о его недостаточной подготовленности к выполнению работы. В то же время отсутствие изменений в ответ на физическую нагрузку относительного количества форменных элементов в лейкоцитарной формуле следует считать либо признаком плохой приспособляемости организма к физическим нагрузкам, либо чрезмерностью физического напряжения для данного индивидуума.
|
|
|
29. Тромбоциты.
Тромбоциты — это мелкие, безъядерные кровяные пластинки
(бляшки Биццоцери) неправильной формы, диаметром 2-5 микрон. Несмотря на отсутствие ядра, тромбоциты обладают активным метаболизмом и являются третьими самостоятельными живыми клетками крови. Число их в периферической крови колеблется от 250 до 400 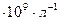 продолжительность жизни тромбоцитов составляет 8-12 дней.
продолжительность жизни тромбоцитов составляет 8-12 дней.
Тромбоцитам принадлежит ведущая роль в свертывании крови. Недостаток тромбоцитов в крови —тромбопения— наблюдается при некоторых заболеваниях и выражается в повышенной кровоточивости.
Уже через доли секунды после повреждения стенки сосуда в зоне травмы наблюдается спазм сосудов, и развивается цепь тромбоцитарных реакций, в результате которых образуется тромбоцитарная пробка. Прежде всего, происходит активация тромбоцитов факторами, выделяющимися из поврежденных тканей сосуда, а также малыми количествами тромбина — фермента, образующегося в ответ на повреждение. Затем происходит склеивание (агрегация) тромбоцитов друг с другом и с фибриногеном, содержащимся в плазме крови, и одновременное прилипание (адгезия) тромбоцитов к коллагеновым волокнам, находящимся в стенке сосуда, и поверхностным адгезивным белкам клеток эндотелия. В процесс вовлекается все большее и большее число тромбоцитов, поступающих в зону повреждения.
Первая стадия адгезии и агрегации обратима, но позже эти процессы становятся необратимыми. Агрегаты тромбоцитов уплотняются, образуя пробку, плотно закрывающую дефект в сосудах малого и среднего размера. Из адгезированных тромбоцитов высвобождаются факторы, активирующие все клетки крови и некоторые факторы свертывания, находящиеся в крови, в результате чего на основе тромбоцитарной пробки формируется фибриновый сгусток. В сети фибрина задерживаются форменные элементы крови и в результате образуется кровяной сгусток. Позднее из сгустка вытесняется жидкость, и он превращается в тромб, который препятствует дальнейшей потере крови, он же является барьером для проникновения патогенных агентов. Такая тромбоцитарно-фибриновая гемостатическая пробка может противостоять повышенному кровяному давлению после восстановления тока крови в поврежденных сосудах среднего размера.
|
|
|
Механизм прилипания тромбоцитов к эндотелию сосудов в зонах с малой и большой скоростью тока крови различается набором так называемых адгезивных рецепторов — белков, расположенных на клетках кровеносных сосудов.
Свертывание крови осуществляется посредством особой функциональной системой организма - свертывающей системой крови.
Свертывающая система крови - это совокупность органов и тканей, синтезирующих и утилизирующих ряд факторов, обеспечивающих свертывание крови в месте повреждения ткани.
Печень, а также ретикулярная система, являются основными органами, продуцирующими эти факторы свертывания. В настоящее время принято выделять 13 таких факторов. Все их делят на плазменные, тканевые и клеточные.
Под противосвертывающей системой следует понимать совокупность органов и тканей, которые синтезируют и утилизируют группу факторов, обеспечивающих жидкое состояние крови, то есть препятствующих свертыванию крови в сосудах. К таким органам и тканям относятся сосудистая система, печень, некоторые клетки крови и другое. Эти органы и ткани вырабатывают вещества, которые получили на звание ингибиторов свертывания крови или естественных антикоагулянтов. Они вырабатываются в организме постоянно, в отличие от искусственных антикоагулянтов, которые вводятся при лечении предтромбических состояний.
 2015-03-20
2015-03-20 1884
1884








