1. Молярная масса этого соединения равна 61,7 г/моль, если оно содержит одну этильную группу и 123,4 г/моль, если таких групп две. Первый ответ невозможен, т. к. молярная масса цинка больше, чем 61,7. Второй ответ соответствует молекуле диэтилцинка, Et2Zn.
2. Содержание углерода и водорода в Х вместе составляет 81,8 %. Это заставляет предположить, что цинк в молекуле Х отсутствует, а оставшиеся 18,2 % приходятся на кислород. Тогда молекулярная формула Х: С5Н12О. Это соединение образуется из этилового эфира муравьиной кислоты (HCO2C2H5) и диэтилцинка, генерируемого in situ из цинка и этилиодида. Пять атомов углерода в Х могут оказаться двумя путями: а) 3 атома углерода из этилформиата и 2 атома из диэтилцинка; б) 1 атом из этилформиата и 4 атома из диэтилцинка. В первом случае молекула Х должна содержать также два атома кислорода, что не соответствует рассчитанной молекулярной формуле. Второй вариант реализуется, если несущий частичный отрицательный заряд атом углерода из диэтилцинка атакует по несущему частичный положительный заряд карбонильному атому углерода, образовавшийся интермедиат отщепляет алкоголят цинка с образованием пропионового альдегида, который реагирует далее со второй молекулой диэтилцинка.
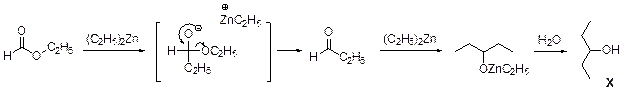
3. Из данных по содержанию в Y разных элементов можно определить молекулярную формулу Y как С9Н16O3. Учитывая ответ на предыдущий вопрос, можно сделать вывод, что диэтилцинк реагирует только по одной сложноэфирной группе:
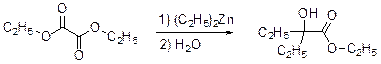
4. Молекулярный пик галогеналкана А проявляется в виде дублета в соотношении 1: 1. Это говорит о том, что один из атомов, присутствующих в молекуле, имеет два изотопа, причем их содержание в природе равно примерно 1: 1. Из четырех галогенов, углерода и водорода такое распределение имеет только бром. Молекулярная формула А: С n H2 n +1Br. Тогда 12 n / (14 n + 81) = 0,22. Отсюда n = 2. Вещество А – этилбромид. При его реакции с магнием теоретически может образоваться два продукта: диэтилмагний (аналогично реакции с цинком) или этилмагнийбромид. Как известно, реактивы Гриньяра – это алкилмагнийгалогениды. Это можно определить и из данных по содержанию в В водорода: значение, данное в условии, согласуется с формулой C2H5MgBr, но не с формулой (C2H5)2Mg. Когда реактив Гриньяра вылили на сухой лед, прошла реакция C2H5MgBr с СО2 с образованием C2H5СО2– MgBr+, а после нейтрализации выделили соответствующую кислоту С. Если сухой лед добавлять к избытку C2H5MgBr, образующаяся соль реагирует далее. После гидролиза выделяется диэтилкетон (D). Реакция этилбромида с водной щелочью дает этанол (F), который при нагревании с пропионовой кислотой в присутствии H2SO4 превращается в этилпропионат G.
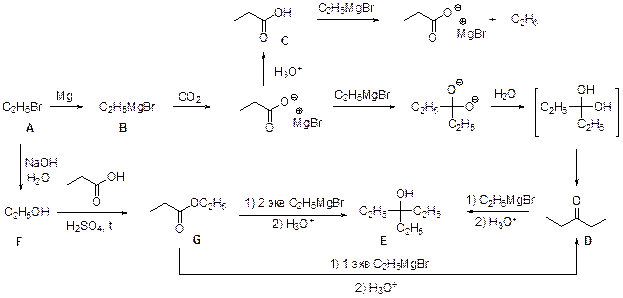
Система оценивания:
1. 2 балла.
2. 2 балла
3. 2 балла
4. 7 структур по 2 балла. Всего 14 баллов.
Итого 20 баллов.
 2015-04-12
2015-04-12 402
402








