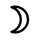 | – серебро, Луна, понедельник |  | – огонь (элемент) |
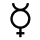 | – ртуть, Меркурий, среда, философская Ртуть |  | – воздух (элемент) |
 | – медь, Венера, пятница |  | – вода (элемент) |
 | – золото, Солнце, воскресенье |  | – земля (элемент) |
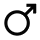 | – железо, Марс, вторник |  | – сера, философская Сера |
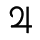 | – олово, Юпитер, четверг |  | – соль, философская Соль |
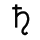 | – свинец, Сатурн, суббота | 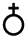 | – эликсир (философский камень) |
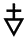 | – Великое делание (трансмутация) |  | – завершение Великого делания |
К числу несомненных практических достижений греко-египетских алхимиков следует отнести открытие явления амальгамирования металлов (описано Диоскоридом, I век н.э.). Александрийскими алхимиками был усовершенствован способ извлечения золота и серебра из руд, для чего широко применялась ртуть, получаемая из киновари или каломели. Амальгаму золота начали применять для позолоты. Алхимиками был разработан также способ очистки золота купелированием – нагреванием руды со свинцом и селитрой.
Помимо практического значения, уникальная способность ртути образовывать амальгаму привела к появлению представления о ртути, как об особом, "первичном" металле. Тому же способствовали и необычные свойства соединения ртути с серой – киновари, – которая в зависимости от условий получения имеет различную окраску – от красной до синей.
Первым значительным представителем александрийской алхимии, имя  которого дошло до наших дней, являлся Болос Демокритос из Менде, известный ещё как Псевдо-Демокрит (около 200 до н.э.). Написанная Болосом книга "Физика и мистика" состоит из четырёх частей, посвящённых золоту, серебру, драгоценным камням и пурпуру. У Болоса впервые сформулирована идея трансмутации металлов – превращения одного металла в другой, прежде всего неблагородных металлов (свинца или железа) в золото, ставшая основной задачей всего алхимического периода.
которого дошло до наших дней, являлся Болос Демокритос из Менде, известный ещё как Псевдо-Демокрит (около 200 до н.э.). Написанная Болосом книга "Физика и мистика" состоит из четырёх частей, посвящённых золоту, серебру, драгоценным камням и пурпуру. У Болоса впервые сформулирована идея трансмутации металлов – превращения одного металла в другой, прежде всего неблагородных металлов (свинца или железа) в золото, ставшая основной задачей всего алхимического периода.
Следует отметить, что возможность трансмутации обосновывалась алхимиками на основе теории четырёх элементов-стихий. Сами элементы, сочетанием которых образованы все вещества, способны превращаться друг в друга. Поэтому превращение одного металла, составленного из этих элементов, в другой металл, составленный их тех же элементов в другом сочетании, считалось лишь вопросом метода (искусства). Практической предпосылкой возникновения идеи трансмутации могло быть известное с древности резкое изменение окраски и свойств металла при введении некоторых добавок (например, цвет известной с IV тысячелетия до н.э. мышьяковистой меди варьируется от белого до красноватых и золотистых оттенков).
Осуществление трансмутации металлов и составило основную задачу алхимии на протяжении всего её существования. Первые описания способов изготовления сплавов, подобных благородным металлам, имеются уже в работе Болоса; в частности, там описывается приготовление латуни – жёлтого сплава меди с цинком, каковой сплав, по мнению Болоса, являлся золотом.
Ещё одно дошедшее до нашего времени сочинение александрийского периода – энциклопедия, которую около 300 г. написал Зосим Панополит. В этой книге, представляющей собой производственные рецептуры, обильно сдобренные мистикой, им сведены все знания по khemeia, собранные за предыдущие пять или шесть веков. Зосим определял khemeia как искусство делания золота и серебра, причём особо указывал на запрет разглашения тайн этого искусства.
Помимо упомянутых собраний рецептур, от александрийского периода осталось также и множество герметических текстов, представляющих собой попытку философско-мистического объяснения превращений веществ, к числу которых относится и знаменитая "Изумрудная скрижаль" ("Tabula smaragdina") Гермеса Трисмегиста.
В целом следует отметить, что об александрийском этапе алхимии известно очень мало. Причиной этого является, прежде всего, практически полное уничтожение Александрийской библиотеки. Помимо этого, римский император Диоклетиан (243-315), дабы исключить возможность получения дешёвого золота, что подорвало бы и без того шаткую экономику разваливающейся империи, запретил занятия химией и приказал уничтожить все труды по khemeia.
Утверждение христианства в качестве государственной религии Римской империи при императоре Константине (285-337) привело к ещё большим гонениям на алхимию, пронизанную языческой мистикой и в силу этого, безусловно, являющуюся ересью. Поскольку средоточением естествознания и античной философии являлась Александрийская академия, она неоднократно подвергались разгромам фанатиками-христианами. В 385-415 годах были разрушены многие здания Александрийской академии, в том числе и храм Сераписа. В 529 году римский папа Григорий I запретил чтение древних книг и занятие математикой и философией; христианская Европа погрузилась во мрак раннего средневековья. Формально Александрийская академия прекратила свое существование после завоевания Египта арабами в 640 году. Однако научные и культурные традиции греческой школы на Востоке сохранялись какое-то время в Византийской империи, а затем они были восприняты арабским миром.
Арабская алхимия
В VII веке началось победоносное шествие новой мировой религии – ислама – что привело к созданию огромного Халифата, включившего в себя Малую и Среднюю Азию, Северную Африку (включая, разумеется, и Египет) и юг Пиренейского полуострова в Европе. Арабские халифы, подражая Александру Македонскому, покровительствовали наукам. На Ближнем Востоке – в Дамаске, Багдаде, Кордове, Каире – были созданы университеты, на несколько столетий ставшие главными научными центрами и давшие человечеству целую плеяду выдающихся учёных. Слово khemeia преобразовалось в арабском языке в al-khimiya, давшее название описываемому этапу. Влияние ислама в арабских университетах было сравнительно слабым; кроме того, изучение трудов античных авторов не противоречило трём обязательным исламским догматам – вере в Аллаха, в его пророков и загробный суд. Благодаря этому на Арабском Востоке могли свободно развиваться научные представления, в основе которых лежало научное наследие античности, в том числе и александрийская khemeia.
Теоретической основой арабской алхимии стало учение Аристотеля и его идея о взаимопревращаемости элементов. Однако для интерпретации опытных данных, касающихся свойств металлов, теория Аристотеля оказалась не слишком удобной, поскольку описывала, прежде всего, физические свойства вещества. Арабский алхимик Айюб ал Рухави (769-835) давал следующее весьма громоздкое и туманное объяснение свойств металлов, основанное на аристотелевом учении: "Золото содержит больше влажности, чем серебро, поэтому оно более ковко. Золото жёлтое, а серебро белое, т.к. первое содержит больше тепла, а второе – больше холода. Медь суше, чем серебро или золото, и её цвет более красен, т.к. она теплее. Олово более влажно, чем серебро или золото, так же обстоит дело и со свинцом. Это объясняет, почему они так легко плавятся на огне. Больше всего влажности в ртути, поэтому она, подобно воде, испаряется на огне. Что касается железа, то оно землистее и суше, чем все остальные, … и оно с трудом поддаётся действию огня и не плавится, подобно другим, если только плавящая сила не приведена в тесное соприкосновение с ним". Развитие алхимической практики потребовало создания новой теории, основанной на химических свойствах веществ.
Абу Муса Джабир ибн Хайан (721-815), в европейской литературе известный под именем Гебер, разработал ртутно-серную теорию происхождения металлов, которая составила теоретическую основу алхимии на несколько последующих столетий. Джабир ибн Хайан создал теорию, призванную более конкретно объяснять свойства металлов (в частности, такие, как блеск, ковкость, горючесть) и обосновывать возможность трансмутации. Следует особо отметить, что ртутно-серная теория представляла собой попытку теоретического обобщения опытных данных в достаточно частном вопросе, не претендуя на всеобщность объяснения. Это в корне отличает её от классических натурфилософских учений. Суть ртутно-серной теории состоит в следующем.
В основе всех металлов лежат два принципа – Ртуть (философская Ртуть) и Сера (философская Сера). Ртуть является принципом металличности, Сера – принципом горючести. Принципы новой теории, таким образом, выступают как носители определённых свойств металлов, установленных в результате экспериментального изучения действия высоких температур на металлы. Важно отметить, что на протяжении многих веков принималось, будто действие высоких температур (метод огня) есть наилучший метод для упрощения состава тела. Следует подчеркнуть, что философская Ртуть и философская Сера не тождественны ртути и сере как конкретным веществам. Обычные ртуть и сера представляют собой своего рода свидетельства существования философских Ртути и Серы как принципов, причём принципов, скорее духовных, нежели материальных. Металл ртуть, по мнению Джабира ибн Хайана, представляет собой почти чистый принцип металличности (философская Ртуть), содержащий, тем не менее, некоторое количество принципа горючести (философской Серы).
Согласно учению Джабира, сухие испарения, конденсируясь в недрах Земли, дают Серу, мокрые – Ртуть. Затем под действием теплоты два принципа соединяются, образуя семь известных металлов – золото, серебро, ртуть, свинец, медь, олово и железо. Золото – совершенный металл – образуется, только если вполне чистые Сера и Ртуть взяты в наиболее благоприятных соотношениях. В земле, согласно Джабиру, образование золота и других металлов происходит постепенно и медленно; "созревание" золота можно ускорить с помощью некоего "медикамента" или "эликсира" (al-iksir, от греческого ξεριον, т.е. "сухой"), который приводит к изменению соотношения Ртути и Серы в металлах и к превращению последних в золото и серебро. Поскольку плотность золота больше плотности ртути, считалось, что эликсир должен быть очень плотной субстанцией. Позднее в Европе эликсир получил название "философский камень" (Lapis Philosophorum).

Проблема трансмутации, таким образом, в рамках ртутно-серной теории сводилась к задаче выделения эликсира, обозначаемого алхимиками астрологическим символом Земли.
По мнению алхимиков, процесс превращения "несовершенных металлов" в "совершенный металл" – золото – может быть отождествлён с "излечением" металлов. Поэтому эликсир, согласно представлениям последователей Гебера, должен был обладать ещё многими магическими свойствами – исцелять все болезни, и, возможно, давать бессмертие. Именно эти "побочные функции" эликсира и закрепились в современном значении этого слова в русском языке. Вообще следует отметить, что арабская алхимия всегда самым тесным образом была связана с медициной, которая в арабском мире была развита весьма высоко (в частности, в Багдаде ещё в VIII веке появилась первая государственная аптека), и практически все арабские алхимики были известны ещё и как врачи.
Среди арабских учёных выделяется знаменитый бухарский врач Абу Али аль Хусейн ибн Абдаллах ибн Сина, или Авиценна (980-1037), явившийся первым критиком идеи трансмутации металлов, каковую он считал невозможной, и считавший основной задачей алхимии приготовление лекарственных средств.
Абу Бакр Мухаммед ибн Закарийа Ар-Рази (864-925), в европейской литературе известный как Разес, внёс в ртутно-серную теорию некоторые изменения. Поскольку свойства таких веществ, как соли металлов, довольно сложно объяснить с использованием двух принципов, Ар-Рази добавил к ним третий принцип, принцип растворимости (хрупкости) – философскую Соль. Ртуть и Сера, по его мнению, образуют твёрдые вещества лишь в присутствии этого третьего принципа. В таком виде теория трёх принципов приобрела логическую завершённость и просуществовала в неизменном виде несколько веков.
Ар-Рази предпринял также попытку объединить учение Аристотеля – главную теоретическую основу алхимии – с атомистической идеей. Четыре стихии Аристотеля, по мнению Ар-Рази, это четыре вида атомов, движущихся в пустоте и различающихся формой и размером. Среди многочисленных заслуг Ар-Рази следует также отметить предложенную им классификацию веществ на три царства – минеральные, растительные и животные. Ар-Рази в своих сочинениях подробнейшим образом описывал химическую посуду, оборудование, весы и лабораторные приёмы. Вообще для арабских алхимиков было характерно тщательное отношение к описанию эксперимента; весы и лабораторная техника уже к XI веку достигли высокой степени совершенства. В частности, Абу-ар-Райхан Мухаммед ибн Ахмед Аль-Бируни и Абд ар-Рахман Ал Хазини приводили в своих трудах величины плотностей металлов, отличающиеся от современных значений менее чем на один процент.
В целом именно во время арабского этапа были созданы основные теории алхимии, разработан понятийный аппарат, лабораторная техника и методика эксперимента. Арабские алхимики добились несомненных практических успехов – ими выделены сурьма, мышьяк и, по-видимому, фосфор, получены уксусная кислота и растворы сильных минеральных кислот. Арабская алхимия, в отличие от александрийской, была вполне рациональна; мистические элементы в ней представляли собой скорее дань традиции. Важнейшей заслугой арабских алхимиков стало создание рациональной фармации, развившей традиции античной медицины.
После XII века по ряду причин (как внутренних, так и внешних) арабская алхимия начала приходить в упадок. Последним крупным арабским алхимиком стал Ал Джилдаки (первая половина XIV века), написавший ряд сочинений, очень полно суммирующих труды его предшественников. Центр научной мысли переместился в Европу.
Европейская алхимия
Европейские государства, прежде всего страны южной Европы, достаточно тесно контактировали с Византией и арабским миром, особенно после начала крестовых походов (1-й начался в 1096 году). Европейцы получили возможность ознакомиться и с блестящими достижениями арабской цивилизации, и с наследием античности, сохранившимся благодаря арабам. В XII веке начались попытки перевода на латинский язык арабских трактатов и сочинений античных авторов. Тогда же в Европе были созданы первые светские учебные заведения – университеты: в Болонье (1119), Монпелье (1189), Париже (1200). Начиная с XIII века, можно говорить о европейской алхимии как об особом этапе алхимического периода.
Следует отметить, что между арабской и европейской алхимией имели место весьма существенные отличия. Европейская алхимия развивалась в обществе, где христианская (католическая) церковь активно вмешивалась во все светские дела; изложение идей, противоречащих христианским догматам, было делом весьма небезопасным. Алхимия в Европе с момента своего зарождения находилась на полуподпольном положении; в 1317 году папа Иоанн XXII предал алхимию анафеме, после чего всякий алхимик в любой момент мог быть объявлен еретиком со всеми вытекающими последствиями. Однако европейские властители, как светские, так и церковные, объявив алхимию вне закона, в то же время покровительствовали ей, рассчитывая на выгоды, которые сулило нахождение способа получения золота. Вследствие этого европейская алхимия, как и александрийская, изначально являлась герметической наукой, доступной только посвящённым. Этим объясняется характерное для европейской алхимии чрезвычайно туманное изложение достигнутых результатов. Впрочем, в течение довольно долгого времени европейские сочинения по алхимии представляли собой лишь переводы либо компиляцию арабских трактатов.
 |
| Крылатый из бескрылый драконы - аллегория Ртути и Серы |
Первым знаменитым европейским алхимиком стал монах-доминиканец Альберт фон Больштедт (1193-1280), более известный как Albertus Magnus (Альберт Великий). Труды Альберта Великого ("Книга об Алхимии" и пр.) сыграли важную роль в том, что натурфилософия Аристотеля стала наиболее значимой для европейских учёных позднего средневековья и начала Нового Времени. Альберт Великий первым из европейских алхимиков детально описал свойства мышьяка, почему ему иногда приписывают открытие этого вещества. Альберт Великий высказывал даже мнение о том, что металлы состоят из ртути, серы, мышьяка и нашатыря.
Современником Альберта Великого был английский монах-францисканец Роджер Бэкон (1214-1292), написавший, в частности, знаменитейший трактат "Зеркало Алхимии". В трактате даётся подробное описание природы металлов с точки зрения ртутно-серной теории. Роджер Бэкон определял алхимию следующим образом: "Алхимия есть наука, указывающая, как приготовлять и получать некоторое средство, эликсир, которое, брошенное на металл или несовершенное вещество, делает их совершенными в момент прикосновения". По мнению Бэкона и последователей, приготовление эликсира из "первичной субстанции" должно было осуществиться в три стадии – нигредо (чёрная стадия), альбедо (белая, в результате которой получается малый эликсир, способный превращать металлы в серебро) и рубедо (красная, продуктом которой и является великий эликсир – магистерий).
Роджер Бэкон подразделял алхимию на умозрительную (теоретическую), которая исследует состав и происхождение металлов и минералов, и практическую, занимающуюся вопросами добывания и очистки металлов, приготовления красок и т.п. Бэкон был одним из первых, кто привёл описание чёрного пороха, и иногда считается его изобретателем. Необходимо отметить, что появление огнестрельного оружия стало сильнейшим стимулом для развития алхимии и её тесного переплетения с ремесленной химией.
В работах Альберта Великого и Роджера Бэкона, как и в сочинениях арабских алхимиков, доля мистицизма была сравнительно невелика. В то же время для европейской алхимии в целом мистические элементы значительно более характерны, нежели для арабской. К основоположникам мистических течений часто относят испанского врача Арнальдо де Виллановы (1240-1313) и Раймунда Луллия (1235-1313). Их труды также были посвящены трансмутации (Луллий даже утверждал, будто ему удавалось получать философский камень и золото), причём особый упор делался на магических операциях, необходимых для получения желаемых результатов.
Мистические течения в европейской алхимии занимали очень значительное место. Алхимики-мистики сформулировали дополнительные задачи своей науки; общее число задач было равно, естественно, семи:
1. Приготовление Эликсира или Философского Камня (Lapis Philosoiphorum);
2. Создание гомункулуса;
3. Приготовление алкагеста – универсального растворителя;
4. Палигенез, или восстановление растений из пепла;
5. Приготовление мирового духа (spiritus mundi) – магической субстанции, одно из свойств которой – способность растворять золото.
6. Извлечение квинтэссенции.
7. Приготовление жидкого золота (aurum potabile), совершеннейшего средства для излечения.
Достижению поставленных целей должны были послужить двенадцать основных алхимических операций, каждая из которых соотносилась с определённым зодиакальным созвездием. Именно по мистическим соображениям мышьяк и сурьму алхимики отказывались признавать самостоятельными металлами, т.к. для них не хватает планет, которых, по тогдашним представлениям, всего семь; мистическая связь алхимии и астрологии имела для алхимиков большее значение, чем факты. Мистицизм и закрытость европейской алхимии породили, естественно, значительное число мошенников от алхимии.
Тем не менее, в XIV-XV веках европейская алхимия добилась значительных успехов, сумев превзойти арабов в постижении свойств вещества. В 1270 году итальянский алхимик кардинал Джованни Фиданца (1121-1274), известный как Бонавентура, в одной из попыток получения универсального растворителя получил раствор нашатыря в азотной кислоте (aqua fortis), который оказался способным растворять золото, царя металлов (отсюда и название – aqua Regis, т.е. царская водка). Имя самого значительного из средневековых европейских алхимиков, работавшего в Испании в XIV веке, осталось неизвестным – он подписывал свои сочинения именем Гебера. Псевдо-Гебер первым подробно описал сильные минеральные кислоты – серную и азотную. Использование в концентрированных минеральных кислот в алхимической практике привело существенному росту знаний алхимиков о веществе.
Многие сведения о различных веществах приводятся в сочинениях знаменитого алхимика XV века Василия Валентина: подробно описывается сурьма, соединения цинка, висмута, олова, свинца, кобальта, способы получения и свойства соляной кислоты и винного спирта и т.д.
 |
| Открытие фосфора Х.Брандом (картина Дж.Райта) |
Кроме легендарного Василия Валентина, в XV-XVII веках в Западной Европе широкой известностью – либо благодаря своим мнимым успехам в получении философского камня, либо благодаря своим сочинениям, – пользовались многие алхимики: Николас Фламель, Александр Сетоний, Иоганн Исаак Голланд, Михаил Седзивой, Венцель Зейлер и многие другие. Алхимические идеи были чрезвычайно популярны в обществе; вера в чудодейственные свойства философского камня, казалось, была незыблемой. Однако к середине XVI века в европейской алхимии стало очевидным быстро прогрессирующее разделение. С одной стороны – вырождающееся мистическое направление, представители которого по-прежнему пытались осуществить трансмутацию металлов с помощью магии, с другой – набирающие силу рациональные течения. Наиболее значительными из последних являлись иатрохимия и техническая химия, ставшие своего рода переходным этапом от классической алхимии к новой научной химии.
Алхимии изначально были присущи весьма серьёзные отрицательные черты, которые, в конце концов, и сделали её тупиковой ветвью развития естествознания. Во-первых, это ограниченность предмета лишь трансмутацией металлов; все алхимические операции с веществом были подчинены этой главной цели. Во-вторых – мистицизм, в большей или меньшей степени присущий всем алхимикам. В-третьих, это догматизм теории – учение Аристотеля, лежащее в основе идеи трансмутации, принималось за истину в последней инстанции без каких-либо обоснований. Наконец, изначально характерная для алхимии закрытость являлась существенным препятствием для развития этой науки. Тем не менее, уязвимость алхимии для критики с точки зрения современной науки никоим образом не означает, что труд многих поколений алхимиков был бессмысленным и бесполезным.
Главным результатом алхимического периода, помимо накопления значительного запаса знаний о веществе, стало становление эмпирического (опытного) подхода к изучению свойств вещества. Алхимиками была разработана ртутно-серная теория (теория трёх принципов), призванная обобщить опытные данные. В целом алхимический период явился совершенно необходимым переходным этапом между натурфилософией и экспериментальным естествознанием.
Иатрохимия и техническая химия
Совершенно новое понимание задач алхимии было изложено в трудах основоположников технической химии Ваноччо Бирингуччо (1480-1539) "О пиротехнии" и Георга Бауэра (1494-1555), более известного как Агрикола, "De Re Metallica". Сочинения этих авторов представляли собой своего рода энциклопедии, посвящённые минералогии, металлургии, горному делу, производству керамики, т.е. технологическим процессам, предполагающим химические операции с веществами. Характерной особенностью трудов представителей технической химии стало стремление к максимально ясному, полному и достоверному описанию опытных данных и технологических процессов. Именно в поисках способов совершенствования химической технологии Бирингуччо и Агрикола видели задачу алхимии.
Немецкий врач и алхимик Филипп Ауреол Теофраст Бомбаст фон Гогенгейм, вошедший в историю под псевдонимом Парацельс (1493-1541) стал основоположником другого рационального направления в алхимии – иатрохимии (от греческого ιατροσ – врач). В теоретическом отношении Парацельс являлся классическим алхимиком – он разделял древнегреческое учение о четырёх элементах-стихиях и арабскую теорию трёх принципов. Парацельс не был чужд мистике – он занимался поисками эликсира жизни и даже утверждал, будто нашёл его; в его сочинениях можно найти подробный рецепт приготовления гомункулуса. Однако, подобно Авиценне, Парацельс негативно относился к идее трансмутации металлов (не отрицая, впрочем, принципиальной возможности трансмутации). Парацельс утверждал, что задача алхимии – изготовление лекарств: "Химия – один из столпов, на которые должна опираться врачебная наука. Задача химии вовсе не в том, чтобы делать золото и серебро, а в том, чтобы готовить лекарства". Медицина Парацельса основывалась на ртутно-серной теории. Он считал, что в здоровом организме три принципа – Ртуть, Сера и Соль – находятся в равновесии; болезнь представляет нарушение равновесия между принципами. Для восстановления равновесия Парацельс использовал в медицинской практике многие лекарственные препараты минерального происхождения – соединения мышьяка, сурьмы, свинца, ртути и т.п. – в дополнение к традиционным растительным препаратам.
Вследствие резко усилившихся миграций людей, способствующих распространению инфекционных заболеваний (что усугублялось царящей в средневековой Европе тотальной антисанитарией), борьба с эпидемиями приобрела во времена Парацельса чрезвычайное значение. Благодаря несомненным успехам, достигнутым Парацельсом в медицине, его взгляды завоевали широкое признание. К представителям иатрохимии (спагирикам, как называли себя последователи Парацельса) можно отнести многих известных алхимиков XVI - XVII веков.
Андреас Либавий (1540-1616) прославился первым в истории учебником химии – "Алхимия", – вышедшим в 1597 году. Соглашаясь с Парацельсом в том, что главная задача алхимии состоит в служении медицине, Либавий яростно критиковал туманно-мистические элементы в учении Парацельса. Тем не менее, он считал, что трансмутация возможна, и её осуществление явится венцом науки. Другой видный представитель иатрохимии – итальянский врач Анджело Сала – напротив, отрицал возможность трансмутации металлов: "...ибо то, что не золото, ни я и никто другой не сможет никогда превратить в золото".
Важную роль в развитии рациональной алхимии сыграл Иоганн Рудольф Глаубер (1604-1670), разработавший способы получения целого ряда неорганических веществ. Другой известный алхимик Отто Тахений (1620-1699) попытался внести изменения в ртутно-серную теорию, утверждая, что все соли образованы двумя принципами – кислотой и щёлочью. Ещё один представитель иатрохимии Ян Баптист ван Гельмонт (1577-1664) был одним из первых учёных, поставивших вопрос об истинных простых составных частях сложных тел. Подвергая сомнению аристотелевские стихии и принципы алхимиков на том основании, что их присутствие невозможно обнаружить в составе большинства тел, Ван Гельмонт предлагал считать простыми телами лишь те, которые могут быть выделены при разложении сложных тел. Так, поскольку при разложении растительных и животных веществ всегда выделялась вода, Ван Гельмонт считал её простым телом и главной составной частью сложных тел. В поисках других простых тел Ван Гельмонт много экспериментировал с металлами. Он доказал, что при растворении серебра в крепкой водке (азотной кислоте) металл лишь меняет форму своего существования и может быть вновь выделен из раствора в том же количестве. Этот опыт интересен и как один из первых примеров количественного исследования явления.
В целом рациональные течения в алхимии – иатрохимия и техническая химия – достигли довольно значительных экспериментальных успехов и заложили основы для научной химии, становление которой начинается в середине XVII века. Не следует, однако, считать, что появление научной химии автоматически означало конец "классической" алхимии. Алхимические традиции сохранялись в науке ещё долгое время, и многие выдающиеся естествоиспытатели продолжали считать трансмутацию металлов возможной.
3. ПЕРИОД СТАНОВЛЕНИЯ
Экспериментальное естествознание XVII века - Р.Бойль и возникновение научной химии - Теория флогистона - Кислородная теория горения - Химическая революция
Экспериментальное естествознание XVII века
В XV-XVI веках в Европе начался период быстрого роста торговли и материального производства. К XVI веку техника в Европе вышла на уровень заметно более высокий, чем в период расцвета Античного мира. При этом изменения в технических приемах опережали их теоретическое осмысление. Технические изобретения XVI века и блестящие успехи мореплавания (разрешившие, кстати, длившийся столетиями финансовый кризис, связанный с нехваткой драгоценных металлов) одновременно ставили перед наукой новые проблемы, которые существовавшая ранее наука разрешить не могла. Дальнейшее усовершенствование техники упиралось в главное противоречие эпохи – противоречие между сравнительно высоким уровнем достигнутых к этому времени технологических знаний и резким отставанием теоретического естествознания.
Развитие философии и естествознания в эпоху Возрождения привело к глубокому кризису аристотелевской картины мира и поставило задачу выработки отражающей реальные свойства действительности физической концепции, а потребности технического прогресса привели к созданию основ научного эксперимента. Быстрому развитию в Европе новых философских систем способствовала также и Реформация, начавшаяся в XVI веке.
Сочетание социально-экономических и технических факторов вызвало сдвиг в общественном сознании, усилило потребность в выработке новой философии, отрицавшей роль авторитета (как религиозных доктрин, так и античных учений) и утверждавшей приоритет научного доказательства. В начале XVII века появились крупные философские произведения, оказавшие существенное влияние на развитие естествознания. Английский философ Френсис Бэкон выдвинул тезис о том, что решающим доводом в научной дискуссии должен являться эксперимент. Вместо принятого с античных времён дедуктивного метода Бэкон предложил новую логику науки – индукцию, основанную на умозаключении от частного к общему (весьма символичными являются названия сочинений Бэкона – "Новый органон" (1620) и "Новая Атлантида", прямо противопоставляемые "Органону" и "Атлантиде" Аристотеля).
Семнадцатый век в философии ознаменовался также возрождением атомистических представлений. Математик (основатель аналитической геометрии) и философ Рене Декарт, известный также как Картезий, утверждал, что все тела состоят из корпускул различной формы и размеров; форма корпускул связана со свойствами вещества. В то же время Декарт считал, что корпускулы делимы и состоят из единой материи. Декарт отрицал представления Демокрита о неделимых атомах, движущихся в пустоте, не решаясь допустить существование пустоты. Корпускулярные идеи, весьма близкие к античным представлениям Эпикура, высказывал и французский философ Пьер Гассенди. Группы атомов, образующие соединения, Гассенди называл молекулами (от латинского moles – кучка). Корпускулярные представления Гассенди завоевали довольно широкое признание среди естествоиспытателей.
Инструментом разрешения противоречия между высоким уровнем технологии и крайне низким уровнем знаний о природе стало в XVII веке новое экспериментальное естествознание.
Огромные успехи в XVII веке были достигнуты в области физики, механики, математики и астрономии. Галилео Галилей не только основал классическую механику, но и ввёл в физику новый образ мышления, в полной мере использующий экспериментальный метод. Немецкий астроном Иоганн Кеплер в 1609 году привёл в соответствие с астрономическими данными гелиоцентрическую систему, которую предложил в 1543 году Николай Коперник, и которая в первоначальном виде содержала множество неточностей. Эванджелиста Торричелли, Блез Паскаль и Отто фон Герике провели в середине XVII века свои знаменитые опыты по изучению вакуума и атмосферного давления. Герике начал также исследования в области электростатики; Христиан Гюйгенс создал волновую теорию света и разработал основные законы оптики. Исаак Ньютон открыл законы классической механики и закон всемирного тяготения. Его капитальный труд "Математические начала натуральной философии" (1687) обобщил не только собственные исследования автора, но и опыт предшественников, результатом чего явилось создание единой механической картины мира, господствовавшей вплоть до рубежа XIX и XX столетий. Все эти и многие другие блестящие открытия ознаменовали собой первую научную революцию, результатом которой стало становление нового естествознания, целиком основанного на экспериментальных данных. Основой естествознания становится принцип количественного измерения в экспериментальных исследованиях. Это находит свое выражение в изобретении разнообразных измерительных приборов – хронометров, термометров, ареометров, барометров, весов и т.д.
Новое естествознание породило и новые организационные формы – были созданы научные общества и академии наук. Ещё в 1560 году итальянский естествоиспытатель Джиованни Баттиста Делла Порта начал проводить в своём доме регулярные собрания, называемые Академией тайн природы. В XVII веке появились официально учреждённые академии с соответствующими органами и статутом: Академия естествоиспытателей (Леопольдина) в Германии (1652), Академия опыта во Флоренции (1657), Королевское общество (1662) в Лондоне, Парижская Академия точных наук (1663).
Одним из следствий произошедшей во второй половине XVII века научной революции явилось создание новой – научной – химии. Создателем научной химии традиционно считается Роберт Бойль.
Роберт Бойль и возникновение научной химии
Британский учёный Роберт Бойль являлся одним из крупнейших химиков, физиков и философов своего времени. В качестве основных научных достижений Бойля в химии можно отметить основание им аналитической химии (качественный анализ), исследования свойств кислот, введение в химическую практику индикаторов, изучение плотностей жидкостей с помощью изобретённого им ареометра. Нельзя не упомянуть и открытый Бойлем закон, носящий его имя (называемый также законом Бойля-Мариотта). Однако главной заслугой Бойля стала предложенная им новая система химической философии, изложенная в книге "Химик-скептик" (1661). Книга была посвящена поискам ответа на вопрос, что именно следует считать элементами, исходя из современного уровня развития химии. Бойль писал: "Химики до сих пор руководствовались чересчур узкими принципами, не требовавшими особенно широкого умственного кругозора; они видели свою задачу в приготовлении лекарств, в получении и превращении металлов. Я смотрю на химию с совершенно иной точки зрения: не как врач, не как алхимик, а как должен смотреть на неё философ. Я начертал здесь план химической философии, который надеюсь выполнить и усовершенствовать своими опытами и наблюдениями". Книга построена в форме беседы между четырьмя философами: Фемистом, перипатетиком (последователем Аристотеля), Филопоном, спагириком (сторонником Парацельса), Карнеадом, излагающим взгляды "мистера Бойля", и Элевтерием, беспристрастно оценивающим аргументы спорщиков. Дискуссия философов подводила читателя к выводу, что ни четыре стихии Аристотеля, ни три принципа алхимиков не могут быть признаны в качестве элементов. Бойль подчёркивал: "Нет никаких оснований присваивать данному телу название того или иного элемента только потому, что оно похоже на него одним каким-либо легко заметным свойством; ведь с тем же правом я мог бы отказать ему в этом названии, поскольку другие свойства являются разными". Исходя из опытных данных, Бойль показал, что понятия современной химии должны быть пересмотрены и приведены в соответствие с экспериментом.
Элементы, согласно Бойлю – практически неразложимые тела (вещества), состоящие из сходных однородных (состоящих из первоматерии) корпускул, из которых составлены все сложные тела и на которые они могут быть разложены. Корпускулы могут различаться формой, размером, массой. Корпускулы, из которых образованы тела, остаются неизменными при превращениях последних.
Главную задачу химии Бойль видел в изучении состава веществ и зависимости свойств вещества от его состава. При этом понятие состава Бойль считал возможным употреблять только тогда, когда из элементов, выделенных из данного сложного тела, можно обратно восстановить исходное тело (т.е. он фактически принимал синтез за критерий правильности анализа). Бойль в своих трудах не назвал ни одного элемента в новом понимании этого понятия; не указал он и число элементов, отмечая лишь, что "не будет абсурдом, если предположить, что число это много больше трёх или четырёх". Таким образом, книга "Химик-скептик" представляет собой не ответ на насущные вопросы химической философии, но постановку новой цели химии. Главное значение работы Бойля заключается в следующем:
1. Формулировка новой цели химии – изучения состава веществ и зависимости свойств вещества от его состава.
2. Предложение программы поиска и изучения реальных химических элементов;
3. Введение в химию индуктивного метода;
Представления Бойля об элементе как о практически неразложимом веществе (следует отметить, что тождество терминов "элемент" и "простое вещество" сохранялось до середины XIX века) быстро получили широкое признание среди естествоиспытателей. Однако создание теоретических представлений о составе тел, способных заменить учение Аристотеля и ртутно-серную теорию, оказалось очень сложной задачей. В последней четверти XVII века появились т.н. эклектические воззрения, создатели которых пытались увязать алхимические традиции и новые представления о химических элементах. Большое влияние на современников оказали взгляды французского химика Николя Лемери, автора широко известного учебника "Курс химии".
Учебник Лемери начинался с определения предмета химии: "Химия есть искусство, учащее, как разделять различные вещества, содержащиеся в смешанных телах. Я понимаю под смешанными телами те, которые образуются в природе, а именно: минералы, растительные и животные тела". Далее Лемери перечислял "химические начала", т. е. основные составные части тел. После некоего "универсального духа" (который сам автор признаёт "несколько метафизичным"), Лемери на основании анализа посредством огня выделял пять основных материальных начал веществ: спирт (иначе "ртуть"), масло (иначе "сера"), соль, вода ("флегма") и земля. Первые три начала – активные, вода и земля – пассивные.
Лемери, однако, отмечал, что эти субстанции являются для нас "началами" лишь постольку, поскольку химики не смогли далее разложить эти тела; очевидно, эти "начала" могут быть в свою очередь разделены на более простые. Таким образом, то, что принимается в качестве начал, – это субстанции, полученные в результате разделения смешанных тел и отделённые лишь настолько, насколько позволяют это сделать средства, которыми располагают химики.
На рубеже XVII-XVIII веков научная химия находилась лишь в самом начале своего пути; важнейшими препятствиями, которые лишь предстояло преодолеть, являлись сильные ещё алхимические традиции (ни Бойль, ни Лемери не отрицали принципиальную возможность трансмутации), ложные представления об обжиге металлов как о разложении и спекулятивный (умозрительный) характер атомизма.
Теория флогистона
Первая теория научной химии – теория флогистона – в значительной степени основывалась на традиционных представлениях о составе веществ и об элементах как носителях определённых свойств. Тем не менее, именно она стала в XVIII веке главным условием и основной движущей силой развития учения об элементах и способствовала полному освобождению химии от алхимии. Именно во время почти столетнего существования флогистонной теории завершилось начатое Бойлем превращение алхимии в химию.
Флогистонная теория горения была создана для описания процессов обжига металлов, изучение которых являлось одной из важнейших задач химии конца XVIII века. Металлургия в это время столкнулась с двумя проблемами, разрешение которых было невозможно без проведения серьёзных научных исследований – большие потери при выплавке металлов и топливный кризис, вызванный почти полным уничтожением лесов в Европе.
Основой для теории флогистона послужили традиционные представления о горении как о разложении тела. Феноменологическая картина обжига металлов была хорошо известна: металл превращается в окалину, масса которой больше массы исходного металла (Бирингуччо ещё в 1540 г. показал, что вес свинца увеличивается после прокаливания); кроме того, при горении имеет место выделение газообразных продуктов неизвестной природы. Целью химической теории стало рациональное объяснение этого феномена, которое можно было бы использовать для решения конкретных технических задач. Последнему условию не отвечали ни представления Аристотеля, ни алхимические взгляды на горение.
Создателями теории флогистона считаются немецкие химики Иоганн Иоахим Бехер и Георг Эрнст Шталь. Бехер в книге "Подземная физика" (1669) изложил свои очень эклектичные взгляды на составные части тел. Таковыми, по его мнению, являются три вида земли: первая – плавкая и каменистая (terra lapidea), вторая – жирная и горючая (terra pinguis) и третья – летучая (terra fluida s. mercurialis). Горючесть тел, по мнению Бехера, обусловлена наличием в их составе второй, жирной, земли. Система Бехера очень похожа на алхимическое учение о трёх принципах, в котором горючесть обусловлена наличием серы; однако Бехер считает, что сера является сложным телом, образованным кислотой и terra pinguis. По сути, теория Бехера представляла собой одну из первых попыток предложить нечто новое взамен алхимического учения о трёх принципах. Увеличение массы металла при обжиге Бехер традиционно объяснял присоединением "огненной материи". Эти взгляды Бехера послужили предпосылкой к созданию теории флогистона, предложенной Шталем в 1703 году, хотя и имеют с ней очень мало общего. Тем не менее, сам Шталь всегда утверждал, что авторство теории принадлежит Бехеру.
Суть теории флогистона можно изложить в следующих основных положениях:
1. Существует материальная субстанция, содержащаяся во всех горючих телах – флогистон (от греческого φλογιστοζ – горючий).
2. Горение представляет собой разложение тела с выделением флогистона, который необратимо рассеивается в воздухе. Вихреобразные движения флогистона, выделяющегося из горящего тела, и представляют собой видимый огонь. Извлекать флогистон из воздуха способны лишь растения.
3. Флогистон всегда находится в сочетании с другими веществами и не может быть выделен в чистом виде; наиболее богаты флогистоном вещества, сгорающие без остатка.
4. Флогистон обладает отрицательной массой.
Теория Шталя, подобно всем предшествующим, также исходила из представлений, будто свойства вещества определяются наличием в них особого носителя этих свойств. Положение флогистонной теории об отрицательной массе флогистона (значительно более позднее и признававшееся не всеми сторонниками теории) было призвано объяснить тот факт, что масса окалины (или всех продуктов горения, включая газообразные) больше массы обожжённого металла.
Процесс обжига металла в рамках теории флогистона можно отобразить следующим подобием химического уравнения:
Металл = Окалина + Флогистон
Для получения металла из окалины (или из руды), согласно теории, можно использовать любое тело, богатое флогистоном (т.е. сгорающее без остатка) – древесный или каменный уголь, жир, растительное масло и т.п.:
Окалина + Тело, богатое флогистоном = Металл
Необходимо подчеркнуть, что эксперимент может только подтвердить справедливость этого предположения; это являлось хорошим аргументом в пользу теории Шталя. Флогистонная теория со временем была распространена на любые процессы горения. Тождество флогистона во всех горючих телах было обосновано Шталем экспериментально: уголь одинаково восстанавливает и серную кислоту в серу, и земли в металлы. Дыхание и ржавление железа, по мнению последователей Шталя, представляют собой тот же процесс разложения содержащих флогистон тел, но протекающий медленнее, чем горение.
Теория флогистона позволила, в частности, дать приемлемое объяснение процессам выплавки металлов из руды, состоящее в следующем. Руда, содержание флогистона в которой мало, нагревается с древесным углем, который очень богат флогистоном; флогистон при этом переходит из угля в руду, и образуются богатый флогистоном металл и бедная флогистоном зола.
Следует отметить, что в исторической литературе имеются серьёзные разногласия в оценке роли теории флогистона – от резко негативной до положительной. Однако нельзя не признать, что теория флогистона имела целый ряд несомненных достоинств:
– она просто и адекватно описывает экспериментальные факты, касающиеся процессов горения;
– теория внутренне непротиворечива, т.е. ни одно из следствий не находится в противоречии с основными положениями;
– теория флогистона целиком основана на экспериментальных фактах;
– теория флогистона обладала предсказательной способностью.
Флогистонная теория – первая истинно научная теория химии – послужила мощным стимулом для развития количественного анализа сложных тел, без которого было бы абсолютно невозможным экспериментальное подтверждение идей о химических элементах. Следует отметить, что положение об отрицательной массе флогистона фактически сделано на основании закона сохранения массы, который был открыт значительно позднее. Это предположение само по себе способствовало дальнейшей активизации количественных исследований. Ещё одним результатом создания флогистонной теории явилось активное изучение химиками газов вообще и газообразных продуктов горения в частности. К середине XVIII века одним из важнейших разделов химии стала т.н. пневматическая химия, основоположники которой Джозеф Блэк, Даниил Резерфорд, Генри Кавендиш, Джозеф Пристли и Карл Вильгельм Шееле явились создателями целой системы количественных методов в химии.
Во второй половине XVIII века теория флогистона завоевала среди химиков практически всеобщее признание. На основе флогистонных представлений сформировалась номенклатура веществ; предпринимались попытки связать такие свойства вещества, как цвет, прозрачность, щёлочность и т.п., с содержанием в нём флогистона. Французский химик Пьер Жозеф Макёр, автор весьма популярного учебника "Элементы химии" и "Химического словаря", писал в 1778 году, что флогистонная теория "…наиболее ясна и наиболее согласна с химическими явлениями. Отличаясь от систем, порождённых воображением без согласия с природой и разрушаемых опытом, теория Шталя – надёжнейший путеводитель в химических исследованиях. Многочисленные опыты… не только далеки от того, чтобы её опровергнуть, но, наоборот, становятся доказательствами в её пользу". По иронии судьбы, учебник и словарь Макёра появились в то время, когда век флогистонной теории подошёл к концу.
Кислородная теория горения
Нефлогистонные представления о горении и дыхании зародились даже несколько ранее флогистонной теории. Жан Рей, которому наука обязана постулатом "все тела тяжелы", ещё в 1630 году высказывал предположение, что увеличение массы металла при обжиге обусловлено присоединением воздуха. В 1665 году Роберт Гук (1635-1703) в работе "Микрография" также предположил наличие в воздухе особого вещества, подобного веществу, содержащемуся в связанном состоянии в селитре.
 |
| Опыт Мейоу по сжиганию тел под колоколом |
Дальнейшее развитие эти взгляды получили в книге "О селитре и воздушном спирте селитры", которую написал в 1669 году английский химик Джон Мейоу. Мейоу пытался доказать, что в воздухе содержится особый газ (spiritus nitroaëreus), поддерживающий горение и необходимый для дыхания; обосновывал он это предположение знаменитыми опытами с горящей свечой под колоколом. Однако выделить этот spiritus nitroaëreus в свободном состоянии удалось лишь более чем через сто лет. Открытие кислорода было сделано независимо друг от друга почти одновременно несколькими учёными.
Карл Вильгельм Шееле получил кислород в 1771 году, назвав его "огненным воздухом"; однако результаты опытов Шееле были опубликованы лишь в 1777 году. По мнению Шееле, "огненный воздух" представлял собой "кислую тонкую материю, соединённую с флогистоном".
Джозеф Пристли выделил кислород в 1774 году нагреванием оксида ртути. Пристли считал, что полученный им газ представляет собой воздух, абсолютно лишённый флогистона, вследствие чего в этом "дефлогистированном воздухе" горение идёт лучше, чем в обычном.
Большое значение для создания кислородной теории горения имели, кроме того, открытие водорода Кавендишем в 1766 году и азота Резерфордом в 1772 году (следует отметить, что Кавендиш принял водород за чистый флогистон).
Значение сделанного Шееле и Пристли открытия смог правильно оценить французский химик Антуан Лоран Лавуазье. В 1774 году Лавуазье опубликовал трактат "Небольшие работы по физике и химии", где высказал предположение о том, что при горении происходит присоединение к телам части атмосферного воздуха. После того, как Пристли в 1774 году посетил Париж и рассказал Лавуазье об открытии "дефлогистированного воздуха", Лавуазье повторил его опыты и в 1775 году опубликовал работу "О природе вещества, соединяющегося с металлами при их прокаливании и увеличивающего их вес" (впрочем, Лавуазье приписывал приоритет открытия кислорода себе). Наконец, в 1777 году Лавуазье сформулировал основные положения кислородной теории горения:
1. Тела горят только в "чистом воздухе".
2. "Чистый воздух" поглощается при горении, и увеличение массы сгоревшего тела равно уменьшению массы воздуха.
3. Металлы при прокаливании превращаются в "земли". Сера или фосфор, соединяясь с "чистым воздухом", превращаются в кислоты.
Примечательно, что в своей работе "О горении вообще", излагая теорию, прямо противоположную теории флогистона, Лавуазье, тем не менее, отзывался о последней следующим образом: "Различные явления обжигания металлов и горения очень удачно объясняются гипотезой Шталя,… но приходится допускать существование в горючих телах огненной материи".
Новая кислородная теория горения (термин кислород – oxygenium – появился в 1877 году в работе Лавуазье "Общее рассмотрение природы кислот и принципов их соединения") имела ряд существенных преимуществ по сравнению с флогистонной. Она более проста, чем флогистонная, не содержала в себе "противоестественных" предположений о наличии у тел отрицательной массы, и, главное, не основывалась на существовании субстанций, не выделенных экспериментально. Вследствие этого кислородная теория горения довольно быстро получила широкое признание среди естествоиспытателей (хотя полемика между Лавуазье и флогистиками длилась ещё много лет).
Химическая революция
Значение кислородной теории оказалось значительно бóльшим, чем просто объяснение явлений горения и дыхания. Отказ от теории флогистона потребовал пересмотра всех основных принципов и понятий химии, изменения терминологии и номенклатуры веществ. Поэтому с создания кислородной теории начался переломный этап в развитии химии, названный "химической революцией".
В 1785-1787 годах четыре выдающихся французских химика – Антуан Лоран Лавуазье, Клод Луи Бертолле, Луи Бернар Гитон де Морво и Антуан Франсуа де Фуркруа, – по поручению Парижской академии наук разработали новую систему химической номенклатуры. Логика новой номенклатуры предполагала построение названия вещества по названиям тех элементов, из которых вещество состоит. Основные принципы этой номенклатуры используются до настоящего времени.
В 1789 году Лавуазье издал свой знаменитый учебник "Элементарный курс химии", целиком основанный на кислородной теории горения и новой химической номенклатуре. Появление этого курса собственно и ознаменовало, по мнению Лавуазье, химическую революцию (1789 – год начала Французской революции, одной из жертв которой станет в 1794 году и Лавуазье). В "Элементарном курсе химии" Лавуазье привёл первый в истории новой химии список химических элементов (таблицу простых тел), разделённых на несколько типов:
| 1. Простые вещества, относящиеся ко всем царствам природы, которые можно рассматривать как элементы: | |
| СВЕТ ТЕПЛОРОД КИСЛОРОД | АЗОТ ВОДОРОД |
| 2. Простые неметаллические вещества, окисляющиеся и дающие кислоты: | |
| СЕРА ФОСФОР УГОЛЬ | РАДИКАЛ МУРИЕВОЙ КИСЛОТЫ (Cl) РАДИКАЛ ПЛАВИКОВОЙ КИСЛОТЫ (F) РАДИКАЛ БУРОВОЙ КИСЛОТЫ (B) |
| 3. Простые металлические вещества, окисляющиеся и дающие кислоты: | ||
| СУРЬМА СЕРЕБРО МЫШЬЯК ВИСМУТ ЗОЛОТО ВОЛЬФРАМ | КОБАЛЬТ МЕДЬ ОЛОВО ЖЕЛЕЗО ПЛАТИНА ЦИНК | МАРГАНЕЦ РТУТЬ МОЛИБДЕН НИКЕЛЬ СВИНЕЦ |
| 4. Простые солеобразующие землистые вещества: | ||
| ИЗВЕСТЬ ГЛИНОЗЁМ | МАГНЕЗИЯ КРЕМНЕЗЁМ | БАРИТ |
Касательно земель Лавуазье на основании их абсолютной инертности к кислороду высказывал предположение о том, что земли представляют собой оксиды неизвестных элементов, впоследствии полностью подтвердившееся. Особую группу для земель в своей таблице элементов Лавуазье выделил, поскольку строго придерживался определения элемента, данного Бойлем: "Если мы… свяжем с названием элементов… представление о последнем пределе, достигаемым анализом, то все вещества, которые мы ещё не смогли никаким способом разложить, являются для нас элементами. …Мы не можем уверять, что считаемое нами сегодня простым является таковым в действительности". Данную концепцию элементов принято называть эмпирико-аналитической, поскольку Лавуазье избрал критерием определения элемента опыт и только опыт, категорически отвергая любые неэмпирические рассуждения об атомах и молекулах, само существование которых невозможно подтвердить опытным путём. Эту концепцию Лавуазье предельно ясно сформулировал в предисловии к своему учебнику: "Я не считал возможным уклониться от требований строгого закона – не заключать ничего сверх того, что даёт непосредственно опыт и не стараться спешными заключениями восполнять молчание фактов".
Созданная Лавуазье рациональная классификация химических соединений основывалась, во-первых, на различии в элементном составе соединений и, во-вторых, на характере их свойств (кислоты, основания, соли, солеобразующие вещества, органические вещества). При этом, как и Бойль, Лавуазье считает, что свойства вещества определяются его составом. Зависимость свойств вещества от состава, описанная Лавуазье, представляет собой закономерность, отражающую взаимосвязь между качественными и количественными характеристиками вещества.
Важнейшим результатом исследований Лавуазье явилось формулирование им закона сохранения массы. Проанализировав результаты собственных исследований количественного состава веществ и соотношения масс реагентов и продуктов реакции, а также результаты подобных исследований других учёных, Лавуазье показал, что во всех случаях масса веществ в ходе химических реакций не изменяется: "Можно принять в качестве принципа, что во всякой операции количество материи одинаково до и после опыта, что качество и количество начал остаются теми же самыми". Следует отметить, что Лавуазье вывел закон сохранения массы опять-таки исключительно из экспериментальных данных, не используя каких-либо теоретических предпосылок, не основанных на опыте.
Химическая революция завершила период становления химии; она ознаменовала собой полную рационализацию химии, окончательный отказ от устаревших натурфилософских и алхимических представлений о природе вещества и его свойств. После химической революции химия вступила в период количественных законов, в котором была создана и развита новая концепция химического элемента – атомно-теоретическая.
4. ПЕРИОД КОЛИЧЕСТВЕННЫХ ЗАКОНОВ
(АТОМНО-МОЛЕКУЛЯРНОЙ ТЕОРИИ)
Стехиометрия - Атомистическая теория Дальтона - Проблема определения атомных масс - Электрохимические теории сродства
Стехиометрия
Блестящие успехи количественных методов исследования вещества, сделавшие возможной химическую революцию, уже в начале XIX века привели к новому фундаментальному изменению в естествознании вообще и в химии в частности. За открытым Лавуазье законом сохранения массы последовал целый ряд новых количественных закономерностей – стехиометрические законы.
Первым стехиометрическим законом стал закон эквивалентов, который сформулировал немецкий химик Иеремия Вениамин Рихтер в результате проведённых им в 1791-1798 годах опытов по изучению количеств вещества в реакциях нейтрализации и обмена, обобщённых в работе "Начальные основания стехиометрии или искусства измерения химических элементов". Первоначальная формулировка закона эквивалентов (термин "эквивалент" ввёл в 1767 году Г.Кавендиш) была следующей: "Если одно и то же количество какой-либо кислоты нейтрализуется различными количествами двух оснований, то эти количества эквивалентны и нейтрализуются одинаковым количеством любой другой кислоты".
Открытый Рихтером закон подтвердил убеждения многих химиков в том, что химические соединения взаимодействуют не в произвольных, а в строго определённых количественных соотношениях. Однако за этим последовала длительная дискуссия о том, присуща ли такая определённость всем без исключения химическим процессам. Основным предметом дискуссии стал вопрос о том, является ли постоянным соотношение элементов в соединении, состоящем из двух или более элементов, или же состав зависит от способа получения вещества. Клод Луи Бертолле, основываясь на предложенной им теории химического сродства*, обусловленного силами притяжения и зависящего от плотности вещества и его количества, отстаивал предположение о том, что элементный состав вещества может изменяться в некоторых пределах в зависимости от условий, в которых оно было получено.
В полемику с Бертолле отважился вступить французский химик Жозеф Луи Пруст. С помощью тщательных анализов в 1799-1806 годах Пруст установил, что отношение количеств элементов в составе соединения всегда постоянно. Выводы Бертолле, как показал Пруст, были ошибочны из-за неточности анализов и недостаточной чистоты исходных веществ. Дискуссия завершилась блестящей победой Пруста. Закон постоянства состава (постоянных отношений) в итоге не просто был признан большинством химиков, но стал одним из главных химических законов. Однако вопрос о причинах постоянства состава оставался открытым, поскольку из чисто аналитической концепции химического элемента это никоим образом не следует. Разрешить существующие сомнения могло лишь предположение о дискретности материи, однако атомистические взгляды по-прежнему не имели никаких экспериментальных доказательств.
*Термин избирательное сродство предложил в 70-е годы XVIII века Торберн Улаф Бергман для объяснения реакционной способности веществ; он же составил первые таблицы сродства.
Атомистическая теория Дальтона
Экспериментальное подтверждение атомной гипотезы нашёл английский химик Джон Дальтон. В начале XIX века Дальтон открыл несколько новых эмпирических закономерностей: закон парциальных давлений (закон Дальтона), закон растворимости газов в жидкостях (закон Генри-Дальтона) и, наконец, закон кратных отношений.
Объяснить эти закономерности (прежде всего закон кратных отношений), не прибегая к предположению о дискретности материи, невозможно. Основываясь на законе кратных отношений, открытом в 1803 году, и законе постоянства состава, Дальтон разработал свою атомно-молекулярную теорию, изложенную в вышедшем в 1808 году труде "Новая система химической философии".
Основные положения теории Дальтона состояли в следующем:
1. Все вещества состоят из большого числа атомов (простых или сложных).
2. Атомы одного вещества полностью тождественны. Простые атомы абсолютно неизменны и неделимы.
3. Атомы различных элементов способны соединяться между собой в определённых соотношениях.
4. Важнейшим свойством атомов является атомный вес.
Уже в 1803 года в лабораторном журнале Дальтона появилась первая таблица относительных атомных весов некоторых элементов и соединений; в качестве точки отсчёта Дальтон выбрал атомный вес водорода, принятый равным единице. Для обозначения атомов элементов Дальтон использовал символы в виде окружностей с различными фигурами внутри. Впоследствии Дальтон неоднократно корректировал атомные веса элементов, однако для большинства элементов им приводились неверные значения атомных весов.
| Простые атомы | Сложные атомы | ||||
 | Водород | 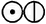 | Аммиак | ||
 | Кислород | 5.66 | 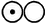
 Сейчас читают про:
|
 2015-04-17
2015-04-17 4108
4108






