Важнейшей количественной кинетической характеристикой химической реакции является ее скорость.Существует несколько понятий, определяющих скорость химических превращений.
1. Скоростью образования i-го компонента (скорость химической реакции по i-му веществу) (ri) называется изменение количества этого вещества (числа молекул или количества молей) в единицу времени в единице реакционного пространства:
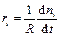 , (4.1)
, (4.1)
где R –величина реакционного пространства, 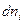 - изменение количества молей i -гокомпонента. Если реакция гомогенная и протекает в объеме, то реакционным пространством является объем (R ≡ V). Если реакция гетерогенная и протекает на границе фаз, то реакционным пространством является поверхность (R ≡ S).
- изменение количества молей i -гокомпонента. Если реакция гомогенная и протекает в объеме, то реакционным пространством является объем (R ≡ V). Если реакция гетерогенная и протекает на границе фаз, то реакционным пространством является поверхность (R ≡ S).
Количество вещества, реагирующего в единицу времени, всегда пропорционально величине реакционного пространства. Поэтому скорость относят к единице реакционного пространства. Изменение количества вещества в реакционном пространстве может быть обусловлено как протеканием реакции, так и обменом веществом с окружающей средой. Поэтому следует отдельно рассматривать открытые и закрытые системы.
 2015-04-01
2015-04-01 414
414








