Для насыщенных углеводородов характерны реакции радикального замещения
s - связи в молекулах алканов практически неполярны, обладают высокой прочностью, не подвергаются гетеролитическому разрыву под действием электрофилов и нуклеофилов. Могут участвовать в реакциях только с высокореакционноспособными радикалами.
Радикалы могут быть получены в процессе:
1) термолиза (тепловая энергия);
2) фотолиза (лучистая энергия);
3) окисления-восстановления (химическая энергия);
4) под действием вибрации и ультразвука (механическая энергия).
Механизм радикального замещения характерен для радикального галогенирования и окисления кислородом:
1) Радикальное галогенирование
Галогены очень сильно различаются по своей реакционной способности. Практическое значение имеют только хлорирование и бромирование, так как со фтором органические молекулы реагируют со взрывом, а йод замедляет радикальные процессы.
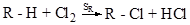
Механизм:
1. Инициирование (зарождение цепи)
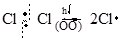
2. Рост цепи
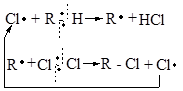
3. Обрыв цепи
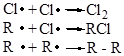
2) Окисление кислородом:
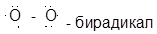
| 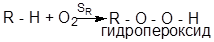
|
молекула кислорода
Механизм:
1. Инициирование (зарождение цепи)
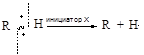
2. Рост цепи
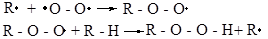
3. Обрыв цепи

Если реакция окисления проходит под действием атмосферного воздуха, то она называется автоокислением, например, образование гидропероксидов при стоянии на свету и воздухе простых эфиров, в том числе диэтилового эфира, применяемого в медицине, а также порча пищевых продуктов на воздухе. В организме к подобным процессам относится пероксидное окисление липидов:
Пероксидное окисление липидов:
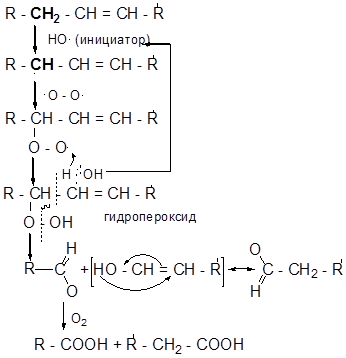
В результате образуются карбоновые кислоты с более короткими углеводородными цепями.
Выбор реакционного центра в реакциях SR
Для сложных органических соединений реакция радикального замещения протекает избирательно в тех атомах углерода субстрата, которые дают наиболее устойчивые промежуточные радикалы. Для выбора реакционного центра необходимо учитывать следующие правила:
Правила устойчивости радикалов:
1. Устойчивость промежуточного радикала повышается, если рядом с атомом углерода в реакционном центре имеется двойная связь или ароматическое кольцо:
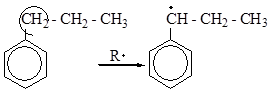
2. Устойчивость радикалов уменьшается в ряду:
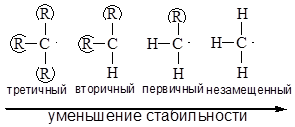
 2015-05-06
2015-05-06 950
950








