Общая формула: 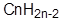
Для алкинов характерна только структурная изомерия (изомерия цепи и положения тройной связи).
Способы получения:
Из простых веществ ацетилен был получен впервые в XIX веке французским химиком Бертло:
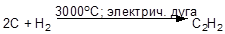
В промышленности ацетилен получают крекингом метана:
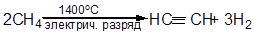
Наиболее перспективным промышленным методом является получение ацетилена из оксида углерода (II) и водорода в присутствии катализатора:
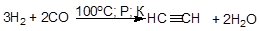
В лаборатории ацетилен обычно получают из карбида кальция:
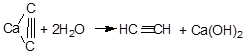
Однако, этот синтез достаточно дорог, так как получение карбида связано с высокими энергозатратами:
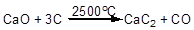
Более дешевыми методами являются реакции получения алкинов из ди- и тетра- галогенопроизводных алканов:
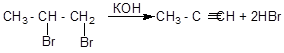
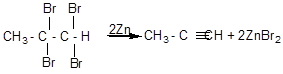
Химические свойства:
В алкинах атомы углерода, участвующие в образовании тройной связи, находятся в состоянии sp гибридизации:

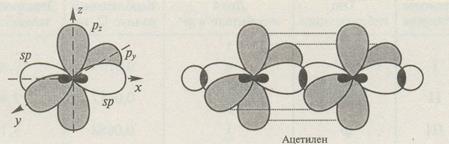
1. Реакции присоединения (АЕ):
а) галогенирование
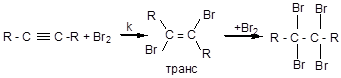
б) гидрогалогенирование
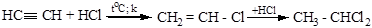
в) гидратация (реакция Кучерова)
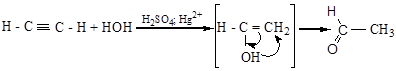
г) гидрирование
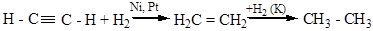
д) присоединение спиртов
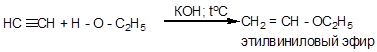
2. Реакции полимеризации:
а) реакция Ньюленда
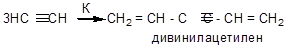
б) реакция Зелинского
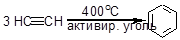
4. Окисление
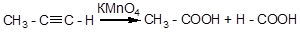
Горение ацетилена в кислороде сопровождается выделением тепла, позволяющего достигать температуры до 3000оС (автогенная сварка, резка металлов).
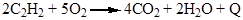
На воздухе ацетилен горит коптящим пламенем, т.к. в результате неполного сгорания образуется углерод.
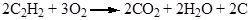
4. Образование ацетиленидов
Ацетилен и его гомологи с тройной связью на конце молекулы способны взаимодействовать со щелочными металлами и солями некоторых тяжелых металлов (Ag, Cu) с замещением водорода при тройной связи на металл с образованием ацетиленидов.

 2015-05-06
2015-05-06 2195
2195








