В итоге путей распада аминокислот в организме образуются аммиак, углекислый газ и вода. Углекислый газ частично выводится из организма, а другая часть используется для синтеза жирных кислот, пуриновых и пиримидиновых азотистых оснований, глюкозы.
Аммиак образуется в основном при дезаминировании аминокислот, распада пуриновых и пиримидиновых азотистых оснований, глутамина и биогенных аминов.
Для организма аммиак очень токсичен, особенно для ЦНС. Поэтому организм выработал эффективные механизмы обезвреживания аммиака. Основные механизмы: образование глутамина, восстановительное аминирование, нейтрализация органических и неорганических кислот, синтез мочевины.
Образование глутамина. Синтез глутамина происходит в основном в местах непосредственного образования аммиака, например в печени и мозге, где обнаружена активная глутаминсинтетаза, катализирующая этот синтез. В результате предотвращается проявление токсического действия аммиака.
Включенный в молекулу глутамина азот аммиака используется организмом для синтеза пуриновых и пиримидиновых азотистых оснований, мукополисахаридов (глюкозамины). Это показывает взаимосвязь обмена белков с обменом нуклеопротеидов и углеводов. Кроме того, глутамин транспортирует аммиак в почки.
Восстановительное аминирование — это процесс связывания аммиака с альфа-кетокислотами с образованием заменимых аминокислот. Активный фермент глутаматдегидрогеназа катаболизирует образование глутаминовой кислоты из альфа-кетоглутаровой кислоты.
Нейтрализация неорганических и органических кислот аммиаком приводит к образованию аммонийных солей. Этот процесс активно протекает в почках.
Синтез мочевины служит основным путем детоксикации аммиака у человека и главной формой выделения белкового азота из организма. Печень является органом, где происходит обезвреживания аммиака.
Процесс синтеза мочевины можно разделить на три этапа. На первых двух этапах две молекулы аммиака связываются в безвредные для организма соединения, а на третьем этапе фактически образуется молекула мочевины.
I этап. Молекула аммиака и углекислого газа за счет энергии, освобождающейся при распаде АТФ, превращается в карбомоилфосфат, который, взаимодействуя с орнитином (аминокислота, не входящая в состав белков), образует цитруллин, где зафиксированы первая молекула аммиака и углекислого газа.
II этап. Вторая молекула аммиака связывается с альфа-кетоглутаровой кислотой с образованием глутаминовой кислоты (восстановительное аминирование). А глутаминовая кислота в ходе переаминирования передает зафиксированную вторую молекулу аммиака в виде аминогруппы на щавелевую кислоту, которая при этом превращается в аспарагиновую кислоту.
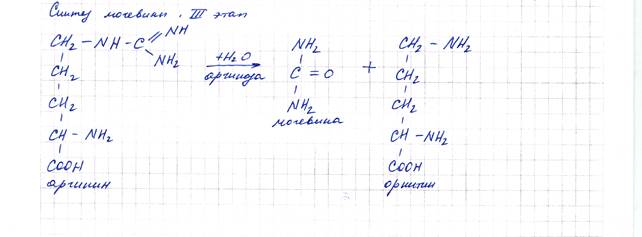
III этап. На этом этапе цитруллин и аспарагиновая кислота при участии АТФ образуют аргининянтарную кислоту, содержащую две связанных молекулы аммиака. Эта кислота распадается на фумаровую кислоту и аргинин. Под действием аргиназы аргинин образует мочевину и орнитин. Мочевина поступает из печени в кровь, где ее содержание — 0,2-0,3 г/л, а затем выводится почками из организма. Орнитин вновь используется в синтезе мочевины.


 2015-04-30
2015-04-30 5781
5781








