Первая попытка создания модели атома принадлежит Дж. Дж. Томсону (1903). Согласно этой модели, атом представляет собой непрерывно заряженный положительным зарядом шар радиусом порядка 10-10 м, внутри которого около своих положений равновесия колеблются электроны. Суммарный положительный заряд шара равен заряду электронов, так что атом в целом нейтрален.
В 1911г. Э. Резерфорд, анализируя процесс рассеяния a- частиц при прохождении через тонкие слои вещества, предложил ядерную (планетарную) модель атома. Согласно Резерфорду, атом представляет собой систему зарядов, в центре которой расположено тяжелое положительное ядро с зарядом Ze, имеющее размер 10-15-10-14 м и массу, практически равную массе атома. Вокруг ядра в области с линейными размерами порядка 10-10 м расположены Z электронов, распределенных по всему объему, образуя электронную оболочку атома.
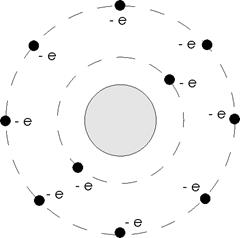 |
Рис. 1. Планетарная модель атома.
Однако ядерная модель оказалась в противоречии с законами классической механики и электродинамики. Поскольку система неподвижных зарядов не может находиться в устойчивом состоянии, Резерфорду пришлось отказаться от статической модели атома и предположить, что электроны движутся вокруг ядра по замкнутым круговым орбитам. Но в этом случае электроны будут двигаться с ускорением (так как любое тело, двигаясь по окружности, обладает центростремительным ускорением), в связи с чем, согласно классической электродинамике, они должны непрерывно излучать электромагнитные волны. Процесс излучения сопровождается потерей энергии, так что электрон, в конечном счёте, должен упасть на ядро. Этого же не происходит.
Попытки построить модель атома в рамках классической физики не привели к успеху. Выход из создавшегося тупика был найден в 1913г. датским физиком Нильсоном Бором. В теории Бора не содержалось принципиального отказа от описания поведения электронов в атоме при помощи законов классической физики, однако, ему пришлось делать некоторые ограничения, противоречащие классическим представлениям. Эти ограничения сформулированы в виде двух постулатов:
1. Существуют некоторые стационарные состояния атома, находясь в которых он не излучает энергии. Стационарным состоянием атома соответствуют стационарные орбиты, по которым движутся электроны, имеющие дискретные квантованные значения момента импульса, удовлетворяющие условию:
 (n = 1,2.3…).
(n = 1,2.3…).
2. При переходе электрона с одной стационарной орбиты на другую излучается (поглощается) один фотон с энергией 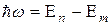 , равной разности энергий соответствующих стационарных состояний.
, равной разности энергий соответствующих стационарных состояний.
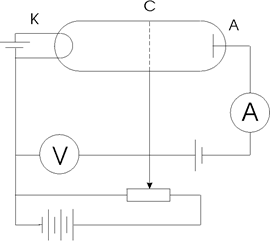 |
Квантовый характер поглощения энергии атомом, постулированный Бором, экспериментально подтверждён опытами Франка и Герца, поставленными в 1913 г. Схема установки изображена на рис.2.
Рис. 2.
В трубке, заполненной парами ртути, под небольшим давлением (~1мм рт. ст.) имелись три электрода: катод К, сетка С и анод А. Электроны, вылетающие из разогретого катода, ускорялись разностью потенциалов U, приложенной между катодом и сеткой. Эту разность потенциалов можно было плавно менять. Между сеткой и анодом создавалось слабое задерживающее электрическое поле 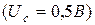 , тормозившее движение электронов к аноду.
, тормозившее движение электронов к аноду.
Электроны, встречающие на своём пути атомы, могут испытывать с ними соударения двоякого рода.
Первый тип соударений - упругие столкновения, в результате которых энергия электронов не изменяется, а изменяется лишь направление скорости электронов. Такие столкновения, хотя и затрудняют попадание электронов на анод, не могут явиться причиной резкого спада анодного тока в трубке, который должен возрастать с увеличением ускоряющей разности потенциалов U.
Второй тип возможных соударений электронов с атомами - неупругие столкновения - связан с потерей электронами их энергии и передачей этой энергии атомам ртути.
В соответствии с постулатами Бора каждый из атомов ртути может поглотить лишь определённую энергию и перейти в одно из возбуждённых энергетических состояний. Ближайшее к нормальному состоянию атома ртути – возбуждённое состояние, отстоящее от основного по шкале энергий на 4,86 эВ.
До тех пор, пока электроны, ускоряемые полем, не приобретут энергию W1 = 4,86 эВ, они испытывают лишь упругие столкновения, и анодный ток возрастает. Как только кинетическая энергия достигает 4,86 эВ, начинаются неупругие столкновения. Электрон с таким значением энергии полностью отдаёт её атому ртути, вызывая переход одного из электронов атома из нормального энергетического состояния в возбуждённое. Такой электрон, потерявший свою кинетическую энергию, не сможет преодолеть задерживающее его поле и не достигнет анода. Таким образом, при разности потенциалов между катодом и сеткой, равной 4,86 эВ, должно происходить резкое падение анодного тока. Аналогичное явление происходит при W 2= 2 × 4,86 эВ, W 3 = 3 × 4,86 эВ и, вообще говоря, при Wn = n × 4,86 эВ, когда электроны могут испытывать два, три и т.д. неупругих соударения с атомами ртути, теряя полностью свою энергию и не достигая анода. На рис.3 приведена характерная кривая зависимости анодного тока от разности потенциалов между катодом и сеткой в опытах Франка и Герца.
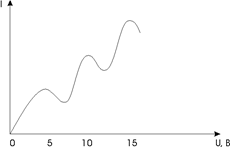 |
Рис. 3.
 2015-05-13
2015-05-13 615
615








