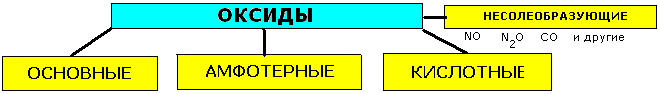
Оксиды- сложные вещества, состоящие из двух химических элементов, один из которых кислород в степени окисления -2.
Реакционная способность элементов во взаимодействии с кислородом, вообще
говоря, уменьшается при перемещении вправо вдоль каждого периода. Например,
в 3-м периоде два s-металла, натрий и магний, и два р-элемента, алюминий и
фосфор, бурно реагируют с кислородом, образуя оксиды. В том же периоде
элементы кремний и сера способны только медленно реагировать с кислородом.
Хлор и аргон, расположенные в правом конце периода, вообще не реагируют с
кислородом.
Электроположительные s-металлы образуют ионные оксиды, как, например, оксид
натрия Na2O и оксид магния MgO. Оксиды элементов, расположенных в
средней и правой частях периода, являются преимущественно ковалентными
соединениями, как, например, оксиды азота и серы.
Кислотно-основный характер оксидов тоже изменяется от основного у оксидов
элементов левой части периода к амфотерному у оксидов элементов средней части
|
|
|
периода и далее к кислотному у оксидов элементов правой части периода.
Например, s-металлы обычно образуют оксиды, которые растворяются в воде с
образованием щелочных растворов:
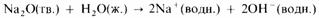
Молекулярные оксиды р-элементов, например диоксид углерода и триоксид серы,
обычно обладают кислотными свойствами. Закономерное изменение основных
свойств с переходом к кислотным свойствам наглядно проявляется у оксидов
элементов 3-го периода.
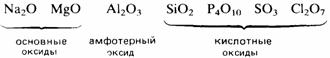
ПОЛУЧЕНИЕ ОКСИДОВ.
| Окисление кислородом | простых веществ | 2Mg +O2=2MgO | |||
| сложных веществ | 2H2S+3O2=2H2O+2SO2 | ||||
| Разложение | нагреванием солей | СaCO3=CaO+CO2 
| |||
| нагреванием оснований | Cu (OH)2=CuO+H2O | ||||
| нагреванием кислородсодержащих кислот | H2SO3=H2O+SO2 
| ||||
| нагреванием высших оксидов | 4CrO3=Cr2O3+3O2 
| ||||
| Окисление низших оксидов | 4FeO+O2=2Fe2O3 | ||||
| Вытеснение летучего оксида менее летучим | Na2CO3+SiO2=Na2SiO3+CO2 
| ||||
| |||||
| Основные-реагируют с избытком кислоты с образованием соли и воды.Основным оксидам соответствуют основания. 1.Взаимодействие с водой(оксиды щелочных и щелочноземельных мет.) CaO+H2O=Ca(OH)2 2.Все-с кислотами МgO+2HCl=MgCl2+H2O 3.С кислотнями оксидами CaO+CO2=CaCO3 4.С амфотерными оксидами Li2O+Al2O3=2LiAlO2 | Амфотерные (ZnO, Al2O3,Cr2O3, MnO2) 1.Взаимодействуют как с кислотами, так и с основаниями. ZnO+2HCl=ZnCl2+H2O ZnO+2NaOH+H2O=Na2[Zn(OH)4] 2.Реагируют с основными и кислотными оксидами ZnO+CaO=CaZnO2 ZnO+SiO2=ZnSiO3 | Кислотные-реагируют с избытком щелочи с образованием соли и воды. Кислотным оксидам часто соответствуют кислоты. 1.Большинство взаимодействуют с водой SO3+H2O=H2SO4 2.Со щелочами NaOH+SiO2=Na2SiO3+H2O 3.С основными оксидами SiO2+CaO=CaSiO3 4.С амфотерными оксидами Al2O3+3SO3=Al2(SO4)3 | |||
Жиры» их состав и свойства. Жиры в природе, превращение жиров в организме. Продукты технической переработки жиров, понятие о синтетических моющих средствах. Защита природы от загрязнения CMC.
|
|
|
Жиры – это сложные эфиры глицерина и высших карбоновых кислот (стеариновой, пальмитиновой, линоленовой, олеиновой и др.). Синтез одного из жиров (тристеарина) можно представить схемой:
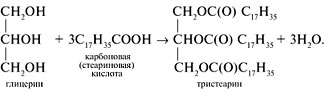
По происхождению жиры подразделяют на животные и растительные.
К животным жирам относят свиной и говяжий жиры, барсучье сало, жиры млекопитающих, рыбий жир.
Растительные жиры называют маслами. Известны соевое, подсолнечное, оливковое, облепиховое, кокосовое и другие масла.
В составе животных жиров преобладают остатки предельных кислот, а в составе растительных – остатки непредельных кислот.
Остатки карбоновых кислот могут быть одинаковыми (простые жиры) или различными (смешанные жиры).
По физическим свойствам жиры – легкоплавкие, твердые или жидкие вещества. Жиры нерастворимы в воде, зато хорошо растворяются в органических растворителях (ацетон, керосин, бензин).
Проведите лабораторный опыт и посмотрите, происходит ли растворение жира (подсолнечного масла) в холодной воде, бензине и ацетоне.
Жиры не имеют точки плавления и плавятся в широком интервале температур. При высоких температурах жиры разлагаются. Плотность жиров меньше 1 г/мл, они бывают различными по окраске, впитывают запахи других веществ.
Химические свойства жиров определяются их принадлежностью к классу сложных эфиров. Поэтому наиболее характерная реакция жиров – гидролиз. Непредельные жиры могут вступать в реакцию окисления, например окисляются кислородом воздуха.
Реакция гидролиза жиров:
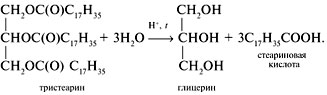
Уравнение реакции гидрирования жиров:
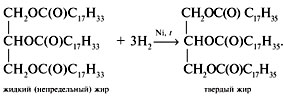
Все природные жиры — смесь глицеридов, не только симметричных, т.е. с тремя одинаковыми остатками жирных кислот, но и смешанных. Симметричные глицериды встречаются чаще в растительных маслах. Животные жиры отличаются весьма разнообразным составом жирных кислот. Жирные кислоты, входящие в состав триглициридов, определяют их свойства. Триглицириды способны вступать во все химические реакции, свойственные эфирам. Наибольшее значение имеет реакция омыления, в результате которой из триглицирида образуется глицерин и жирные кислоты.
Омыление происходит как при гидролизе, так и при действии кислот или щелочей.
Жиры — питательное вещество, является обязательной составной частью сбалансированного пищевого рациона человека. Они — важный источник энергии, который можно рассматривать как природный пищевой концентрат большой энергетической ценности, способный в небольшом объеме обеспечить организм энергией. Средняя потребность жиров для человека — 80-100 г в сутки. Один грамм жиров при окислении дает 9,3 ккал. Жиры также являются растворителями витаминов A, D и E. Обеспеченность организма в этих витаминах зависит от поступления жиров в составе пищи. С жирами в организм вводится комплекс биологически активных веществ, играющих важнейшую роль в нормальном жировом обмене.
СМС это "вещества или смеси веществ, применяемые в водных растворах для очистки (отмывки) поверхности твёрдых тел от загрязнений." Они содержат гидрофильную часть (в данном случае - карбоксильную группу) и гидрофобную часть (углеводородный радикал).
Другие названия синтетических моющих средств - детергенты и CMC. Примеры CMC: мыло, моющее средство для посуды, шампунь и т.д.
Как работают синтетические моющие средства? Очень просто. Но перед этим давайте разберёмся, какую грязь нужно отмывать с их помощью. Грязь, которую нужно отмывать с помощью детергентов - это грязь, которую не получается отмыть простой водой. То есть, это нерастворимая в воде грязь. Например, это жир. Или масло. Соответственно, поскольку вода не может отмыть жир или масло, то нужны вещества, которые позволят это сделать. Собственно, этим и занимаются синтетические моющие средства. Как же они это делают? Как уже говорилось, очень просто: детергенты состоят из двух частей. Одна часть растворяется в масле, а вторая часть-растворяется в воде.
|
|
|
Принцип работы CMC - молекула детергента одним концом (который может соединиться с жиром) Синтетические моющие средства встраивается в жир. Несколько молекул окружают каплю жира со всех сторон. Результат: грязь с жиром стала растворяться в воде. Почему? Потому что синтетические моющие средства спрятали свои "жирные" части в грязь, а "водные" части выставили наружу. Соответственно, вода легко отделяет обработанную детергентами часть жиросодержащей грязи.
Итак, вывод: в нашем случае синтетические моющие средства - это вещества, которые с помощью своего двойного строения позволяют растворять воде то, что она обычно растворить не может, например, подсолнечное масло со сковородки.
Чем вредят синтетические моющие средства в воде?
То есть, мы определили, что такое CMC, как они работают, и теперь можем переходить к их влиянию в воде. Могут ли детергенты оказаться в воде? Естественно, так как именно для воды они и предназначены.
Рассмотрим примерный путь, каким проходит детергент в обычном доме:
Первый шаг - покупка синтетического моющего средства для мытья посуды.
Второй шаг - намыливание этим CMC губки и мытьё сковороды с маслом.
Далее детергент окружает масло, заставляет его растворяться в воде, и попадает в канализацию.
Оттуда синтетическое моющее средство попадает в реку.
Синтетические моющие средства Возможно, между канализацией и рекой существует очистительная станция. Но поскольку в нашей стране очистительные станции слегка устарели (лет на 20), то будем считать, что её нет.
Итак, CMC в реке. И основные, кто страдает or синтетических моющих средств - это животные, которые дышат жабрами. То есть, рыбы, раки и прочие мелкие зверьки. Почему страдают именно они? Потому что CMC прилипают к жабрам, вода начинает прилипать к CMC, в жабры льётся вода, и рыбы захлёбываются. И умирают. Или (если детергентов не очень много), просто растут больными и хилыми. Другими словами: в обычном состоянии, хоть вода и попадает в жабры, но она не касается их, поскольку они покрыты отталкивающим воду веществом - специальным жиром. А поскольку моющие средства растворяют жир, то рыба не может пользоваться жабрами.
|
|
|
Вывод: синтетические моющие средства действительно вредны для водных обитателей.
3. Задача. Какое количество вещества этана получится при пропускании 6,72 г этена, содержащего 20% примесей, с водородом над нагретым никелевым катализатором?

 2015-05-13
2015-05-13 2234
2234







