Кривой заряжения называют зависимость потенциала электрода Е от количества электричества ∆Q, сообщенного электроду. Чаще всего при снятии кривых заряжения поддерживают постоянным ток, пропускаемый через ячейку: I = const, иначе говоря, измерения проводят в гальваностатических условиях. Так как при I = const количество электричества и время t связаны между собой прямой пропорциональной зависимостью ∆Q = I*t, то наряду с изображением кривой заряжения в координатах Е - ∆Q можно пользоваться координатами Е – t.
Для того чтобы при снятии кривых заряжения получить данные о строении двойного электрического слоя, необходимо соблюдение некоторых условий. Прежде всего, следует исключить возможность протекания посторонних электрохимических реакций, например, электровосстановление кислорода и электроокисление водорода, растворенных в электролите, процессы с участием различных загрязнений и т.д. Измерения следует проводить в области потенциалов, где фарадеевские процессы (например, выделение газообразного водорода или кислорода, растворение материала электрода и т.п.) не протекают.
Впервые условия снятия кривых заряжения платинового электрода были сформулированы А.Н.Фрумкиным и А.И.Шлыгиным, которые выполнили первые такие измерения на платинированной платине.
На полной кривой заряжения (Рис.1) можно выделить три области: водородную (0,05 – 0,35 В), двойнослойную (0,4 – 0,75 В) и кислородную (0,75 – 1,45 В) (относит. н.в.э.).
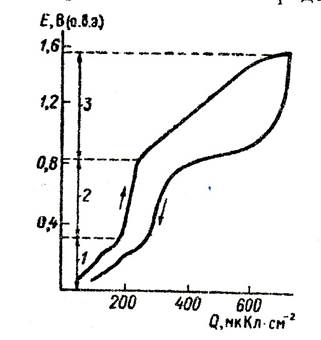
Рис.1
Кривая заряжения платинового электрода в 0,5М растворе H2SO4
1 – водородная, 2 – двойнослойная, 3 – кислородная области
Следует иметь в виду, что это деление условно. Количество электричества ∆Q, сообщенное электроду, затрачивается на изменение количества адсорбированного водорода ∆АН или кислорода ∆АО и изменение свободного заряда поверхности ∆q. Основная часть подводимого электричества в водородной и кислородной областях кривой заряжения затрачивается соответственно на посадку – ионизацию водорода или кислорода. В двойнослойной области основная часть подводимого электричества затрачивается на изменение заряда двойного электрического слоя. Было доказано, что в сернокислых растворах в двойнослойной области потенциалов происходит постепенное уменьшение количества адсорбированного водорода и возрастание количества адсорбированного кислорода, т.е. наблюдается перекрывание областей адсорбции водорода и кислорода. Степень этого перекрывания зависит от рН раствора и концентрации ионов SO42- и уменьшается с уменьшением рН и с ростом концентрации SO42-. В целом, однако, количество адсорбированных водорода и кислорода в сернокислых растворах на платине в двойнослойной области невелико. Степень перекрывания областей адсорбции водорода и кислорода зависит также от природы металла. Так, она наименьшая в сернокислых растворах на палладии и возрастает при переходе к платине, иридию, родию, рутению и осмию.
По кривой заряжения можно приближенно рассчитать количество адсорбированных атомов водорода ∆АН и кислорода ∆АО. Определив ∆АН и ∆АО, следует убедиться, что количество электричества, затраченное на посадку монослоя кислорода, в два раза больше, чем количество электричества, полученное при ионизации водорода, т.е. ∆АО = 2∆АН, поскольку на посадку одного атома кислорода требуется два электрона.
Зная ∆АН, можно рассчитать истинную поверхность электрода, поскольку на одном поверхностном атоме платины адсорбируется один атом водорода. Для этого можно использовать как величину ∆АН, поделив ее на 1,31.1015 (т.е. число атомов, адсорбированных на 1 см2 поверхности электрода), так и ее эквивалент в электрических единицах, поделив его на 2,1.10-4 Кл, что соответствует монослою водорода на 1 см2 поверхности. Знание истинной поверхности позволяет рассчитать фактор шероховатости, который равен отношению истинной поверхности к видимой.
 2015-05-26
2015-05-26 582
582








