обнаружили химическое действие
электрического тока
NaCl + H2O = +NaOH + H -Cl
+ _
| Электролиз – явление выделения на электродах веществ, входящих в состав электролита, при прохождении через него электрического тока. |
| - |
+ _
_ +
_ +
| Электролитической диссоциацией называется расщепление молекул электролита на положительные и отрицательные ионы под действием растворителя. |
1833 г. фр. физик Фарадей – законы электролиза .
Первый закон
Масса вещества выделяющегося на электроде, пропорциональна электрическому заряду, прошедшему через электролит.
m = k Qили m = k I Δt
k – электролитический коэффициент вещества.
[k] = [ 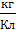 ] ]
|
Второй закон
Электролитический коэффициент вещества пропорционален его химическому эквиваленту.
k =  * *  F- постоянная Фарадея
F = e Na = 9, 648 * 104 Кл/моль
F- постоянная Фарадея
F = e Na = 9, 648 * 104 Кл/моль
 – химический эквивалент вещества,
где А – атомная масса, n – валентность элемента. – химический эквивалент вещества,
где А – атомная масса, n – валентность элемента.
|
| Первый гальванический элемент |

Носители тока в жидкостях – «+» и «-» ионы.
| Газы |
| Несамостоятельный разряд – разряд, происходящий под действием внешнего ионизатора. |
| Самостоятельный разряд – разряд, который не прекращается, если убрать внешний ионизатор. |
Ионизация – явление отрыва электрона от атома.
виды ионизации: самостоятельный разряд возникает
- Термоионизация – ионизация за счёт при ионизации электронным ударом.
столкновения атомов при высокой температуре.
 2015-05-26
2015-05-26 650
650








