Специфический иммунный ответ развивается в организме параллельно с развитием инфекции или после вакцинации и приводит к формированию ряда специфических эффекторных механизмов противоинфекционной защиты:
1. Гуморальный иммунный ответ (В-лимфоцит);
2. Клеточный иммунный ответ (Т-лимфоцит);
3. Иммунологическая память (Т- и В-лимфоциты);
4. Иммунологическая толерантность.
К этим механизмам относятся эффекторные молекулы ( антитела ) и эффекторные клетки ( Т-лимфоциты и макрофаги) иммунной системы.
Гуморальные иммунные реакции
В гуморальных иммунных реакциях участвуют три клеточных типа: макрофаги (Аг-представляющие клетки), Т-хелперы и В-лимфоциты.
Аг-представляющие клетки фагоцитируют микроорганизм и перерабатывают его, расщепляя на фрагменты (процессинг Аг). Фрагменты Аг выставляются на поверхности Аг-представляющей клетки вместе с молекулой МНС. Комплекс «Аг-молекула МНС класса II» предъявляется Т-хелперу. Распознавание комплекса Т-хелпером стимулирует секрецию ИЛ-1 макрофагами.
Т-хелпер под действием ИЛ-1 синтезирует ИЛ-2 и рецепторы к ИЛ-2; последний стимулирует пролиферацию Т-хелперов, а также ЦТЛ. Таким образом, после взаимодействия с Аг-представляющей клеткой Т-хелпер приобретает способность отвечать на действие ИЛ-2 бурным размножением. Биологический смысл этого явления состоит в накоплении Т-хелперов, обеспечивающих образование в лимфоидных органах необходимого пула плазматических клеток, вырабатывающих АТ к данному Аг.
В-лимфоцит. Активация В-лимфоцита предполагает прямое взаимодействие Аг с молекулой Ig на поверхности В-клетки. В этом случае сам В-лимфоцит перерабатывает Аг и представляет его фрагмент в связи с молекулой МНС II на своей поверхности. Этот комплекс распознает Т-хелпер, отобранный при помощи того же Аг. Узнавание рецептором Т-хелпера комплекса Аг-молекула МНС класса II на поверхности В-лимфоцита приводит к секреции Т-хелпером ИЛ-2, ИЛ-4, ИЛ-5, ИЛ-6, под действием которых В-клетка размножается, образуя клон плазматических клеток (плазмоцитов). Плазмоциты синтезируют антитела. Часть зрелых В-лимфоцитов после антигензависимой дифференцировки циркулируют в организме в виде клеток памяти.
Антитела, специфически взаимодействуя с антигенными детерминантами (эпитопами) на поверхности микроорганизмов, образуют с ними иммунные комплексы, что ведет к активации мембраноатакующего комплекса системы комплемента и лизису микробных клеток. Кроме того, иммунные комплексы, включающие микроорганизмы и специфические антитела, быстрее и легче захватываются фагоцитирующими клетками организма при участии Fc-рецепторов. При этом ускоряется и облегчается внутриклеточная гибель и переваривание. Защитная роль антител в антитоксическом иммунитете определяется также их способностью нейтрализовать токсины. Секреторные иммуноглобулины класса А обеспечивают местный специфический иммунитет слизистых оболочек, препятствуя прикреплению и проникновению патогенных микроорганизмов.
Вместе с тем гуморальная защита малоэффективна против внутриклеточно паразитирующих бактерий, риккетсий, хламидий, микоплазм, грибов, простейших и вирусов. Против этих возбудителей более эффективны клеточные механизмы специфического иммунитета, к которым относится иммунное воспаление - реакция гиперчувствительности замедленного типа (ГЗТ) и цитотоксическая активность Т-киллеров, NК-клеток, макрофагов.
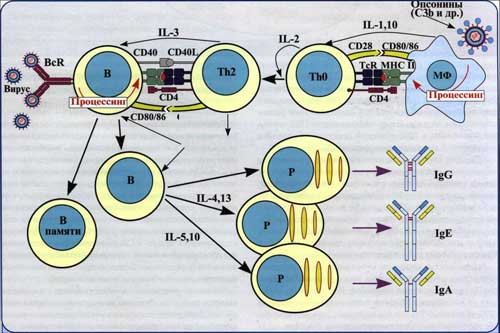
Рис. 1. Гуморальный иммунный ответ. В результате кооперации макрофагов, Т-хелперов и В-лимфоцитов и дальнейшей дифференцировки В-лимфоцитов в плазматические клетки, последние продуцируют антитела, которые нейтрализуют антиген.
Клеточные иммунные реакции
В очаге иммунного воспаления Т-эффекторы ГЗТ, активированные при контакте с микробными антигенами, продуцируют лимфокины, индуцирующие микробоцидные механизмы фагоцитов. В результате усиливается внутриклеточная гибель захваченных фагоцитами возбудителей.
Гибель клеток-«мишеней» вместе с паразитирующими в них возбудителями может наступить вследствие их распознавания Т-киллерами, специфически сенсибилизированных против микробных антигенов.
Другой механизм гибели зараженных клеток носит название антителозависимой цитотоксичности (АЗЦТ). Он заключается в распознавании микробных антигенов на мембране зараженной клетки-«мишени» антителами, адсорбированными на Fc-рецепторах NK-клеток или макрофагов. При этом цитотоксичность является результатом действия лизосомных ферментов и других продуктов секреции данных клеток.
В целом клеточные механизмы обеспечивают защиту организма против факультативно и облигатно внутриклеточных паразитов, что позволяет оценивать напряженность специфического иммунитета по результатам кожно-аллергической реакции. Этим же объясняется и тот факт, что наиболее эффективными для специфической профилактики таких инфекций являются вакцины из живых ослабленных микроорганизмов, активирующие клеточные механизмы иммунитета.
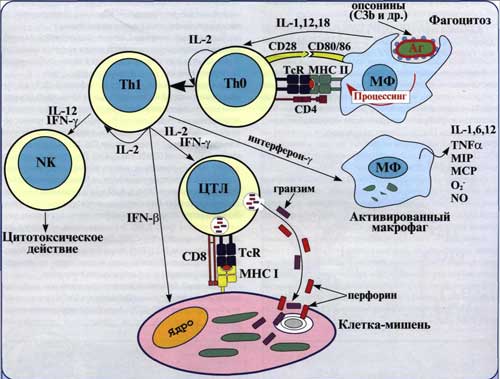
Рис. 2. Клеточный иммунный ответ опосредован активированными Т-хелперами макрофагами и другими фагоцитирующими клетками, а также цитотоксическими Т-лимфацитами.
Иммунологическая память
Иммунологическая память - способность организма отвечать на повторное введение антигена иммунной реакцией, характеризующейся большей силой и более быстрым развитием.
Клетки иммунологической памяти - долгоживущие Т- и В-лимфоциты, сохраняющие многие годы способность реагировать на повторное введение антигена, так как вырабатываются рецепторы к этому антигену. Иммунологическая память проявляется как ускоренный специфический ответ наповторноевведение антигена.
Иммунологическая память к антигенным компонентам окружающей среды лежит в основе аллергических заболеваний, а к резус-антигену (возникает при резус-несовместимости беременности) - в основе гемолитической болезни новорожденных. Феномен иммунологической памяти используется в практике вакцинации людей.
Иммунологическая толерантность
Иммунологическая толерантность - явление, противоположное иммунному ответу и иммунологической памяти, проявляющееся в том, что на введение антигена вместо выработки иммунитета в организме развивается ареактивность, инертность, отсутствие ответа на антиген.
Иммунный ответ против собственных тканей организма в нормальных условиях не развивается, т.е. иммунная система толерантна к подавляющему большинству Аг тканей организма (аутоантигены). Искусственная толерантность к чужеродным Аг может быть вызвана иммунизацией по определенной схеме (например, толерантность «низкой дозы» - дробное введение Аг в возрастающих количествах или толерантность «высокой дозы» - однократное введение Аг в высокой дозе).
 2015-05-26
2015-05-26 1929
1929
