Диаграммы состояния в графической форме показывают равновесный фазовый состав сплавов в зависимости от температуры и концентрации компонентов.
Общие закономерности существования фаз в равновесных условиях в математической форме выражаются правилом фаз Гиббса:
C=K-F+1,
где К - число компонентов, образующих систему; F - число фаз; С - число степеней свободы.
Компонентами называют вещества, образующие систему. Фаза - это однородная часть системы, отделенная от других частей (фаз) поверхностью раздела, при переходе через которую свойства вещества меняются скачком.
Под степенями свободы понимают внешние и внутренние факторы (температура, концентрация), которые можно изменять, не выводя систему из данного фазового состава. (Используйте правило фаз при ответе на вопросы 67, 68, 69, 70, 72).
При построении диаграмм состояния используют кривые охлаждения сплавов, полученные при термическом анализе. По точкам перегиба и температурных остановок, вызванных тепловым эффектом превращений, определяют температуры фазовых превращений.
Однокомпонентная диаграмма представляет собой температурную шкалу с нанесенными на нее точками фазовых превращений.
Межкомпонентная диаграмма помимо температурной оси (оси ординат), имеет ось концентраций (ось абсцисс). Один конец оси абсцисс соответствует чистому компоненту, например А, другой - В. Все промежуточные точки оси соответствуют сплавам с различным соотношением компонентов.
Трехкомпонентные диаграммы имеют вид трехгранной равносторонней призмы, в основании которой лежит концентрационный треугольник, а ребра являются температурными осями. Вершины концентрационного треугольника соответствуют чистым компонентам, стороны - концентрационным осям двойных систем, точки внутри треугольника - тройным сплавам. При определении концентрации компонентов в тройном сплаве через заданную точку (фигуративную точку) треугольника проводят линии, параллельные его сторонам. Отрезок линии, заключенный между фигуративной точкой и стороной треугольника, отнесенный к длине стороны, равен содержанию компонента (в долях единицы), которому соответствует вершина, противолежащая стороне.
Диаграмма, подобная представленной на рис. 24, называется диаграммой с неограниченной растворимостью компонентов в твердом состоянии. Линия диаграммы A'cВ' называется линией ликвидус. Выше этой линии все сплавы существуют в виде однофазного жидкого раствора (L). Линия A'fB' - линия солидус. Ниже нее все сплавы находятся в твердом состоянии (в данном случае в виде неограниченного твердого раствора α). Между линиями А'сВ' и А'fВ' сплавы имеют двухфазный состав (L + α).
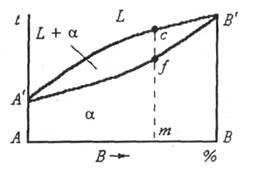
Рис. 24
Химический состав фаз и их относительное количество в сплаве при температуре соответствующей двухфазной области, определяют с помощью правила отрезков.
Чтобы определить химический состав фаз, нужно через заданную точку, характеризующую состояние сплава (фигуративную точку), провести коноду (конодой называется горизонтальная линия, лежащая в двухфазной области диаграммы и опирающаяся своими концами на фазовые границы). Проекции концов коноды на ось концентраций покажут состав соответствующих фаз. Отношение длины отрезка, заключенного между фигуративной точкой и одним из концов коноды, к длине всей коноды равно относительному количеству фазы, на границу с которой опирается второй конец коноды. (Используйте правило отрезков при ответе на вопросы 65, 66).
На рис. 30 представлена диаграмма с отсутствием растворимости компонентов в твердом состоянии. Здесь линия АСВ - ликвидус, DCE - солидус. Кристаллизация всех сплавов этой системы заканчивается на линии DCE эвтектическим превращением остатка жидкой фазы в механическую смесь кристаллов компонентов А и В. Образовавшаяся таким образом смесь называется эвтектической или эвтектикой. Сплав, кристаллизация которого начинается непосредственно с эвтектического превращения (в данном случае сплав, фигуративная линия котоpoго проходит через точку С), называется эвтектическим.
На рис. 31 представлена диаграмма с ограниченной растворимостью компонентов в твердом состоянии (диаграмма с эвтектикой). Помимо линий ликвидус и солидус (АСВ и ADCEB) диаграмма содержит линии DF и EG предельной растворимости компонента В в твердом растворе α (А(В)) и компонента А в твердом растворе β (В(А)), соответственно. Кристаллизация сплава "с" начинается после пересечения линии ликвидус с выделения кристаллов твердого раствора β. Затем при пересечении линии DCE (линии эвтектики) образуется эвтектическая смесь из твердых растворов α и β. При дальнейшем охлаждении, в связи с уменьшением растворимости компонента А в В (А) выделяются кристаллы твердого раствора и, богатого компонентом А. В конечном счете структура сплава представлена первичными кристаллами β, эвтектикой (α + β) и вторичными кристаллами α.
На рис. 33, В представлена диаграмма с ограниченной растворимостью компонентов в твердом состоянии (диаграмма с перитектикой). Перитектическое превращение протекает на линии CDE. Существо его состоит в том, что кристаллы твердого раствора α, выделившиеся при охлаждении ниже линии АЕ, взаимодействуют с остатком жидкой фазы, следствием чего является образование твердого раствора β.
Диаграммы с устойчивым химическим соединением имеют вид двух или нескольких диаграмм, приложенных друг к другу по фигуративной линии химического соединения. Диаграммы с неустойчивым химическим соединением внешне напоминают диаграмму с перитектикой, однако вместо твердого раствора здесь образуется химическое соединение (границы твердого раствора как бы стягиваются в одну вертикальную линию).
Вид диаграмм состояния, в которых компоненты испытывают полиморфные превращения, зависит от характера взаимодействия аллотропических модификаций компонентов. В ряде случаев они напоминают обычные диаграммы, расположенные этажами. Нередко в таких системах встречаются превращения, сходные по виду с эвтектическим, но с распадом не жидкости, а твердого раствора Превращение подобного типа, в отличие от эвтектического, называют эвтектоидным.
 2015-05-26
2015-05-26 1059
1059








