Растворение твердых электролитов прекращается, когда образуется насыщенный раствор, в котором устанавливается гетерогенное равновесие между твердой фазой и перешедшими в раствор ионами. Например:
CaSO4 (т)  Ca2+(р-р) + SO42–(р-р)
Ca2+(р-р) + SO42–(р-р)
В выражение константы этого гетерогенного равновесия не входит концентрация твердой фазы (см. особенности закона действия масс для гетерогенных процессов): K= [Ca2+][SO42–].
В насыщенном растворе твердого электролита произведение концентраций его ионов есть величина постоянная при данной температуре. Она называется произведением растворимости. ПР(CaSO4) = [Ca2+][SO42–].
Если молекула электролита содержит несколько одинаковых ионов, то концентрации этих ионов, согласно закону действия масс, должны быть возведены в соответствующие степени. Например: PbI2  Pb2+ + 2 I–, ПР(PbI2) = [Pb2+][I–]2.
Pb2+ + 2 I–, ПР(PbI2) = [Pb2+][I–]2.
Зная произведения растворимости, можно решать вопросы, связанные с образованием или растворением осадков при химических реакциях. Например, пусть диссоциация соли АВ происходит на два иона:
АВ  А+ + В–
А+ + В–
Обозначив растворимость через s (моль/л), получим [A+]=[B–]= s, ПР=[A+][B–]= s 2. На практике чаще возникает обратная задача определения растворимости. Для соли, диссоциирующей на два иона, 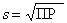 . Значения ПР можно найти в химических справочниках. Например, ПР(AgCl)=1,8·10–10, ПР(AgBr)=6·10–13, ПР(BaSO4)=1,1·10–10, ПР(HgS)=10–52. Если соль имеет общую формулу AB2, то она диссоциирует по уравнению:
. Значения ПР можно найти в химических справочниках. Например, ПР(AgCl)=1,8·10–10, ПР(AgBr)=6·10–13, ПР(BaSO4)=1,1·10–10, ПР(HgS)=10–52. Если соль имеет общую формулу AB2, то она диссоциирует по уравнению:
AB2  A2+ + 2 B–
A2+ + 2 B–
В этом случае [A2+]= s, [B–] =2 s, ПР=[A2+][B–]2 = s · (2 s)2 = 4 s 3, 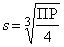 .
.
Если фактическое произведение концентраций (ПС) ионов в некотором растворе превышает значение произведения растворимости, т.е. ПС>ПР, то раствор является пересыщенным, и из него выпадает осадок. Условие растворения осадка (ненасыщенности раствора): ПС<ПР. Оба процесса идут с одинаковой скоростью, и система приходит в состояние равновесия при ПС=ПР (насыщенный раствор).
 2015-05-26
2015-05-26 400
400







