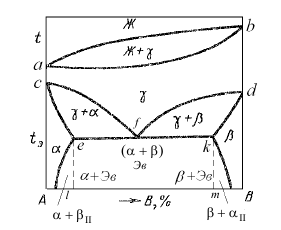
В соответствии с данной диаграммой состояния (рис. 3.7) ком-
поненты А и В в высокотемпературной области имеют одинаковый
тип кристаллической решетки и неограниченно растворимы друг
в друге, образуя твердые растворы .
В точках а и b происходит кристаллизация компонентов А и В
с кристаллическими решетками A и B соответственно. При темпе-
ратурах, соответствующих точкам с и d, происходит изменение кри-
сталлических решеток компонентов А и В и превращение их в моди-
фикации A и B. Соответственно новые образующиеся твердые
растворы B в A обозначим и A в B – . Точка е показывает
максимальную растворимость компонента B в A, а точка k соот-
ветственно компонента A в B.
Вследствие полиморфных превращений компонентов А и В при
понижении температуры ниже линий cf и df начинается распад
- фазы с образованием -фазы для сплавов, расположенных левее
точки f, и -фазы, для сплавов, находящихся правее точки f. Для
сплавов состава левее точки e на линии ce процесс распада -фазы за-
канчивается и образуется однофазный -сплав. Аналогично, для
сплавов правее точки k ниже линии dk образуется однофазный
- сплав.
Состав -фазы при кристаллизации изменяется в соответствии
с линией ce, -фазы – с линией dk, а -фазы – с линией cfd. В точке f
возникает нонвариантное состояние, т. к. при распаде -фазы одно-
временно кристаллизуются две фазы и , происходит эвтектоид-
ное превращение
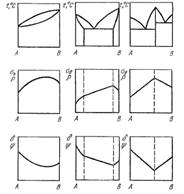
17) Свойства сплавов в значительной степени определяются фазо-
вым составом, о котором можно судить по диаграммам состояния
1. При образовании твердых растворов свойства сплавов изменя-
ются по криволинейной зависимости, причем многие из них могут су-
щественно превосходить свойства исходных компонентов (в первую
очередь электросопротивление). Поэтому распад твердых растворов на
две и более фазы приводит к увеличению электропроводности.
2. При образовании механических смесей свойства сплавов из-
меняются по линейному закону (аддитивно). Значения свойств нахо-
дятся в интервале между свойствами чистых компонентов.
3. В сплавах с ограниченной растворимостью при концентраци-
ях, cоответствующих однофазному твердому раствору, изменяются
свойства по криволинейному закону, а в двухфазной области – по ли-
нейному. Крайние точки на прямой соответствуют свойствам пре-
дельно насыщенных твердых растворов.
4. При образовании химических соединений на диаграмме кон-
центрация–свойства при соответствующей концентрации наблюдает-
ся перелом, т. к. химические соединения обладают индивидуальными
свойствами, отличными от свойств исходных составляющих.
18)
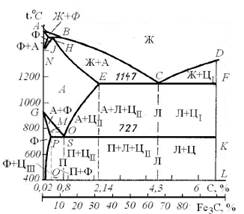
Диаграмма состояния Fe–Fe3C (рис. 4.2) характеризует фазовый
состав и структуру в системе с концентрацией от чистого железа до
цементита, содержащего 6,67 % С. По оси абсцисс диаграмма имеет
две шкалы, показывающих содержание углерода в сплаве и количест-
во цементита
Точки А и D характеризуют температуру плавления железа
и цементита соответственно. Точки N и G – температуры полиморф-
ных превращений железа. Точки Н и Р характеризуют максимальную
растворимость углерода в ОЦК решетке железа в высокотемператур-
ной и низкотемпературной областях. Точка Е определяет максималь-
ную растворимость углерода в железе с ГЦК решеткой.
Фазовые превращения в системе Fe–Fe3C происходят как при
затвердевании из жидкого агрегатного состояния, так и в твердом аг-
регатном состоянии. Первичная кристаллизация идет в областях меж-
ду линиями ликвидус (ABCD) и солидус (AHJECF). Вторичная кри-
сталлизация в твердом агрегатном состоянии является следствием
полиморфного превращения железа и изменения растворимости угле-
рода в железе с изменением температуры.
На линии ликвидус начинается кристаллизация из расплава со-
ответственно на участке АВ – феррита (Ф), на участке ВС – аустени-
та (А) и на участке СD – цементита первичного (ЦI). На линиях АН
и JЕ завершается кристаллизация Ф и аустенита из жидкой фазы.
Для диаграммы Fe–Fe3C характерны три изотермических пре-
вращения:
– перитектическое на линии HJВ при температуре 1499 °С
ФН + ЖB АJ;
– эвтектическое на линии ECF при температуре 1147 °С
ЖC АE + ЦF;
– эвтектоидное на линии PSK при температуре 727 °С
19)
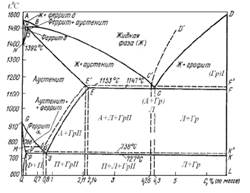
Диаграмма состояния железо–графит (Fe–C) называется диа-
граммой стабильного равновесия, т. к. при кристаллизации из жидкой
фазы на линии CD образуется стабильная модификация углерода –
графит. Образование графита может происходить также в результате
вторичных превращений и при распаде предварительно образовавше-
гося цементита. Процесс образования в системе графита называется
графитизацией.
Диаграмма стабильного равновесия системы Fe–C приведена на
рис. 4.6.
Для удобства сравнения диаграмма Fe–C, изображенная пунк-
тирными линиями, наложена на диаграмму Fe–Fe3C. На рис. 4.6 вид-
но, что в системе Fe–C происходит изменение точек эвтектического и
эвтектоидного превращений. Эвтектика образуется при температуре
1153 °С при содержании углерода в жидкой фазе 4,26 % и состоит из
аустенита и графита. В диапазоне температур 1153…738 °С вследст-
вие снижения растворимости углерода в -Fe образуется графит вто-
ричный. Максимальная растворимость углерода в -Fe в точке E' со-
ставляет 2,11 %. Эвтектоидное превращение в системе железо–графит
происходит при температуре 738 °С при содержании углерода в ау-
стените 0,7 %. Эвтектоид состоит из феррита и графита вторичного.
Кристаллы графита имеют форму лепестков, выходящих из од-
ного центра. При этом кристаллы вторичного графита выделяются на
лепестках первичного и эвтектического графита.
Кристаллизация в соответствии с диаграммой Fe–C возможна
лишь при весьма медленном охлаждении и при введении в железоуг-
леродистые сплавы графитизирующих добавок, в частности, кремния.
20) С увеличением количества углерода
увеличивается твердость, предел текучести, предел прочности сталей,
снижается пластичность, ударная вязкость, плотность
Пределы прочности и текучести возрастают при увеличении ко-
личества углерода в стали до 1,0 %, после чего начинается их сниже-
ние. Причиной этому является образование цементной сетки вокруг
зерен перлита.
Кремний дегазирует сталь, увеличивая плотность отливки,
растворяясь в феррите повышает предел текучести стали, снижает
способность к вытяжке и холодной высадке
Марганец связывает се-
ру, образуя сульфид марганца MnS в виде отдельных частиц. Раство-
ряясь в феррите, марганец повышает предел прочности, не снижая
пластичности, снижает склонность сталей к красноломкости, т. е.
хрупкости при повышенных температурах.
Сера и фосфор являются вредными примесями, попадающими
в стали из чугуна при их производстве. Сера, взаимодействуя с желе-
зом, образует сульфид железа FeS. Сульфидные включения сущест-
венно снижают механические свойства, особенно ударную вязкость
и пластичность, а также предел выносливости сталей, ухудшают их
коррозийную стойкость и свариваемость.
Фосфор, соединяясь с железом, образует фосфиды железа Fe3P,
которые располагаются по границам зерен, повышая порог хладно-
ломкости и снижая коррозийную стойкость сталей. Фосфор, раство-
ряясь в феррите и аустените, искажает кристаллическую решетку, по-
нижает пластичность, ударную вязкость, увеличивая предел
прочности и предел текучести сталей
Азот и кислород, образуя соответственно нитриды и оксиды,
располагающиеся по границам зерен, снижают пластичность, удар-
ную вязкость, предел выносливости, повышают порог хладноломко-
сти, ухудшают обрабатываемость сталей методами пластического де-
формирования.
Водород охрупчивает сталь, способствует образованию флоке-
нов (трещин овальной формы), холодных трещин при сварке.
21Легирующие элементы вводятся в стали для управления процес-
сами кристаллизации, изменения физико-механических и технологи-
ческих свойств сплавов. При введении в стали легирующих элементов
они могут образовывать следующие фазы:
– твердые растворы;
– легированный цементит или собственные карбиды;
– интерметаллидные соединения.
Все легирующие элементы, за исключением углерода, водорода,
азота и бора (отчасти), образуют с железом твердые растворы заме-
щения. Растворяясь в железе, они влияют на положение характерных
точек на диаграмме состояния Fe–Fe3C, определяющих области суще-
ствования -Fe и -Fe, температур эвтектических и эвтектоидных
превращений.
вращений.
По влиянию на температурную область существования поли-
морфных модификаций железа легирующие элементы можно разде-
лить на две группы. К первой группе относятся элементы, понижаю-
щие точку А3 и повышающие точку А4. К таким элементам относятся:
никель, марганец, медь, кобальт, азот
Ко второй группе относятся легирующие элементы, понижаю-
щие точку А4 и повышающие точку А3. В эту группу входят: хром,
вольфрам, молибден, ванадий, кремний, алюминий и др
ытывают фазовых превращений при нагреве и охлаждении.
По отношению к углероду легирующие элементы можно разде-
лить на две группы:
– графитизирующие;
– карбидообразующие.
К первой группе относятся легирующие элементы: кремний, ни-
кель, медь, алюминий, кобальт, которые не образуют карбидов, а на-
ходятся в твердых растворах.
К карбидообразующим элементам относятся Fe, Mn, Cr, Mo, W,
V, Nb, Zr, Ti, которые приведены здесь по возрастающей степени
сродства к углероду и у
стойчивости карбидов.
 2015-05-26
2015-05-26 1039
1039
