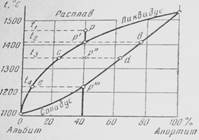
 Для того чтобы понять причины образования структур магматических пород, необходимо познакомиться с главнейшими типами термических диаграмм, иллюстрирующими процессы кристаллизации силикатных расплавов. Для построения простейших диаграмм кристаллизации пользуются двумя взаимно перпендикулярными осями, из которых ось ординат — температурная шкала, ось абсцисс — шкала составов. Кривая на диаграмме, отражающая начало кристаллизации и отвечающая составу расплава, называется ликвидус (жидкий); кривая, обозначающая конец кристаллизации и определяющая состав кристаллов, называется солидус (твердый). Линии ликвидуса и солидуса делят плоскость диаграммы на отдельные поля, в пределах которых устойчивы определенные фазы — физически однородные части системы (расплав, кристаллы). Положение любой точки в пределах диаграммы определяется составом и температурой и отражает состояние системы — ее фазы и их относительные количества.
Для того чтобы понять причины образования структур магматических пород, необходимо познакомиться с главнейшими типами термических диаграмм, иллюстрирующими процессы кристаллизации силикатных расплавов. Для построения простейших диаграмм кристаллизации пользуются двумя взаимно перпендикулярными осями, из которых ось ординат — температурная шкала, ось абсцисс — шкала составов. Кривая на диаграмме, отражающая начало кристаллизации и отвечающая составу расплава, называется ликвидус (жидкий); кривая, обозначающая конец кристаллизации и определяющая состав кристаллов, называется солидус (твердый). Линии ликвидуса и солидуса делят плоскость диаграммы на отдельные поля, в пределах которых устойчивы определенные фазы — физически однородные части системы (расплав, кристаллы). Положение любой точки в пределах диаграммы определяется составом и температурой и отражает состояние системы — ее фазы и их относительные количества.
При понижении температуры расплав будет взаимодействовать с выделившимися кристаллами и вся система начнет смещаться влево по линиям ликвидуса и солидуса, так как анортит постепенно удаляется из системы, а остаточная жидкость соответственно обогащается альбитом.
|
|
|
 Кристаллы и расплав в течение всего процесса кристаллизации непрерывно взаимодействуют друг с другом с одновременным изменением состава и кристаллов и расплава в направлении обогащения менее тугоплавким компонентом (в данном примере — альбитом).Первые кристаллы, выделившиеся из расплава, всегда богаче тугоплавким компонентом, чем исходный расплав; последние кристаллы отвечают составу исходного расплава. Состав кристаллов, выделившихся в начальную и конечную стадии кристаллизации, а также температурный интервал процесса кристаллизации зависят только от состава исходного расплава. В природных условиях при медленном спокойном процессе кристаллизации реакция между расплавом и твердой фазой доходит до конца с образованием однородных кристаллов, соответствующих составу исходного расплава. При нарушении равновесия за счет скачкообразного изменения температуры или за счет изменения состава расплава (вследствие притока нового вещества, удаления ранее образовавшихся кристаллов или других причин) равновесие нарушается, выделяющиеся кристаллы не успевают прореагировать с расплавом, что приводит к появлению зональных кристаллов. Состав зональных кристаллов меняется от зоны к зоне, четко свидетельствуя о последовательности выделения минеральных фаз. При нормально направленном ходе кристаллизации центральные части зональных кристаллов обычно обогащены более тугоплавким компонентом, в данном случае — анортитом, внешние зоны — более легкоплавким — альбитом. Зональные плагиоклазы характерны для пород, кристаллизовавшихся в гипабиссальных или поверхностных условиях, менее равновесных, чем глубинные условия кристаллизации. В плагиоклазах основного и среднего состава зональность выражена резче, чем в кислых плагиоклазах.
Кристаллы и расплав в течение всего процесса кристаллизации непрерывно взаимодействуют друг с другом с одновременным изменением состава и кристаллов и расплава в направлении обогащения менее тугоплавким компонентом (в данном примере — альбитом).Первые кристаллы, выделившиеся из расплава, всегда богаче тугоплавким компонентом, чем исходный расплав; последние кристаллы отвечают составу исходного расплава. Состав кристаллов, выделившихся в начальную и конечную стадии кристаллизации, а также температурный интервал процесса кристаллизации зависят только от состава исходного расплава. В природных условиях при медленном спокойном процессе кристаллизации реакция между расплавом и твердой фазой доходит до конца с образованием однородных кристаллов, соответствующих составу исходного расплава. При нарушении равновесия за счет скачкообразного изменения температуры или за счет изменения состава расплава (вследствие притока нового вещества, удаления ранее образовавшихся кристаллов или других причин) равновесие нарушается, выделяющиеся кристаллы не успевают прореагировать с расплавом, что приводит к появлению зональных кристаллов. Состав зональных кристаллов меняется от зоны к зоне, четко свидетельствуя о последовательности выделения минеральных фаз. При нормально направленном ходе кристаллизации центральные части зональных кристаллов обычно обогащены более тугоплавким компонентом, в данном случае — анортитом, внешние зоны — более легкоплавким — альбитом. Зональные плагиоклазы характерны для пород, кристаллизовавшихся в гипабиссальных или поверхностных условиях, менее равновесных, чем глубинные условия кристаллизации. В плагиоклазах основного и среднего состава зональность выражена резче, чем в кислых плагиоклазах.
|
|
|
В случае резкого понижения температуры, что имеет место при вулканических извержениях, могут образоваться кристаллы любого промежуточного состава.
Последовательность выделения главнейших породообразующих минералов можно представить в виде двух реакционных рядов. Один ряд непрерывно-реакционный, свойственный полевым шпатам; другой ряд прерывно-реакционный, характеризующий железо-магнезиальные силикаты. В каждом из рядов вышестоящий минерал, реагируя с жидкой фазой, дает нижестоящий минерал. Стрелками показано направление процесса кристаллизации. Порядок выделения минералов в различных рядах зависит от состава расплава. Каждый минерал данного ряда с соответствующим минералом параллельного ряда образует эвтектику.
Реакционные ряды включают важнейшие породообразующие минералы и объясняют порядок их выделения и парагенезис. Из схемы Боуэна видно, что ассоциация оливинов, пироксенов и основных плагиоклазов обычна; все эти минералы относятся к начальной высокотемпературной стадии кристаллизации. Наоборот, кислые плагиоклазы, натриево-калиевые полевые шпаты и кварц вместе с оливином и пироксеном встречаться не должны, поскольку эти минералы принадлежат к крайним членам реакционных рядов и т. д.
2. Химические потенциалы, их характеристики и роль в процессах экзогенного минералообразования. Химические потенциалы. Потенциал термодинамический — термодинамическая функция состояния, имеющая размерность энергии и являющаяся в определенных условиях критерием равновесности и направления процесса в системе. В химических реакциях одновременно действуют два противоположных фактора — энтропийный (T Δ S) и энтальпийный (Δ H). Суммарный эффект этих противоположных факторов в процессах, протекающих при постоянном давлении и температуре, определяет изменение энергии Гиббса или свободная энергия (G):
ΔG = ΔH-Т ΔS.Характер изменения энергии Гиббса позволяет судить о принципиальной возможности осуществления процесса. При Δ G < 0 процесс может протекать, при Δ G > 0 процесс протекать не может (иными словами, если энергия Гиббса в исходном состоянии системы больше, чем в конечном, то процесс принципиально может протекать, если наоборот — то не может). Если же Δ G = 0, то система находится в состоянии хим. равновесия.
Потенциал окислительно-восстановительный (Eh) — мера интенсивности присоединения или отдачи электронов в окислительно-восстановительной реакции, представленной электродвижущей силой, выражаемой в милливольтах (мв). Этот потенциал служит мерой окислительной или восстановительной способности среды; он измеряется при помощи специальных приборов и обозн. через Eh. Величина Eh зависит от изменения в растворе концентраций Н+ и ОН~ ионов (т. е. от степени кислотности или щелочности среды), от соотношения концентрации окисляющего и восстанавливающегося ионов и от температуры. В частности, при добавлении в раствор кислоты или щелочи его интенсивность окисления или восстановления значительно меняется, т. е. Eh зависит от рН. Следовательно, при определении Eh нужно одновременно определить и рН. Величины применяются в геологии, литологии, гидрогеологии, гл. обр. для выяснения условий осадконакопления, характеристики вод, особенно вод нефтяных м-ний и для др. целей. Попытки определения Eh в твердых г. п., даже с естественной влажностью, еще не дали удовлетворительных результатов. Eh, при котором концентрация окислителя равна концентрации восстановителя (напр., Fe2+ = Fe3+), называется стандартным и обозн. как Ео. В качестве показателя окислительно-восстановительной системы нередко применяют значение гН (редокс) или гН2. Значение гН — это расчетная величина окислительно-восстановительного (ОВ) потенциала, учитывающая влияние рН на ОВ систему. Для перехода от одного значения к другому существует Eh + постоянная величина для системы уравнение rH= при t — 30 °С. С повышением гН парциальное давление водорода в системе уменьшается, а ее окисленность увеличивается. С окислительно-востановительным потенциалом связаны разные геохимические барьеры на которых идет накопление различных видов полезного ископаемого. Геохимические барьеры подразделяются на два типа природные и техногенные. Они разделены на 4 класса: физико-химический, биохимический, механический и социальный.
|
|
|
3. Типоморфизм минералов. Понятие, основные особенности проявления и роль в поисковой минералогии.Типоморфизм минералов, генетическая обусловленность характерных свойств и признаков минералов. Типоморфные свойства и признаки минералов непосредственно характеризуют условия их образования (могут служить показателями Т и Р образования) и особенности минералообразующей среды (вариации щёлочности - кислотности этой среды, парциального давления газов, состава растворов или расплавов и др.). К типоморфным свойствам относят: морфологические особенности выделений минералов (габитус кристаллов, двойники, характер агрегатов и др.); вариации химического состава минерала и содержания в нём изоморфных элементов примесей; некоторые физические свойства (плотность, микротвёрдость, отражательная способность, люминесценция, электрические, магнитные и др.); структурные особенности (степень упорядоченности структур минералов). Наибольший интерес представляют исследования типоморфизм минералов, образующихся в широком диапазоне температур и давлений и присутствующих в разных стадиях формирования месторождений. Типоморфизм минералов используют для решения многих практических задач (при оценке степени рудоносности горных пород, поисках рудных месторождений некоторых типов, определении промышленного значения рудопроявлений, при поиске скрытых рудных тел и т. д.). Понятие о Типоморфизм минералов в современном его значении введено в минералогию А. Е. Ферсманом. Сходство геолого-структурных условий формирования группы месторождений при подобии их главных геохимических черт определяет появление на каждом из таких месторождений однотипных минеральных ассоциаций и близких по составу парагенетических ассоциаций, типоморфных для месторождений данной формации. Как правило, масштабы проявления и последовательность развития во времени процесса рудогенеза на таких месторождениях также подобны. То есть, по типоморфным минеральным ассоциациям можно установить формационную принадлежность месторождения, а в ряде случаев оценить его предполагаемые масштабы и особенности пространственного расположения рудных тел. Все это определяет важное теоретическое и прикладное значение углубленного изучения типоморфных минеральных ассоциаций для геологии рудных месторождений и для совершенствования металлогенических исследований в целом. Основной метод выявления типоморфных минеральных ассоциаций – последовательное накопление, обработка и осмысливание фактического материала о минеральном составе и текстурно-структурных особенностях природных объектов – г. п, руд, минералов, относящихся к различным формациям, фациям и фациальным разновидностям.
|
|
|
Классификации подземных вод по минерализации, компонентному составу (Алекина, Сулина), жесткости и др. Дайте название воды по минерализации, водородному показателю и преобладающим компонентам (химанализ прилагается).
| рН | М, г/л | Основной компонентный состав, мг/л, мг-экв/л, %-мг-экв | ||||||
| Na + + K+ | Ca ++ | Mg ++ | Cl- | SO4-- | CO3-- | HCO3- | ||
| 8,2 | 43,598 | 10801,49 | 4000,00 | 1105,50 | 25164,90 | 2312,20 | - | 213,50 |
| 469,63 | 200,00 | 90,91 | 708,87 | 48,17 | - | 3,50 | ||
| 30,88 | 13,15 | 5,97 | 46,60 | 3,17 | - | 0,23 |
5. Пластовое тело бокситов установлено в базальной части нижнекаменноугольной терригенной толщи. Форма тела, по геоморфологическим признакам, неправильная, слабо удлиненная в направлении с северо-запада к юго-востоку, Мощность тела по единственной вскрывшей его скважине составила 2,6 м. Оконтурить рудное тело по площади и мощности. Составить схему оконтуривания в масштабе. Мощность четвертичных отложений 45 м, перекрывающих глинистых отложений С1 – 15 м.
6. Геохимия щелочных минералов (Na, K, Li) в магматическом процессе. Литий по геохимическим свойствам относится к крупноионным литофильным элементам, в числе которых калий, рубидий и цезий. Содержание лития в верхней континентальной коре составляет 21 г/т.Основные минералы лития — слюда лепидолит — KLi1,5Al1,5[Si3AlO10] (F, OH)2 и пироксен сподумен — LiAl [Si2O6]. Когда литий не образует самостоятельных минералов, он изоморфно замещает калий в широко распространенных породообразующих минералах.Месторождения лития приурочены к редкометалльным гранитным интрузиям, в связи с которыми развиваются литиеносные пегматиты или гидротермальные комплексные месторождения, содержащие также олово, вольфрам, висмут и другие металлы. Стоит особо отметить специфические породы онгониты — граниты с магматическим топазом, высоким содержанием фтора и воды, и исключительно высокими концентрациями различных редких элементов, в том числе и лития.
Калий – мягкий, серебристо-белый, легкий металл, бурно реагирует с водой. Плотность 0,8629 г/см3. Температура плавления 63,51оС. Хранят калий в бензине или в керосине. Кларк калия 2,5% - по распространенности в земной коре занимает 7-е место после O, Si, Al, Fe, Ca, Na. Содержание К в ультраосновных породах – 0,03, в основных – 0,83, в средних – 2,3, в кислых – 3,34, в осадочных – 3,34%. Больше всего калия в щелочных породах агпаитового ряда. Калий входит в состав очень многих минералов, но его главные промышленные минералы – сильвин KCl, карналлит KMgCl3×6H2O, калиевая селитра KNO3, полигалит K2MgCa2[SO4]4×2H2O, каинит KMg[SO4]Cl×3H2O. Эти минералы образуются в конечную фазу галогенеза, после выпадения в осадок основной массы галита. Содержание калия в морской воде 380 мг/л. Такое низкое (по сравнению с натри-ем), содержание калия объясняется его вхождением в состав глинистых минералов –иллитов, входит калий в состав глауконитов, потребляется он микроорганизмами (он входит в состав тканей).
Натрий. Плотность 0,968 г/см3. Температура плавления 97,86оС. Для натрия типичен несовершенный изовалентный изоморфизм с K+ и Li+. Кларк натрия 2,5%. После O, Si, Al, Fe, Ca натрий занимает шестое место по распространенности в земной коре. В ультраосновных породах его 0,57, в основных- 1,94, в средних – 3,0, в кислых – 2,7, в осадочных – 0,66% (в глинах – 0,96, в песчаниках – 0,33, в карбонатах – 0,04%). В морской воде натрия много – 10,5 г/л. Натрий входит в состав более 200 минералов, но основной его минерал – это галит - NaCl. Применяется натрий во многих производствах, например в качестве теплоносителя в атомных реакторах. Необходимый для жизни элемент – суточная потребность человека в натрии – от 2 до 15 г.
 2015-05-30
2015-05-30 1180
1180








