Атомы каждого элемента всегда имеют одинаковое число протонов или электронов (атомный номер), однако в некоторых случаях число нейтронов в атоме может быть разным (атомная масса).
Например, атом водорода может существовать в трех формах.
| Атомный номер | Атомная масса | ||
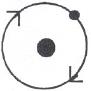 | Водород | ||
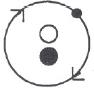 | Дейтерий | ||
 | Тритий |
Все эти три формы атомов водорода имеют по одному протону и электрону, но в дейтерии количество нейтронов равно двум, а в тритии – трем.
Такие формы элементов называются изотопами. Они похожи на основной элемент и имеют похожие химические свойства. Отличие заключается в другой атомной массе.
Изотопы водорода стабильны и существуют в естественных условиях.
Изотопы некоторых других элементов, например, кобальта, нестабильны и не могут неопределенно долго существовать в естественных условиях. Такие изотопы называются нестабильными или радиоактивными. Такие нестабильные изотопы стремятся к стабильности, и будут подвергаться определенным изменениям для того, чтобы образовать более стабильную форму. При этом возможно превращение изотопа одного элемента в совершенно другой элемент. При этом они в той или иной форме испускают излучение. Это явление называется радиоактивным распадом.
 2015-05-30
2015-05-30 1074
1074








