Иммуноглобулины в любом организме представлены чрезвычайно разнообразными по структуре, специфичности и функциям макромолекулами. Физические, антигенные и функциональные различия между константными областями тяжелых цепей определяют у всех млекопитающих и человека наличие 5 классов иммуноглобулинов: IgG, IgM, IgA, IgD, IgE (Рис. 5-9; 5-10). Небольшие вариации в С-областях молекул одного класса определяют подклассы антител. У человека известно 4 подкласса IgG: IgG1, IgG2, IgG3, IgG4 и 2 подкласса IgA: IgA1 и IgA2. Подклассы IgG различаются между собой числом дисульфидных мостиков, соединяющих Н- и L-цепи и аминокислотной последовательностью в шарнирных участках иммуноглобулинов. Различия между подклассами IgA сводятся к числу и расположению дисульфидных мостиков и к взаимному расположению Н- и L-цепей. Изучение иммуноглобулинов показало, что отдельные классы и подклассы антител несут характерные только для данного класса или подкласса антигенные детерминанты, получившие название изоти-пических детерминант (Рис.5-11). Наличие изотипических детерминант позволяет иммунологически отличать классы и подклассы иммуноглобулинов друг от друга.
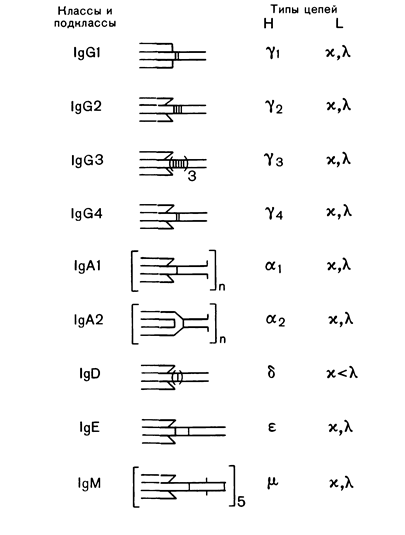
Р и с. 5-9. Классы и подклассы иммуноглобулилов человека.
Кроме изотипических детерминант иммуноглобулиновые молекулы несут аллотипические детерминанты (Рис.5-11).Аллотипические маркеры (ангигенные детерминанты) позволяют иммуноглобулины одного человека (например IgG) отличить от иммуноглобулинов другого человека (IgG).
Иммуноглобулиновые молекулы также чрезвычайно разнообразны по строению их антигенсвязывающей области (V-региону), которая определяет специфичность антитела. Разнообразие антител по специфичности превышает 108. В антигенсвязывающей области антитела располагаются как паратопы, так и идиотопы (Рис. 5-11а).
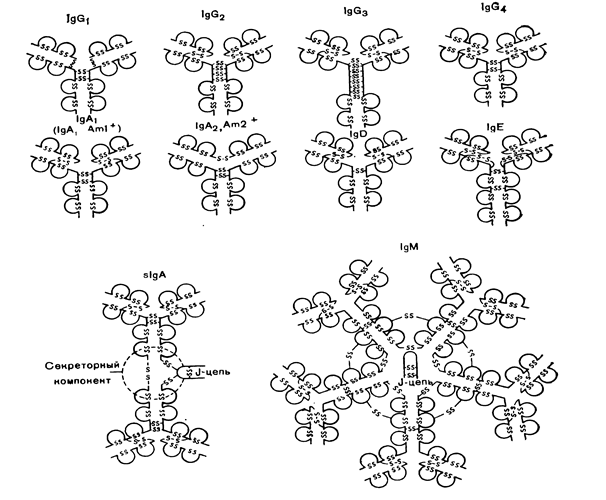
Р и с. 5-10. Структура иммуноглобулинов.
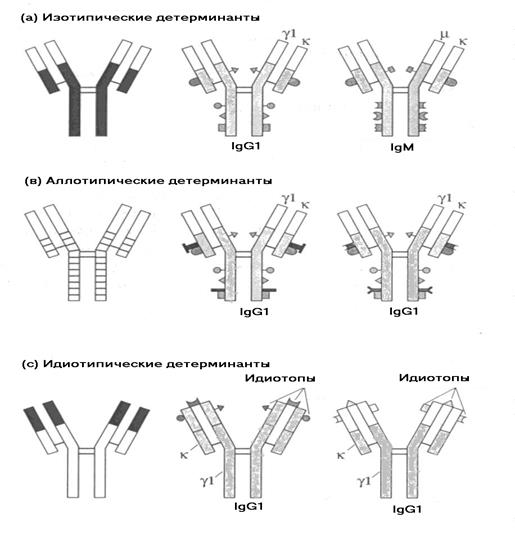
Р и с. 5-11. Антигенные детерминанты иммуноглобулинов.
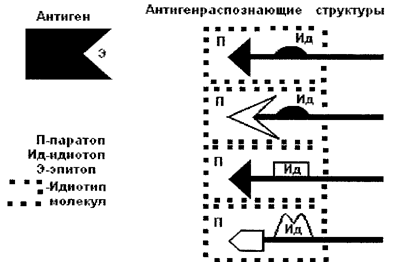
Р и с. 5-11а. Идиотипы антиген-распознающих молекул.
Функциональная н физико-химическая характеристика отдельных классов иммуноглобулинов
Основные физико-химические и биологические свойства иммуноглобулинов человека представлены в табл. 5-1.
Т а б л и ц а 5-1. Основные характеристики иммуноглобулинов человека.
| Свойство | IgM | IgG | IgA | IgD | IgE |
| Молекулярная форма | пентамер | мономер | мономер, димер, и т.д. | мономер | мономер |
| Обозначения: | |||||
| Н-цепи | m | g | a | d | e |
| L-цепи | k или l | k или l | k или l | k или l | k или l |
| Молекулярная формула | (k2m2)5 (l2m2)5 | k2g2 l2g2 | (k2a2)n (l2a2)n | k2d2 l2d2 | k2e2 l2e2 |
| Дополнительные цепи | J-цепь | – | J-цепь, секреторный компонент | – | – |
| Подклассы | IgGl,IgG2, IgG3, IgG4 | IgAl, IgA2 | |||
| Подклассы Н-цепей | – | gl, g2,g3,g4 | a1, a2 | – | – |
| Аллотипы Н-цепей | Мm(2) | Gm (ок. 20) | Аm(2) | – | – |
| Количество доменов Н-цепи | |||||
| Молекулярная массса | 950 000 | 150 000 | 160 000 | 175 000 | 190 000 |
| Валентность антител | 5 или 10 | ? | ? | ||
| Коэффициент седиментации (S) | 19S | 6,6S | 7S, 9S, 11S, 14S | 7S | 8S |
| Содержание углеводов (%) | |||||
| Концентрация в сыворотке, г/л | 0,5 – 2,0 | 12,0 – 14,0 | 1,8 – 2,1 | 0,4 | 0,0025 |
| Процент от общего количества | 5-10 | 75-85 | 7-15 | 0,3 | 0,003 |
| Период полураспада (дни) | 5,1 | 5,8 | 2,8 | 2,5 | |
| Скорость синтеза (мг/кг в день) | 6,7 | 0,4 | 0,016 | ||
| Парапротеинемия | макрогло- булинемия | миелома | миелома | миелома | миелома |
Продолжение таблицы 5-1.
| Свойство | IgM | IgG | IgA | IgD | IgE |
| Агглютинирующая активность | – | – | – | ||
| Фиксация комплемента | + | +(IgGl, 2,3) | – | – | – |
| Активация комплемента(альтернативный путь) | – | +(IgG4) | +(IgAl,2) | + | – |
| Цитофильность к: | |||||
| макрофагам, | – | + | – | – | – |
| лимфоцитам, | – | + | – | – | + |
| К-клеткам, | + | + | – | – | – |
| нейтрофилам, | – | + | + | – | – |
| Моноцитам | – | + | – | – | – |
| Тучным клеткам | – | + | – | – | + |
| Другие биологические свойства | первичный иммунный ответ | вторичный иммунный ответ; перенос через плаценту | характерные антитела в секретах | основная молекула поверхности лимфоцитов | гомоцито-тропные антитела; анафилаксия; аллергия |
IgG представляют собой мономер, имеет у-образную форму, мол. массу 150 000, двухвалентен. Концентрация его в сыворотке здоровых людей составляет в среднем 12,0 г/л.
Молекулы IgG свободно диффундируют из крови в тканевую жидкость; здесь находится почти половина (48,2%) имеющегося в организме IgG. В тканевой жидкости IgG наиболее значим среди других классов иммуноглобулинов в нейтрализации бактериальных токсинов и связывании микроорганизмов. IgG, связываясь с бактериями, активирует комплемент по классическому пути, вызывает хемотаксис полиморфноядерных лейкоцитов.
Скорость биосинтеза IgG составляет 33 мг/кг массы в день, период полураспада – 23 дня (IgG3 – 7-9 дней).
IgM представляет собой пентамер, имеет мол. массу 950 000, валентность - 10 (Рис. 5-13). Концентрация IgM в сыворотке крови составляет 0,5-2 г/л. Этот иммуноглобулин обладает выраженной способностью преципитировать, агглютинировать антигены и лизировать микроорганизмы при участии комплемента. Среди всех иммуноглобулинов IgM проявляет наибольшую способность к связыванию комплемента.
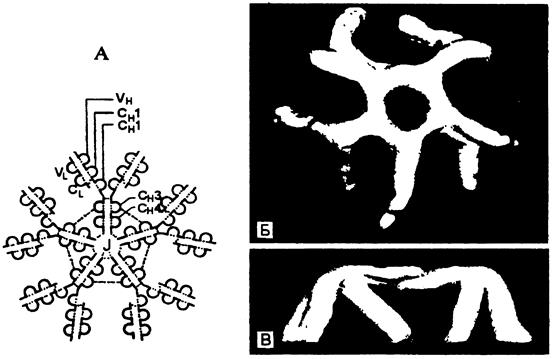
Р и с. 5-13. Структура IgM.
Скорость биосинтеза IgM составляет 6,7 мг/кг массы в день, период полураспада – 5,1 дня. IgM синтезируется на ранних стадиях иммунного ответа, обеспечивая первую линию обороны при бактериемии.
IgA содержится в сыворотке и секретах организма. Сывороточный IgA представлен мономерной формой, двухвалентен, имеет мол. массу 160 000. Концентрация его в сыворотке в среднем составляет 2 г/л. IgA не обладает способностью связывать комплемент, не способен преципитировать растворимые и агглютини-ровать корпускулярные антигены, лизировать микроорганизмы.
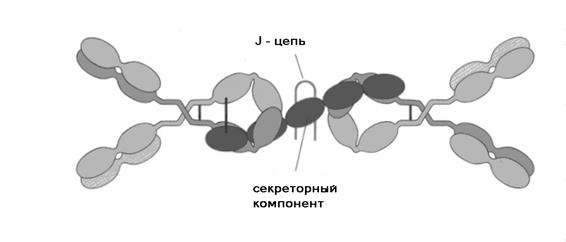
Р и с. 5-14. Строение секреторного иммуноглобулина А
Секреторный IgA состоит из двух IgA-молекул, которые ковалентно связаны J-цепью и с секреторным компонентом (SC). Секреторный компонент представляет собой полимерную иммуноглобулиновую молекулу, состоящую из пяти Ig- подобных доменов. С помощью дисульфидных мостиков SC связан с димером IgA
Секреторный IgA содержится в слюне, слезной жидкости, носовых выделениях, поте, секретах бронхов, легких, слизистых оболочек желудочно-кишечного тракта и мочеполовых путей. Секреторный IgA обеспечивает защиту слизистых оболочек от микроорганизмов, является основным фактором местного иммунитета. Секреторный IgA существует в основном в форме димера, четырехвалентен (Рис 5-14). Синтезируется иммуноглобулин плазматическими клетками лимфоидных скоплений слизистых оболочек в виде мономеров, которые внутри клетки димеризуются при участии J-цепи (Рис. 5-15). В слизистой к димеру IgA присоединяется секреторный компонент (SC - secretory component), продуцируемый эпителиоцитами слизистых оболочек. Секреторный компонент (SC) предохраняет молекулу антитела от действия многочисленных ферментов, находящихся в составе секретов слизистых оболочек.
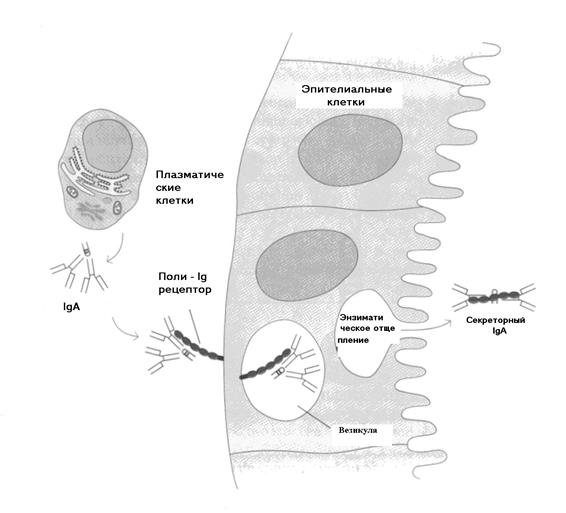
Р и с. 5-15. Транспорт IgA в секреторную жидкость.
Секреторный IgA формируется как единая молекулярная структура в процессе транспорта димера IgA через слизистую. Продуцируемый в подслизистом слое плазматическими клетками, димер IgA связывается поли-Ig-рецепторами (полимерными иммуноглобулиновыми молекулами) эпителиальных клеток слизистого слоя, расположенных на базолатеральной мембране. Образовавшийся комплекс рецептор-IgA затем транспортируется с помощью механизма эндоцитоза внутрь эпителиальной клетки с образованием в ней везикулы, в составе которой этот комплекс далее транспортируется к ее наружной мембране. После слияния везикулы с плазматической мембраной клетки поли-Ig-рецептор энзиматически отщепляется от стенок везикулы и, став свободным (несвязанным с ней), уже в качестве секреторного компонента окончательно встраивается в структуру димера IgA. Путем экзоцитоза, сформированный таким образом sIgA, высвобождается в слизистый секрет.
IgD представляет собой мономер, имеет мол. массу 175000, двухвалентен. Его концентрация в сыворотке составляет до 0,4 мг/мл. Скорость его биосинтеза составляет 0,4 мг/кг массы в день, период полураспада – 2,8 дня. Биологическая функция сывороточного IgD не выяснена.
IgE, по строению мономер, имеет мол. массу 190000, двухвалентен. Концентрация в сыворотке составляет 0,25 мг/л. Скорость биосинтеза IgE составляет 0,02 мг/кг массы в день, период полураспада – 2,5 дня. IgE не обладает способностью связывать комплемент, но прочно и быстро связывается с клетками, в частности, с тучными клетками и базофилами. Взаимодействие IgE с антигеном на поверхности тучных клеток приводит к их дегрануляции и высвобождению вазоактивных аминов, обусловливающих симптомы аллергических реакций. Основная физиологическая функция IgE заключается в защите слизистых оболочек от инфекций. В общем виде структура и функция антител представлена на рис.5-16.
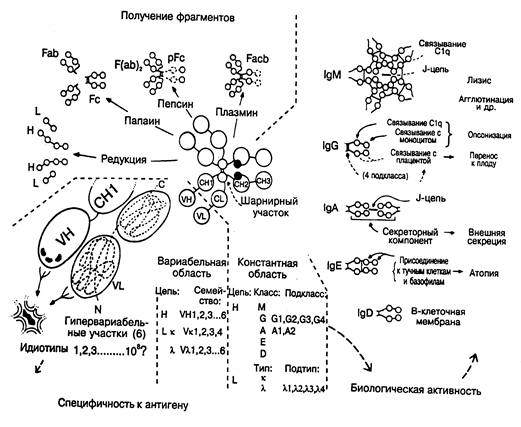
Р и с. 5-16. Структура и функции антител.
 2015-06-10
2015-06-10 5015
5015







