Для полноценного гемостаза тромбоциты должны пройти 3 стадии:
1) адгезию к ставшим доступными при повреждении белкам межклеточного матрикса и переход в активную форму;
2) высвобождениесодержимого своих гранул;
3) агрегацию.
В активирования тромбоцитов участвует фосфатидилинозитольный механизм передачи сигнала. Нормальный неактивный тромбоцит с гладкой поверхностью не обладает способностью прилипать к сосудистой стенке или взаимодействовать с другими тромбоцитами. Однако свойства тромбоцитов резко изменяются при контакте с чужеродной поверхностью, которая возникает при повреждении стенки сосуда. Тромбоцит приходит в контакт с подлежащими под эндотелием белками межклеточного матрикса – коллагеном, фибронектином или ламинином. Для каждого из этих белков у тромбоцита имеется специфические мембранные рецепторы, которые по структуре напоминают интегрины в других клетках. Например, рецептор к ламинину представлен полипептидной цепью (α-цепь), связанной с гликопротеином мембраны тромбоцита ГПIIa. Рецептор к фибронектину тоже димер из двух гликопротеинов ГП1c и ГПIa. При взаимодействии с коллагеном базальной мембраны участвуют несколько рецепторов (ГПIa/ГПIIa, ГПVI и возможно ГПIV и ГПIIb). В условиях высокого артериального давления, которое преобладает в артериолах и микроциркуляционном русле, указанные выше взаимодействия, называемые адгезией тромбоцитов, не проявляются и более прочное взаимодействие поврежденным участком обеспечивается участием фактора Виллебранда, который взаимодействует с тромбоцитарным рецептором, образованным димером ГПIb и IX.
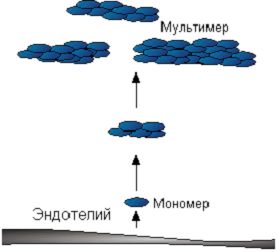
Фактор Виллебранда (ф.В.) - мультимерный гликопротеин, построенные из мономерной формы с мол. массой 200 кДа. Мономер содержит несколько отдельных доменов, которые связывают соответственно фVIII, гепарин, коллаген и рецепторы тромбоцита. Различают низкомолекулярные и высокомолекулярные формы мультимера, которые циркулируют в плазме в комплексе с фактором VIII.
Ф.В. синтезируется клетками эндотелия, которые его секретируют в плазму и депонируют в субэндотелиальном матриксе, а также мегакариоцитами (предшественниками тромбоцитов), которые его хранят в α-гранулах. Для оптимальной адгезии пластинок необходим как растворимый в плазме, так и субэндотелиальный ф.В. Ф.В. взаимодействует с коллагеном и гепариноподобным ГАГ в субэндотелии и через комплекс гликопротенов Ib/IX формирует мостик между тромбоцитом и субэндотелием сосуда. При наследственном дефекте - дефиците фактора Виллебранда (болезнь Виллебранда) или ГП1b (синдром Бернара-Сулье) процесс адгезии тромбоцитов нарушается.
После фиксации тромбоцитов на субэндотелиальных структурах они очень быстро теряют свою дисковидную форму и распластываются на сосудистой стенке (рис.13.7). В основе этих изменений лежит включение фосфатидилинозитольного пути передачи сигнала, вызванного взаимодействием рецепторов с белками субэндотелиального матрикса или тромбином, образующимся в сосудистом русле. Возникающий при этом ДАГ активирует протеинкиназу С, которая катализирует в цитоплазме фосфорилирование специфического белка (мол.масса равна 47 кДа), контролирующего секрецию гранул тромбоцитов. Высвобождающийся из плотных гранул АДФ, вызывает активирование других тромбоцитов, а также вызывает перестройку поверхности тромбоцитов, способствующую улучшению доступа к рецепторам на поверхности мембран для лигандов и, в частности, для фибриногена, присоединение которого к рецепторам (ГПIIb и ГПIIIa) способствует связыванию между собой тромбоцитов и образованию агрегатов тромбоцитов.
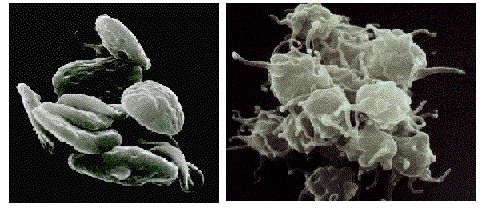
Рис 13.6. Формы неактивных и активных тромбоцитов
Инозитолтрифосфат (ИФ3) мобилизует Са2+ из плотных гранул (или цистерн ЭР), который связывается с калмодулином и активирует специфическую киназу, катализирующую фосфорилирование легких цепей миозина. Последние взаимодействуют с актином с образованием актомиозина (тромбостенина), обеспечивающего подвижность тромбоцитов и их способность изменять форму.
Увеличение уровня ионов кальция в цитоплазме сопровождается также и активированием фосфолипазы А2 (ФЛА2).ФЛА2, гидролизуя фосфолипиды плазматической мембраны, приводит к высвобождению жирных кислот, преимущественно арахидоновой кислоты, используемой как субстрат в синтезе тромбоксана А2 ипростагландинов.
Процесс агрегациитромбоцитов носит двухфазный характер.Первая фаза, продолжительностью до 2 мин, — обратимая. Образующиеся агрегаты рыхлые, непрочные, легко разрушаются и недостаточно хорошо фиксируются. Если на этом этапе активация тромбоцитов прекращается, то тромбоцитарные агрегаты могут распадаться и тромбоциты приобретают свою исходную форму.
При продолжительной и интенсивной стимуляции тромбоцитов первая фаза сменяется фазой необратимой агрегации, которая сопровождается усилением высвобождения факторов агрегации второго порядка, таких, как серотонин, адреналин и сосудосуживающий тромбоксан А2, которые одновременно привлекают другие тромбоциты к агрегации, активируя их. Агрегация ускоряется фибриногеном, который, взаимодействуя со своими рецепторами (ГПIIb /ГПIIIa), связывает между собой соседние тромбоциты. Во время агрегации тромбоцитов наблюдается локальное усиление механизма свертывания с участием белков плазмы крови. Это достигается присоединением фактора V к мембранам тромбоцитов и его активированием. Образованный агрегат тромбоцитов через фазу “вязкого метаморфоза” превращается в тромб, который может надолго закрыть капилляр. Результатом описанного процесса является образование так называемого белого тромба, состоящего из тромбоцитов и фибриногена с небольшой примесью эритроцитов. Описанный выше процесс обеспечивает остановку кровотечения при повреждении капиллярной сети и служит одновременно инициатором процессов с участием белков плазмы крови.
 2015-06-04
2015-06-04 668
668








