Сильные электролиты в отличие от недиссоциирующих и слабо диссоциирующих соединений адсорбируются в виде ионов. Адсорбция в большинстве случаев происходит под действием химических сил, а не сил
Ван – дер - Ваальса, поэтому с ростом температуры величина адсорбции увеличивается.
Ионную адсорбцию называют полярной, так как способные поляризоваться ионы адсорбируются на тех поверхностях, которые состоят из полярных молекул или ионов. Адсорбционная способность ионов зависит от их природы, радиуса и величины заряда. Чем больше радиус иона, тем меньше он гидратируется, тем легче поляризуется, тем выше адсорбционная способность. По возрастающей способности адсорбироваться одно- и двухзарядные катионы можно расположить в лиотропные ряды:
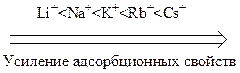
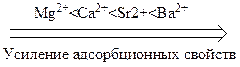
Однозарядные анионы по их возрастающей адсорбционной способности располагаются в таком порядке
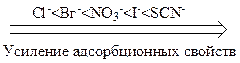
С возрастанием заряда иона увеличивается его поляризуемость и склонность к адсорбции, поэтому
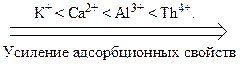
Ионная адсорбция может протекать по двум основным механизмам:
1. Избирательная адсорбция на кристаллах.
2. Ионообменная адсорбция.
И в том, и в другом случае адсорбция ионов связана с образованием двойного электрического слоя (ДЭС) на границе раздела твердой и жидкой фаз.
 2015-06-14
2015-06-14 885
885








