 Одним из основных законов является обнаруженная французским химиком Ф. М. Раулем в 1887 г. закономерность, определяющая некоторые зависящие от концентрации, но не от природы растворённого вещества, свойства растворов.
Одним из основных законов является обнаруженная французским химиком Ф. М. Раулем в 1887 г. закономерность, определяющая некоторые зависящие от концентрации, но не от природы растворённого вещества, свойства растворов.
Над любой жидкой фазой всегда существует определенное (в зависимости от внешних условий) количество газообразной состоящей из того же вещества. Так, над водой, находящейся в атмосфере, обязательно имеется водяной пар. Количество этой паровой фазы выражается парциальным давлением (концентрацией газа), равным общему, при условии, что данный газ занимает общий газовый объем.
Физические свойства растворов (растворимость, температуры замерзания и кипения) в первую очередь обусловлены изменением давления насыщенного пара растворителя над раствором. Франсуа Рауль установил, что давление насыщенного пара растворителя над раствором всегда ниже, чем над чистым растворителем и вывел следующее соотношение:
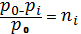 . (7.4.1)
. (7.4.1)
Здесь:
р0 – парциальное давление пара растворителя над чистым растворителем;
рi – парциальное давление пара растворителя над раствором;
ni – мольная доля растворенного вещества.
Таким образом, один из основных законов, определяющих физические свойства растворов можно сформулировать так:
 2015-06-14
2015-06-14 616
616








