Иммунитет - это система защиты организма от всего генетически чужеродного, прежде всего многочисленных микроорганизмов и генетически измененных собственных клеток, включая раковые или отжившие свой срок.
Антигены (Аg) - чужеродные вещества.
Иммунный ответ осуществляется иммунокомпетентными клетками, продуктами их жизнедеятельности - цитокинами и направлен на элиминацию Аg (рис 2.11 Л),
Если в элиминации Аg ведущую роль играют секреторные продукты В-клеток -антитела, то говорят о гуморальной форме иммунного ответа. Если же элиминация А§ осуществляется с непосредственным участием Т-лимфоцитов - о клеточном иммуном ответе.
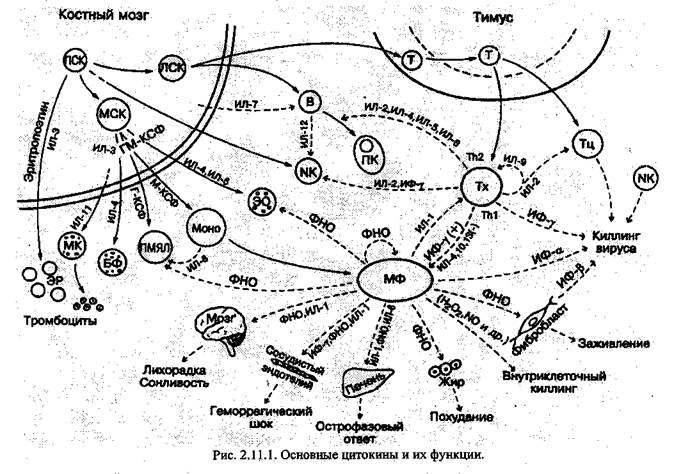
Тип иммунного ответа диктует сам Аg. Если Аg находится на клетке (трасплантант, опухолевая клетка, клетка, инфицированная вирусами или бактериями и т.д.), - в основном развивается клеточный иммунный ответ. На растворимые антигены (белки, полисахариды, а также бактерии, паразиты) формируется гуморальный иммунный ответ, и он осуществляет антибактериальную защиту и нейтрализацию токсинов.
Включение иммунных механизмов начинается с момента проникновения А§ организм (пути проникновения могут быть различные: чрезкожные, дыхательные пути, через желудочно-кишечный тракт, парентеральный, трансплацентарный).
С Аg взаимодействует антигенпрезинтирующая клетка (АПК), К АПК относятся макрофаги различного происхождения (моноциты, гистиоциты, клетки Купфера, мезанги-альные, альвеолярные, эндотелиальные, микроглия, кл. Лангерганса и др.). После обработки Аg и выявления его детерминантных групп в виде фрагмента пептида АПК выставляют эти детерминантные группы на своей поверхности в комплексе со своими антигенами гистосовместимости 2 класса для презентации Аg Т-хелперам. При этом выделяются цитокины и сигнальные адгезивные молекулы (ИЛь ИЛ4 ИЛ6, ИЛ12,ИЛ 15, ФИО, интер-фероны, СД4, СД8, СД8о, СД86 и др.).
На следующем этапе кооперации осуществляется взаимодействие Т-лимфоцитов с В-лимфоцитами (в случае гуморального иммунного ответа), в ходе которого В-лимфоцит распознает А§ на поверхности АПК и получает стимуляцию от АПК ИЛь от Т-хелпера ИЛ2 для последующего деления и дифференцировки в клетки памяти или плазматические клетки, которые синтезируют антитела. Вначале это 1§ М - низкоспецифические, затем, под влиянием лимфокинов, секретируемых Т-хелперами, - высокоспецифические 1§ О и А.
Иммуноглобулины различных классов имеют разное строение и соответственно различные свойства, но все они вступают во взаимодействие с Аg, способствуя в дальнейшем его элиминации (активируя комплемент, что способствует лизису корпускулярного антигена или привлекая фагоциты -~ опсонызация).
Для формирования клеточного иммунного ответа необходимы те же этапы кооперации. Т-хелперы выделяют ИЛ2 и др. цитокины, необходимые для созревания и дифференцировки цитотоксических лимфоцитов, теперь они называются Аg реактивные и способны расправиться с Аg-несущей клеткой с помощью своих цитокинов: ФИО, интерфе-роны. Много лимфокинов действует на фагоциты, например, МУФ - миграцию угнетающий фактор и др. привлекают их к Аg и стимулируют их активность.
Таким образом, при клеточном иммунном ответе цитотоксические лимфоциты через фагоциты, ТЧК-клетки и цитокины разрушают генетически чужеродные клетки.
Иммунопатология включает иммунодефициты, аллергические заболевания, аутоиммунные заболевания и лимфопролиферативные заболевания.
/. Иммунодефицитные состояния: первичные и вторичные. Патогенез СПИДа.
Иммунодефициты - нарушения нормального иммунологического статуса, которые обусловлены дефектом одного или нескольких механизмов иммунного ответа. Они подразделяются на первичные (врождённые, генетически обусловленные) и вторичные.
Вторичные иммунодефициты - это недостаточность иммунной системы, возникшая как следствие какого-то заболевания у ранее здорового человека, эта недостаточность может быть обратимой при устранении вызвавшей её причины.
Вторичный иммунодефицит встречается значительно чаще, чем первичный, почти каждое серьёзное заболевание с длительным течением в какой-то степени ослабляет иммунную систему, а также различные виды лечения химио- и лучевая терапия; все без исключения препараты, которые используют для лечения сердечно-сосудистой системы, ЖКТ, нервной системы оказывают седативное воздействие и на иммунные клетки.
Одним из наиболее клинически значимых вторичных иммунодефицитов является синдром приобретенного иммунодефицита (СПИД) обусловленный инфицированием вирусом иммунодефицита человека (ВИЧ) (рис. 2.11.2.). Следует отметить, что термином СПИД обозначается лишь последняя стадия (по клиническому течению) ВИЧ-инфекции, поскольку иммунодефицит формируется только на заключительном этапе болезни.
Впервые синдром описан в научной литературе в 1981 г. американскими исследователями. Однако ретроспективный анализ позволяет утверждать, что СПИД поражал людей и ранее. Первые случаи синдрома официально были зарегистрированы в США, Африке, на Гаити. В последние годы, когда были налажены методы диагностики СПИДа, выяснилось, что каждые 12-14 месяцев число зарегистрированных случаев синдрома удваивается. Соотношение инфицированных лиц к заболевшим колеблется от 50:1 до 100:1.
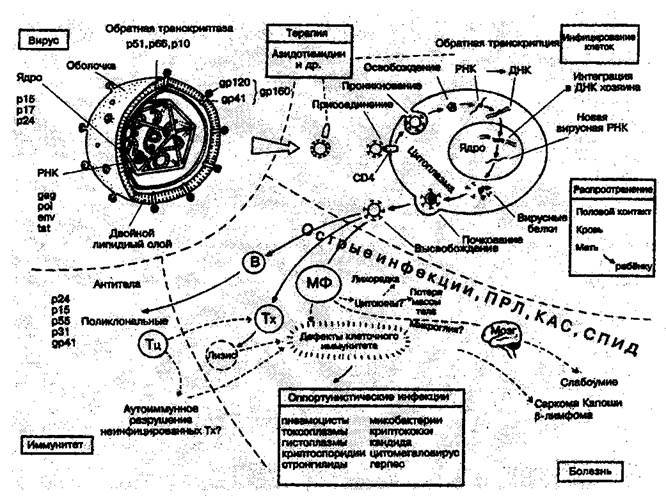
Рис. 2.11.2. Схема развития и проявлений ВИЧ-инфекции и СПИДа.
Наибольшее распространение ВИЧ-инфекция имеет среди гомо- и бисексуальных мужчин, наркоманов, вводящих наркотики внутривенно и пользующихся "коллективными" шприцами; реципиентов гемотрансфузий (больные анемиями); детей родителей, больных ВИЧ-инфекцией.
Возбудитель ВИЧ-инфекции относится к группе ретровирусов подсемейства ленти-вирусов. Они содержат однонитчатую линейную РНК и фермент ревертазу (РНК-зависимая ДНК полимеразу). Репликация вирусной нуклеиновой кислоты идет через стадию синтеза двунитчатой ДНК на матрице РНК. В клетку-мишень проникает ДНК-копия с РНК вируса, котрая интегрируется с клеточным геномом. Транскрипция информации вирусной ДНК осуществляется при участии клеточной РНК-полимеразы. Созревание вириона путем почкования идет на клеточных мембранах. В организм вирус проникает с кровью и ее дериватами, клетками при пересадке тканей и органов, переливании крови, со спермой и слюной через поврежденную слизистую или кожу. Проникнув в организм, возбудитель ВИЧ-инфекции внедряется в клетки, имеющие рецепторы СD4, к которым гликопротеиды вирусной оболочки имеют высокий аффинитет. Наиболее богаты рецепторами СD4 Т-лимфоциты-хелперы, в которые в основном и проникают вирусы. Однако
помимо этого вирус способен внедряться и в моноциты, фагоцитирующие клетки, нейроны, клетки нейроглии, слизистой прямой кишки.
Вирус обнаруживается в крови, в ткани слюнных желез, простаты, яичек. Через 6-8 недель (реже - через 8-9 месяцев) после инфицирования появляются антитела к ВИЧ.
Существует несколько версий о механизме лизиса клеток, пораженных ВИЧ,
Одно из допущений (Р.Галло,1983) заключается в разрушении мембран лимфоцитов, моноцитов, нейронов при "отпочковывании" вируса от клетки с последующим их лизисом. Вероятность гибели клеток пропорциональна количеству рецепторов СD4 на их поверхности. Наибольшее их число имеют Т-хелперы, в связи, с чем их количество значительно уменьшается.
В качестве другого механизма лизиса инфицированных ВИЧ клеток рассматривается возможность встраивания белков вирусной оболочки в клеточные мембраны. В связи с этим клетки распознаются ИКС как чужеродные и уничтожаются (Р.Курт, Х.Бреде,1984).
Гибель клеток связана не только с непосредственным цитопатогенным действием вируса, но и с индукцией апоптоза клеток вследствие перекрестного связывания СD4 белком gр 120.
Полагают также, что инкорпорация ДНК вируса (провируса) в геном Т-хелпера лишает их способности к трансформации и реагированию на регуляторные стимулы, в частности - на ИЛ2.
Допускается также регуляторное подавление Т-хелперов растворимыми факторами супрессии, которые выделяют мононуклеары крови больных СПИДом (Дж. Ло-уренс,1983).
Эти и другие механизмы действия ВИЧ на клетки обуславливают их лизис, вызывая уменьшение их числа. В наибольшей мере это относится к Т-хелперам. Именно по этому развивается лимфопения. Кроме того, подавляется способность Т-хелперов продуцировать ИЛ2.
Одновременно наблюдается снижение (примерно на 80-90%) количества и функциональной активности естественных киллеров (NК-клетки).
Число В-клеток, как правило, остается в пределах нормы, но функциональная активность их нередко снижается.
Количество макрофагов обычно не изменяется, однако выявляется нарушение хемотаксиса и внутриклеточного переваривания чужеродных агентов. Отмечается также расстройство механизма "презентации" макрофагом антигена Т- и В-лимфоцитам.
Указанные изменения создают предрасположенность больных СПИДом к инфекциям, лимфоретикулярным опухолям (саркома Капоши), а также - неспособности к развитию аллергических реакций замедленного типа.
Первичные иммунодефициты подразделяют на 4 главные группы, в зависимости от того, какой компонент иммунной системы неполноценен: дефекты В- или Т- лимфоцитов, фагоцитирующих клеток или комплемента. Лидирует патология В-клеток, т. е. дефекты выработки антител, она составляет более 50% случаев первичного иммунодефицита, патология Т - клеток - 30%, дефекты системы фагоцитов менее 18%, недостаточность комплемента - приблизительно 2%, т. е. наиболее уязвимы те отделы иммунитета, которые эволюционно сформировались позднее. I. Патология В-клеток
1. Агаммаглобулинэмия характеризуется отсутствием В-клеток (болезнь Брутона), неспособностью В-лимфоцитов дифференцироваться в плазматические клетки.
2. Гипогаммаглобулинэмш или избирательная неспособность к продукции какого-либо одного класса иммуноглобулинов, чаще Ig А - селективный имунодефицит Ig А, встречается 1:400. У этих больных часто развиваются аллергия и полиартрит. Страдают рецидивирующими бактериальными инфекциями: стафилококк, стрептококк, пневмококк, нейсерии.
II. Дефекты с преимущественным поражением Т-клеток
1. Синдром Ди-Джорджи - гипоплазия тимуса и паращитовидных желез вследствие недоразвития 3-4 жаберных карманов (характерны гипокальциемическая тетания, врождённая патология сердца), рецидивирующие инфекции появляются уже вскоре после рождения. Инфекции для Т-иммунодефицита другие: вирусные: корь, цито-мегаловирусные, туберкулёз, БЦЖ, грибы, пневмоцисты, кандидоз,
2. Тяжёлый комбинированный иммунодефицит ТКИД (дефекты Т и В-лимфоцитов). Выраженное функциональное нарушение гуморального и клеточного иммунитета. Имеются многообразные дефекты в развитии иммунокомпетентных клеток. Характерны выраженная лимфопения и агаммаглобулинемия. Болеют в основном дети, которые погибают в раннем возрасте.
3. ИД с атаксией-телеангиэктазией, синдром Вискотта-Олдрича - иммунный дефект проявляется в нарушении клеточного иммунитета и снижении антителообра-зования, имеется триада клинических признаков - экзема, тромбоцитопения и инфекционные осложнения.
III. Дефекты миелоидных клеток
1; Хроническая гранулёматозная болезнь - дефект генерации активных форм кислорода.
2. Синдром Чедиака-Хигаси - не формируют фаголизосомы, в других случаях нарушается хемотаксис - «ленивые лейкоциты».
IV. Дефекты системы комплемента (возможен генетически обусловленный дефицит
любого компонента комплемента)
1. Дефект инактиватора - например ингибитора С1 (наследственный ангионевротиче-ский отёк).
2. Дефекты С1С4,С2 обуславливают предрасположенность к болезням иммунных комплексов (СКВ), С5-С9 - предрасположенность к инфекции, вызванной нейсериями.
//- Типы аллергических реакций. Стадии аллергии. Основные проявления аллергии.
Под аллергией понимается форма иммунного ответа организма на вещества антигенной или гаптеновой природы, сопровождающаяся повреждением структуры и функции собственных клеток, тканей и органов.
Аллерген - вещество (антиген, гаптен), вызывающее развитие аллергической реакции.
Протекание реакции на антиген как аллергической связано, во-первых, с характером антигена, его свойствами и количеством, во-вторых, с особенностями реактивности организма.
Повышенной реактивности способствуют:
1. Повышенная проницаемость кожных или слизистых барьеров, ведущая к поступлению в организм антигенов, которые в обычных условиях либо не поступают, либо их поступление ограничено (пыльца растений при поллинозах);
2. Выработка преимущественно 1% класса Е.
3. Нарушение инактивации биологически активных веществ. Например, при низкой активности плазмы крови связывать гистамин (так называемое гистаминопексическое свойство плазмы) освобождение его даже в небольших количествах может привести к патогенному эффекту и тем самым к развитию аллергической реакции.
Многие из этих особенностей детерминированы генетически, другие являются приобретенными.
Аллергены обладают всеми свойствами антигенов (макромолекулярность, преимущественно белковая природа, чужеродность для данного организма и др.).
Многие молекулярные соединения, например, лекарственные препараты, простые химические вещества (бром, йод, хром, никель и др.), а также более сложные продукты
небелковой природы (некоторые микробные продукты, полисахариды и др.), их называют гаптенамщ при попадании в организм, не включает иммунных механизмов, но становятся антигенами после соединения с белками тканей организма. Однако не каждое соединение химического вещества с белком приводит к образованию антигена.
Все аллергены принято делить на две группы: экзо- и эндоаллергены (или аутоал-лергены) образующиеся в самом организме.
Существует классификация, в основе которой лежит способ попадания аллергена в организм:
• воздушные, ингаляционные аллергена (бытовая и производственная пыль, пыльца растений, эпидермис и шерсть животных и др.);
• пищевые аллергены;
• контактные аллергены, проникающие через кожу и слизистые оболочки (химические вещества, лекарства);
• инъекционные (сыворотки, лекарства)
Классификация экзогенных аллергенов по происхождению:
• аллергены неинфекционного происхождения: бытовые, эпидермальные, пыльцевые, пищевые, промышленные.
• инфекционного происхождения: бактериальные, грибковые вирусные.
1. Домашняя пыль - сложный по своему составу аллерген, в который входят пылевые частицы одежды, постельного белья, мебели, грибы (в сырых помещениях), домашние насекомые, бактерии; основной компонент - клещи вида Dermatophagoideus, обитающие в постелях, подушках, питаясь чешуйками рогового слоя эпидермиса.
2. Эпидермальные: перхоть, шерсть животных, перья птиц, чешуя рыб.
3. Лекарственные.
4. Пыльцевые. Пыльца не всех видов растений, а только достаточно мелкая (диаметр не более 30 мкм), обладающая хорошими летучими свойствами. В каждой климатогео-графической зоне свои виды растений (береза, полынь, тимофеевка и др.).
Различные виды пыльцы могут иметь общие аллергены (пыльца злаковых) и поэтому могут давать перекрестные реакции. Лицам, страдающим поллинозами, не стоит увлекаться применением внутрь лечебных трав.
 2015-06-05
2015-06-05 2952
2952








