Имеем концентрированный раствор ρk; Vk; ωk. Надо приготовить раствор с
ω < ωk, тогда воды в раствор надо добавить 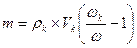 (грамм)
(грамм)
Задача. Ск. воды надо добавить к 0,5л 40% раствора NaOH (ρ = 1430 г/л),
чтобы приготовить 10% раствор щелочи.
Решение: воды надо добавить 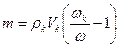
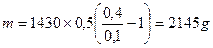
Задача. Вычислить процентную концентрацию раствора (ω%) NaOH, полученном при разбавлении 0,2 литра 2,5М раствора в 5 раз. M(NaOH) = 40
Решение: щелочи в исходном растворе m = C×M×V = 2,5×40×0,2 = 20г. Масса раствора после разбавления 200×5 = 1000 г. 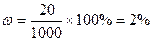
Задача. Сколько мл 0,1М раствора KMnO4 надо взять для приготовления
120мл 0,02М раствора.
Решение: H1×V1 = H2×V2: Vx×0,1 = 120×0,02; Vx = 24 мл. Исходный раствор надо разбавить в 120/24 = 5 раз.
Задача. Вычислить нормальность раствора щелочи NaOH, если 100 г 40%
раствора щелочи разбавили водой до 500 мл
Решение: в 100 г 40% раствора щелочи было 40 г. H = C/1 = 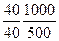 = 2
= 2
Задача. Какой объем раствора с δ = 9,3 кислоты H2SO4 с ρ = 1,05 (г/мл)
потребуется, чтобы приготовить 0,35М раствор кислоты объемом 40мл.
Решение: Vδ×ρ δ = VC C×M; 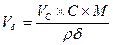 ;
; 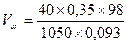 = 14 мл
= 14 мл
Задача. Вычислить объем 2М раствора серной кислоты, приготовленного
из 49 мл 98% раствора H2SO4 (ρ = 1,84 г/мл).
Решение: 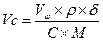 ;
; 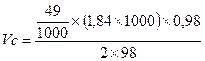 = 0,45(литр)
= 0,45(литр)
Задача. Ск. потребуется (мл) 63% раствора HNO3 (ρ= 1,35г/мл) для
приготовления 500мл 0,5M раствора кислоты M(HNO3) = 63.
Решение: 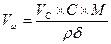 =
= 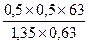 = 18,5 мл
= 18,5 мл
Задача. Какой объем 2М раствора вещества надо взять, чтобы получить 0,5 литра 0,1М раствора. Решение: 2×Vx = 0,5×0,1; Vx = 0,025 л = 25 мл.
 2015-06-05
2015-06-05 3260
3260








