В любой точке диаграммы, когда в сплаве одновременно существуют две фазы, можно определить концентрацию обеих фаз и их количество. Для этого служит так называемое правило отрезков или правило рычага.
В точке а, показывающей состояние сплава К при температуре t1 (риc. 1), сплав состоит из кристаллов сурьмы и жидкости. Выше точки l сплав находится в однофазном состоянии, и концентрация компонентов в этой фазе (т.е. в жидкости) определяется проекцией точки a. При охлаждении из, сплава выделяются кристаллы сурьмы, и состав жидкости изменяется в сторону увеличения в ней свинца. При температуре t1 концентрация сурьмы в жидкости определяется проекцией точки в; это максимальное количество сурьмы, которое может содержать жидкость при t1.
По достижении эвтектической температуры жидкость принимает эвтектическую концентрацию. Следовательно, при охлаждении сплава К концентрация жидкости меняется по кривой 1с. Выделяющиеся кристаллы свинца имеют постоянный состав - это чистый свинец, концентрация которого лежит на вертикальной оси BN.
Первое положение правила отрезков формулируется следующим образом: чтобы определить концентрацию компонентов в фазах, через данную точку, характеризующую состояние сплава, проводят горизонтальную линию до пересечений с линиями, ограничивающими данную область: проекции точек пересечения на ось концентраций показывают составы фаз.
Второе положение правила отрезков формулируется так; для того чтобы определить количественное соотношение фаз, через заданную точку проводят горизонтальную линию. Отрезки этой линии между заданной точкой и точками, определяющими составы фаз, обратно пропорционально количествам этих фаз.
В качестве примера определим концентрацию (состав) фаз и количественное соотношение фаз для сплава с содержанием 60 % Sb и 40 % Pb при 350 °С.
В соответствии с первым положением правила отрезков, концентрация твердой фазы определится проекцией точки а на ось абсцисс, т.е. она равна 100 % Sb, состав жидкой фазы определится проекцией точки в на ось абсцисс, что соответствует 30 % Sb.
В соответствии со вторым положением правила отрезков весовое количество фаз сплава при температуре 350 °С определится отрезками: ва - вес кристаллов Sb, ас - вес жидкой фазы, вс - вес всего сплава.
Спроектировав концентрационные отрезки на ось абсцисс, получим: ва = 60 - 30 = 30 %; ас =100 - 60 = 40 %; ВE=100-30=70 %.
Следовательно, весовое количество сурьмы QSb и жидкости Ql, определится соотношением отрезков:
QSb ва Qс ▪ ва
— = -----,откуда QSb = ------ ▪100 %;
Qс BE BE
Ql ac Qc ▪ ac
— = —; Ql = —— ▪100 %;
Qc BE BE
Qс - количеcтво всего сплава.
Вид диаграммы определяется характером взаимодействий, которые возникают между компонентами в жидком и твердом состояниях.
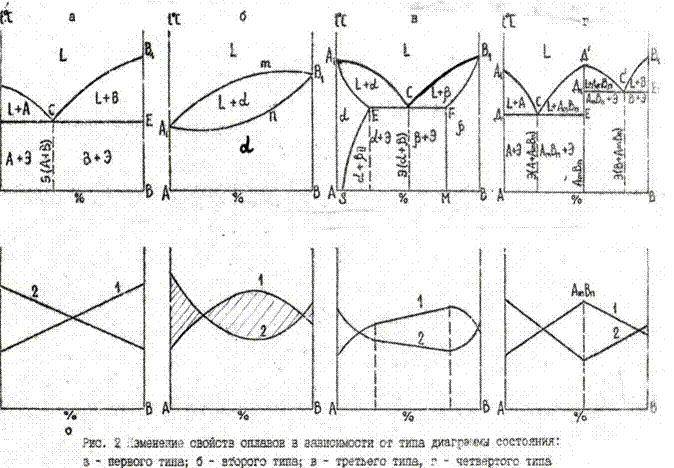
Наиболее типичные диаграммы состояния металлических систем приведены на рис. 5.
1. Диаграмма состояния для сплавов, образующих механические смеси из чистых компонентов (I типа, риc. 5,а).
Оба компонента в жидком состоянии неограниченно растворимы, а в твердом - нерастворимы и не образуют химических соединений,
Компоненты: А и В (К = 2). Фазы: жидкость L, кристаллы А и кристаллы В (Ф = 3).
Линия A1CB1 является линией ликвидус, линия ДСЕ - линией солидус и линией эвтектического превращения. На линии ДСЕ из жидкости концентрации точки С одновременно выделяются кристаллы А состава точки Д и кристаллы В состава точки Е. т.е.
Lc = кр.Ад + кр.ВЕ
Эта механическая смесь называется эвтектикой.
Сплавы, лежащие левее точки С, называют доэвтектическими, а сплавы, лежащие правее точки С, - заэвтектическими.
Доэвтектические сплавы состоят из смеси кристаллов А и эвтектики (кр.А + Э), заэвтектические - из смеси кристаллов В и эвтектики (кр.В + Э).
2. Диаграмма состояния для сплавов с неограниченной растворимостью компонентов в твердом состояния (II типа, рис.5,б).
Оба компонента неограниченно растворимы в жидком и твердом состоянии и не образуют химических соединений.
Компоненты: А,В (К - 2). Фазы: L, кристаллы α (Ф=2),
линия АmВ -линия ликвидус, линия АnВ - линия солидус.
Если два компонента неограниченно растворяются в жидком и твердом состояниях, то возможно существование только двух фаз -жидкого раствора L и твердого α-раствора. Следовательно, трех фаз быть не может, кристаллизации при постоянной температуре не наблюдается и горизонтальной линии на диаграмме нет. Диаграмма состоит из трех областей: жидкость, жидкость - твердый раствор и твердый раствор.
При двух компонентах и двух фазах система моновариантна (С=K-f + l = 2-2+l=l), т.е. если изменяется температура, то изменяется и концентрация компонентов в фазах; каждой температуре соответствуют строго определенные составы Фаз.
Концентрация и количество фаз у сплава, лежащего между линиями ликвидус и солидус, определяется правилом отрезков.
Следует обратить внимание на то, что во всем интервале кристаллизации (между линиями ликвидус и солидус) из жидкого сплава выделяются кристаллы, более богатые тугоплавким компонентом.
3. Диаграмма состояния для сплавов с ограниченной растворимостью в твердом состоянии (III типа, рис. 5,в).
Оба компонента неограниченно растворимы в жидком состоянии, ограниченно - в твердом и не образуют химических соединений.
Компоненты А и В (К = 2), Фазы (L, кристаллы α, кристаллы β (Ф = 3), кристаллы α - твердый раствор компонента В в компоненте А, кристаллы β - твердый раствор компонента А в компоненте В.
Линия A1CB1 - линия ликвидус.
Линия A1ECFB1 - линия солидус.
Линия ECF - линия эвтектического превращения:
Lc = кр.αЕ + кр. βЕ
└ эвтектика ┘
Линия ES - линия ограниченной растворимости в твердом состоянии компонента В в компоненте А.
Линия FM - линия ограниченной растворимости в твердом состоянии компонента А в компоненте В.
Структурные составляющие, образующиеся в процессе охлаждения сплавов данной системы, показаны на рис 5,в.
4. Диаграмма состояния для сплавов, образующих химическое соединение (IV типа, рис. 5,г).
Если компоненты А и В образуют химическое соединение AnBm, то, следовательно, на n + m его атомов приходится n атомов А и m атомов В.
Компоненты А и В (К =2).Фазы: кристаллы А, кристаллы AnBm и L или кристаллы АnBm кристаллы В и L.
Линия A1CДС'B1 - линия ликвидус
Линия ДCEД1E1 - линия солидус
Линия ДСЕ - линия эвтектического превращения:
Lc =кр.Ад + кр.АnВmЕ, (Ф = 3)
└ (эвтектика) ┘
Линия Д1C'E1 - линия эвтектического превращения:
Lc' = кр.АnBmД1. + кр.BЕ1, (Ф = 3)
└ (эвтектика) ┘
Диаграмму состояния, приведенную на рис. 2,г. следует рассматривать как сложную, состоящую ив двух простых диаграмм:
1.Компонент А - химические соединение AnBm.
2.Компонент В - химическое соединение AnBm.
Точка Д' - сингулярная точка, где образуется химическое соединение AnBm.
 2015-06-10
2015-06-10 1513
1513








