Простые эфиры. эпоксисоединения
R-O-R ¢.
R = R ¢ — симметричные
R ¹ R ¢ — смешанными
Синонимы циклических простых эфиров — органические окиси.
Простые насыщенные эфиры
Номенклатура и изомерия
Радикало-функциональная номенклатура:
CH3-О-СН3 — диметиловый эфир,
C2H5-О-СН3 — метилэтиловый эфир
Заместительная номенклатура:
 СН3CH2-ОCН3 СН3CH2-ОCН3 | — | метоксиэтан, |
 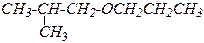 | — | 2-метил-1-пропоксипропан, |
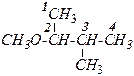 | — | 3-метил-2-метоксибутан. |
С2Н5ОС2Н5 — серный, или медицинский, эфир.
СН3ОСН2СН2ОСН2СН2ОСН3 — диглим (диметиловый эфир диэтиленгликоля)
моноэфиры этиленгликоля имеют общее название — целлозольвы (метилцеллозольв СН3ОСН2СН2ОН, этилцеллозольв С2Н5ОСН2СН2ОН).
Физические и химические свойства
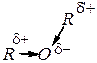 простые эфиры — полярные соединения. Валентный угол СОС составляет 109°—112°. Это влияет на их растворимость в воде — простые эфиры значительно лучше растворимы, чем незамещённые углеводороды.
простые эфиры — полярные соединения. Валентный угол СОС составляет 109°—112°. Это влияет на их растворимость в воде — простые эфиры значительно лучше растворимы, чем незамещённые углеводороды.
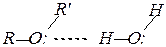
простые эфиры в обычных условиях — инертные химические соединения.
1) В жёстких условиях — нуклеофильное замещение — ацидолиз простых эфиров — реакция Цейзеля:
при повышенном давлении и высокой температуре простые эфиры расщепляются под действием HI, хотя возможно использование H2SO4 или HBr:
R-O-R ¢ + HI ® R-I + R ¢ -OH
Если один из углеводородных радикалов R — третичный, то образуется третичный алкилйодид,
механизм реакции — SN 1:
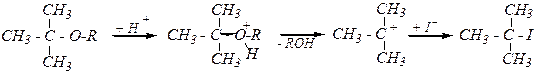
В остальных случаях реакция протекает преимущественно по SN 2-механизму — образуется йодометан и соответствующий спирт:
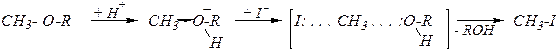
Расщепление метил- и этилалкиловых эфиров посредством HI используют для количественного определения метокси- и этоксигрупп (метод Цейзеля).
2) Взаимодействие со щелочными металлами:
R-О-R ¢ + 2Na ® R-O-Na + R ¢ -Na
3) Оснóвные свойства —могут образовывать с кислотами оксониевые соли:
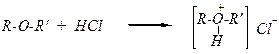
хлорид диалкилоксония
Основания слабые, оксониевые соли в присутствии воды полностью гидролизованы.
Диэтиловый эфир начинает протонироваться в ощутимых количествах только в растворе 30-50%-й серной кислоты.
4) Радикальные реакции по a-углеродному атому.
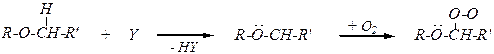
инициирующая
частица

Продуктами окисления — гидропероксиды — нестабильные и взрывчатые соединения. При хранении диалкиловых эфиров с доступом воздуха, особенно на солнечном свету в прозрачных бутылках, всегда образуется примесь гидропероксидов.
 2015-06-26
2015-06-26 1824
1824







