Физический факультет
Отчет
По лабораторной работе
«Оптический спектр излучения атома водорода»
Выполнил:
студент группы №535
Сорокин Д.С.
Проверил:
Марычев М.О.
г. Нижний Новгород
2011 г.
Теоретическая часть
Спектры излучения атомов
Экспериментально установлено, что спектры излучения твердых тел являются сплошными. Напротив, спектры газов содержат узкие спектральные линии.
Более подробные исследования показывают, что спектры разреженных одноатомных газов являются строго линейчатыми – состоящими из отдельных спектральных линий. Спекры молекулярных газов имеют более сложную структуру: группы близких линий образуют широкие полосы.
Следовательно, изолированные атомы любого химического элемента излучают дискретный набор длин волн. Спектр каждого элемента весьма отличается от спектров всех прочих элементов. На этом и основан спектральный анализ.
Самый простой спектр излучения имеет атомарный водород. В видимом диапазоне наблюдаются только четыре узкие линии, которые были обозначены символами Hα, Hβ, Hγ, Hδ в порядке убывания длины волны.
Еще в конце 20 века было установлено, что длины волн этих линий точно описываются простой эмпирической формулой
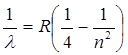 , (1)
, (1)
где 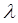 длина волны.
длина волны.
Параметр n для линий Hα, Hβ, Hγ, Hδ принимает значения 3,4,5,6 соответственно.
Очень важным является тот факт, что величина R оказывается одинаковой для всех четырех линий. Постоянная R имеет размерность обратной длины.
Дальнейшие экспериментальные исследования атома водорода в ультрафиолетовом и инфракрасном диапазонах излучения позволили обнаружить множество дискретных спектральных линий. Длины волн всех линий успешно описываются единой формулой:
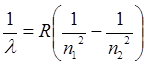 , (2)
, (2)
параметр n1 может принимать любые значения из натурального ряда: 1,2,3 и т.д. Параметр n2 также принимает ряд увеличивающихся целых значений, начиная с n1+1. Согласно формуле (2), каждой паре чисел n1 и n2 (n2 >n1) соответствует определенная длина волны 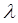 , наблюдающаяся в спектре излучения атома водорода.
, наблюдающаяся в спектре излучения атома водорода.
При n1=1 и для любых n2 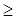 2 все спектральные линии лежат в ультрафиолетовой области и образуют серию Лаймана.
2 все спектральные линии лежат в ультрафиолетовой области и образуют серию Лаймана.
При n1=2 и 3 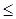 n2
n2 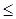 6 спектральные линии попадают в видимый диапазон, а при n2
6 спектральные линии попадают в видимый диапазон, а при n2 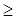 7 – в ультрафиолетовый. Эти линии называют серией Бальмера.
7 – в ультрафиолетовый. Эти линии называют серией Бальмера.
При n1 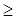 3 и любых возможных значениях n2 (n2
3 и любых возможных значениях n2 (n2 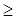 n1) все спектральные линии принадлежат инфракрасной области спектра.
n1) все спектральные линии принадлежат инфракрасной области спектра.
Но для вычисления длины волны любой линии спектра атома водорода используется одна и та же константа R, которую называют постоянной Ридберга. Это указывает на особое значение величины R для теории строения и излучения атома водорода.
Основной целью настоящей лабораторной работы является определение постоянной Ридберга экспериментальным путем.
Практическая часть
1. Мы провели градуировку монохроматора с помощью неоновой и ртутной ламп. Для каждого источника излучения мы использовали оптимальную ширину входной щели монохроматора. Усреднив данные, находим коэффициенты аппроксимирующей кривой полинома шестой степени.
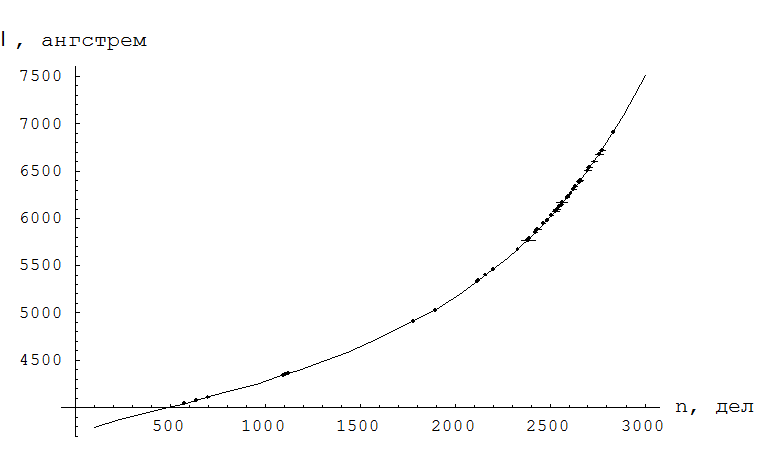
Рис. 1. Градуировочный график.
Аппроксимирующая кривая имеет следующий вид:
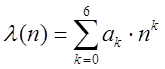 (3)
(3)
Таблица 1. Коэффициенты при степенях аппроксимирующего полинома.
| k | |||||||
| ak, Å | 7533∙10-4 | -6291∙10-7 | 6660∙10-10 | -2967∙10-13 | 6705∙10-17 | -4187∙10-21 |
Теперь для определения погрешности λ (n ±Δ n) найдем коэффициенты A maxk функции 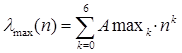 , которая аппроксимирует точки {(n j-Δ n j), λ j} (полученные для градуировки монохроматора), где n j – число делений шкалы монохроматора соответствующее длине волны λ j, а Δ n j погрешность измерения n j.
, которая аппроксимирует точки {(n j-Δ n j), λ j} (полученные для градуировки монохроматора), где n j – число делений шкалы монохроматора соответствующее длине волны λ j, а Δ n j погрешность измерения n j.
Так же найдём коэффициенты A mink функции 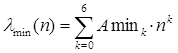 , которая аппроксимирует точки {(n j+Δ n j), λ j}.
, которая аппроксимирует точки {(n j+Δ n j), λ j}.
Таблица 2. Коэффициенты при степенях полиномов λ max(n) и λ min(n).
| k | |||||||
| A maxk, Å | 3060∙10-3 | -5032∙10-6 | 4893∙10-9 | -2457∙10-12 | 6268∙10-16 | -6186∙10-20 | |
| A mink, Å | -1529∙10-3 | 3752∙10-6 | -3558∙10-9 | 1865∙10-12 | -4924∙10-16 | 5321∙10-20 |
Так как в области измерения 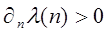 , то
, то 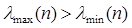 .
.
Рассмотрим окрестность некоторой точки { n 0, λ 0= λ (n 0)} (рис. 2), координата n 0 имеет погрешность Δ n 0. Необходимо оценить погрешность Δ λ 0.
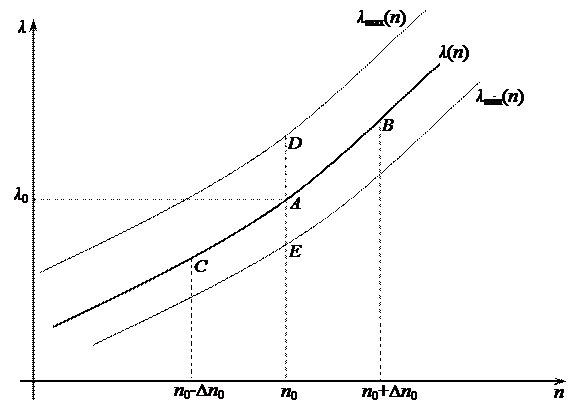
Рис. 2. Окрестность точки { n 0, λ 0}= A, где B ={ n 0+Δ n 0, λ (n 0+Δ n 0)}, C ={ n 0-Δ n 0, λ (n 0-Δ n 0)},
D ={ n 0, λ max(n 0)}, E= { n 0, λ min(n 0)}.
Пусть Δ λn – больший из отрезков AB и AC, т. е. Δ λn =max(AB, AC),
а Δ λa – больший из отрезков AD и AE, т. е. Δ λa =max(AD, AE).
Тогда Δ λ 0 найдём по формуле:
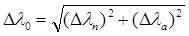 . (4)
. (4)
2. С помощью полученных зависимостей (3) и (4) найдем длины волн и их погрешности спектра атома водорода Hα, Hβ, Hγ, Hδ и сравним результаты с теоретическими.
Таблица 3. Длины волн спектральных линий атома водорода серии Бальмера.
| Hα | Hβ | Hγ | Hδ | |
| λпракт. ±Δ λпракт., Å | 6570±40 | 4864±9 | 4342±3 | 4103±5 |
| λтеор., Å |
3. Зная длины волн, рассчитаем по формуле (1) постоянную Ридберга.
Таблица 4. Постоянная Ридберга для спектральных линий атома водорода серии Бальмера.
| Hα | Hβ | Hγ | Hδ | |
| RH ±Δ RH, см-1 | 109500±700 | 109700±200 | 109670±80 | 109700±100 |
Усреднив полученные результаты, получаем:
RH =(109600±100) см-1.
Выводы:
В ходе выполнения работы мы ознакомились с линейчатым характером спектров излучения атомов, измерили длины волн серии Бальмера в видимом диапазоне спектра излучения атомарного водорода. Значения теоретических данных лежат близко к значениям полученных результатов и попадают в области их доверительных интервалов, что свидетельствует о достаточно большой точности проведенных измерений.
Также мы вычислили постоянную Ридберга RH =(109600±100) см-1. Теоретическое значение данной величины RH =109677см-1 попадает в область доверительного интервала значения, полученного экспериментально.
Литература:
1. Шпольский Э.В. «Атомная физика Т.1»: Москва-издательство «Наука», 1974. - 523 с.
2. Фаддеев М. А. “Элементарная обработка результатов эксперимента”: учебное пособие. – Нижний Новгород: издательство Нижегородского госуниверситета, 2004. – 120 с.
3. Фаддеев М.А. «Оптический спектр излучения атома водорода. Описание лабораторной работы», Нижний Новгород: ННГУ, 2002.
 2015-06-28
2015-06-28 756
756






