Для любой газофазной химической реакции,например, вида 

n1А1 + n2 А2 + n3 А3 = n4 А4 + n5 А5 + n6 А6
константу равновесия при заданной температуре в зависимости от давления вычисляют по формуле:
lg K0P,T = - 
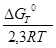
KPP,T = K0P,T (Kg)РТ,
где К0Р,Т - константа равновесия при заданной температуре и давлении, равном 0,1 Мпа;
КРР,Т - константа равновесия при заданной температуре и давлении более 0,5 Мпа;
(К¡)РТ - коэффициент, учитывающий влияние давления,
(К¡)РТ = 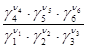 :
:
где ¡ - коэффициенты летучести исходных веществ и продуктов реакции.
Значения ¡ определяют по табличным данным для приведенных параметров p и t
(приложение).
В общем виде константу равновесия можно представить также выражением
КРР,Т = 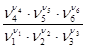 ×
× 

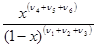 × [ (1 – х)(n1 + n2 + n3 ) + х(n4 + n5 + n6 ) ]-Dn × PDn,
× [ (1 – х)(n1 + n2 + n3 ) + х(n4 + n5 + n6 ) ]-Dn × PDn,
где х - выход продукта;
Dп = n4 + n5 + n6 - n1 - n2 - n3.
В полученное уравнение подставляют ранее найденную величину КРР,Т и решают его аналитически или графически относительно х.
 2015-06-28
2015-06-28 610
610








