Механизм и свойства люминесценции. При возбуждении Л. атом (молекула), поглощая энергию, переходит с основного уровня энергии 1 (рис. 1) на возбуждённый уровень 3. В атомных парах (Hg, Na, Cd и др.), нек-рых простых молекулах и в примесных атомах Л. может происходить непосредственно при переходе 3  1.
1.
В этом случае частоты Л. и возбуждающего света совпадают, а Л. наз. резонансной. При взаимодействии с окружающими атомами возбуждённый атом может передать им часть энергии и перейти на уровень 2, при излучат. переходе с к-рого и происходит Л., наз. спонтанной. Как правило, уровень испускания 2 лежит ниже уровня 3, часть энергии при возбуждении теряется на тепло, а длина волны испущенного света больше, чем поглощённого (стоксова люминесценция; см. Стокса правило).Возможны и процессы, когда излучающий атом получает дополнит. энергию от др. атомов; тогда испущенный квант может иметь меньшую длину волны (антистоксова Л.). Эта добавочная энергия может быть как энергией теплового движения атомов, так и результатом суммирования энергии возбуждения - передачи энергии, поглощённой неск. атомами, одному излучающему атому (см. Кооперативная люминесценция).
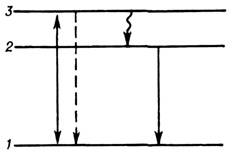
Рис. 1. Схема квантовых переходов при элементарном процессе люминесценции: 1 - основной уровень энергии; 2 - уровень испускания; 3 - уровень возбуждения. Пунктирной линией обозначен переход, соответствующий резонансной люминесценции, волнистой - безызлучательный переход.
 2015-06-24
2015-06-24 1075
1075








