Строение
Атом углерода карбонильной группы находится в sp2 -гибридном состоянии. Он соединен с тремя другими атомами (С, Н, О или С, С, О) s-связями. Остающаяся р -орбиталь перекрывается с р -орбиталью атома кислорода, находящегося в sp2 -cocтoянии, образуя p-связь. Карбонильный углерод и атомы, связанные с ним, лежат в одной плоскости.
Электронное строение карбонильных соединений показано на примере формальдегида.
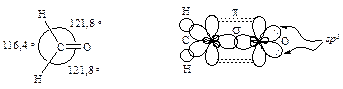
Электроны p-связи смещены в сторону более электроотрицательного атома кислорода. Дипольные моменты альдегидов и кетонов составляют (7,7-9,3)·10-30 Кл·м, что соответствует 40-50 % ионному характеру связи в карбониле.
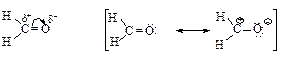
Плоская доступная для атаки карбонильная группа, содержащая двойную связь с электронодефицитным атомом углерода, более всего склонна к реакции нуклеофильного присоединения (АN).
 2015-06-24
2015-06-24 319
319








